Смывы при раке желудка
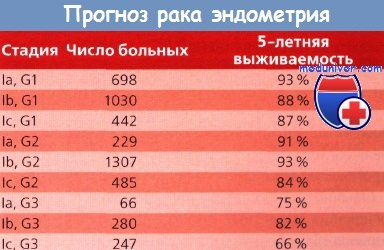
Цитология смывов брюшной полости при раке эндометрия и ее прогноз
Цитологическое исследование перитонеальной жидкости и смывов из брюшной полости определяет не только прогноз, но и стадию заболевания при злокачественных новообразованиях таза. По данным Creasman и Rutledge, у 12% больных раком эндометрия (РЭ) результат этого исследования положительный, у многих из них процесс принимает метастатический характер.
Из 167 пациенток с клинически установленным раком эндометрия (РЭ) I стадии, которым провели хирургическое лечение, злокачественные клетки в смывах были обнаружены у 26 (15,5%). Заболевание рецидивировало у 10 (38 %) из этих 26 больных по сравнению с 14 (9,9 %) из 141 с отрицательным результатом исследования смывов. При ревизии органов брюшной полости во время операции было выявлено, что из 26 пациенток с положительным результатом цитологического исследования у 13 (50 %) заболевание распространилось за пределы матки; 7 (54 %) из них умерли из-за прогрессирования заболевания.
У других 13 больных со злокачественными клетками в смывах процесс не распространялся за пределы матки; впоследствии 6 (46 %) из нихумерли по причине диссеминированного канцероматоза органов брюшной полости. В исследовании GOG, включавшем 621 пациентку, у 76(12 %) при цитологическом исследовании смывов из брюшной полости обнаружены злокачественные клетки.
Из них у 25 % имелись метастазы в лимфоузлах таза по сравнению с 7 % у женщин с отрицательным результатом исследования. Надо признать, что положительный результат цитологического теста на злокачественные клетки в смывах из брюшной полости в определенной степени согласуется с другими известными факторами прогноза, которые можно идентифицировать.
Обычно возникновение рецидивов определяют на основании известных прогностических факторов, включая данные цитологического исследования перитонеальных образцов. В случае отрицательного результата роль известных прогностических факторов остается неизменной, а в случае положительного — влияние благоприятных прогностических факторов нивелируется и ведущее значение приобретают цитологические находки.
Тем не менее Yazigi и соавт. утверждают, что цитологическое исследование смывов из брюшной полости не имеет прогностического значения. Данное исследование отражает результаты обследования и лечения больных РЭ 20 лет назад, когда такой анализ не выполняли, а ориентировались на данные только гистологического исследования. В исходной работе этих авторов многие больные были исключены из выборки по причине отсутствия морфологической документации патологического процесса. Konski и соавт. также не выявили различий в показателях выживаемости в зависимости от результатов цитологического исследования.

Однако в наблюдении этих авторов значительное количество пациенток после хирургического лечения получили ЛТ, которая могла повлиять на изучаемые показатели.
Позднее Sutton, используя многофакторный анализ, установил, что положительные результаты цитологического исследования перитонеальиых смывов — важный прогностический фактор. По данным GOG, у 25 (29%) из 86 больных с обнаруженными злокачественными клетками в промывных водах из брюшной полости наблюдались регионарные рецидивы заболевания или отдаленные метастазы по сравнению с 64 (10,4%) из 611 случаев с отрицательным результатом. Поданным ретроспективного исследования M.D. Anderson Hospital, злокачественные клетки в смывах из брюшной полости обнаружены у 28 (5 %) из 567 пациенток, при этом установлена корреляция со значительным укорочением безрецидивного периода и выживаемостью.
По данным многофакторного анализа у 477 пациенток, результат цитологического исследования был тесно связан с показателем выживаемости и продолжительностью периода без признаков прогрессирования. Grimshaw и соавт. обратили внимание на то, что из 381 больной раком эндометрия (РЭ) выживаемость 24 с положительными результатами цитологического исследования была значительно хуже, чем при отрицательных. Когда сравнили только пациенток с I хирургической стадией заболевания, то при отрицательном заключении цитологического исследования перитонеальных смывов прогноз был более благоприятным, но различие в показателях выживаемости не было статистически значимым.
Lo и соавт., сравнив выживаемость больных раком эндометрия (РЭ) I стадии с положительными (18 женщин) и отрицательными (127 женщин) результатами цитологического исследования, пришли к выводу, что рассматриваемый показатель не зависит от цитологических находок, но только при условии, если опухоль ограничена пределами матки.
Значение цитологического выявления злокачественных клеток в перитонеальных смывах для прогноза рака эндометрия (РЭ) продолжает оставаться предметом дискуссий. Исследования, обнаружившие минимальную эффективность метода или ее отсутствие, обычно охватывали ограниченное число больных раком эндометрия (РЭ) по сравнению с теми, у кого была установлена его прогностическая значимость.
Milosevic и соавт. провели обзор 17 исследований и подсчитали, что у 11 % из 3820 пациенток результаты теста были положительными. Результаты 3 самых круппых исследований (Harming, Turner, Morrow и соавт.), основанные на многофакторном анализе и охватывающие более 1700 больных раком эндометрия (РЭ), свидетельствуют о том, что наличие злокачественных клеток в смывах из брюшной полости — независимый прогностический фактор возникновения рецидивов и низкой выживаемости. Относительный риск рецидивов для всех больных составил 4,7 (ДИ 3,5— 6,3). В каждой из 3 работ установлена корреляция между положительным перитонеальным цитологическим тестом и распространением заболевания за пределы матки.
По данным многофакторного анализа, оказалось, что наличие клеток злокачественной опухоли в перитонеальных смывах остается важным прогностическим фактором даже в том случае, когда заболевание ограничено только маткой. До настоящего времени не определена оптимальная схема лечения рака эндометрия (РЭ) в случаях положительного результата этого анализа. Однако, поданным одного нерандомизированного исследования, использование интраперитонеального введения 32Р улучшает течение заболевания у больных раком эндометрия (РЭ) с опухолевыми клетками, обнаруженными в брюшной полости. Soper дополнил данные Университета Duke об использовании ;ИР у 65 больных раком эндометрия (РЭ), из которых у 53 клинически определена I стадия.
Безрецидивная выживаемость более 24 мес. равнялась 89 % у больных с I клинической стадией заболевания и 94 % — с I патоморфологической (хирургической) стадией. Каких-либо тяжелых острых и отдаленных осложнений не наблюдали, за исключением случаев, когда внутрибрюшное введение 32Р сочетали с дистанционной лучевой терапией (ДЛТ). Эта лечебная методика идентична применяемой при РЯ. Во время лапаротомии определяют объем перитонеальной жидкости, скопившейся в тазу. Если она отсутствует, то в полость таза вводят 100 — 125 мл обычного физиологического раствора. Это легко осуществимо с помощью ирригационного шприца. Затем физиологический раствор отсасывают шприцем и направляют на цитологическое исследование. Эту процедуру проводят всем больным, которых оперируют по поводу рака эндометрия (РЭ).
Классификация стадий рака эндометрия

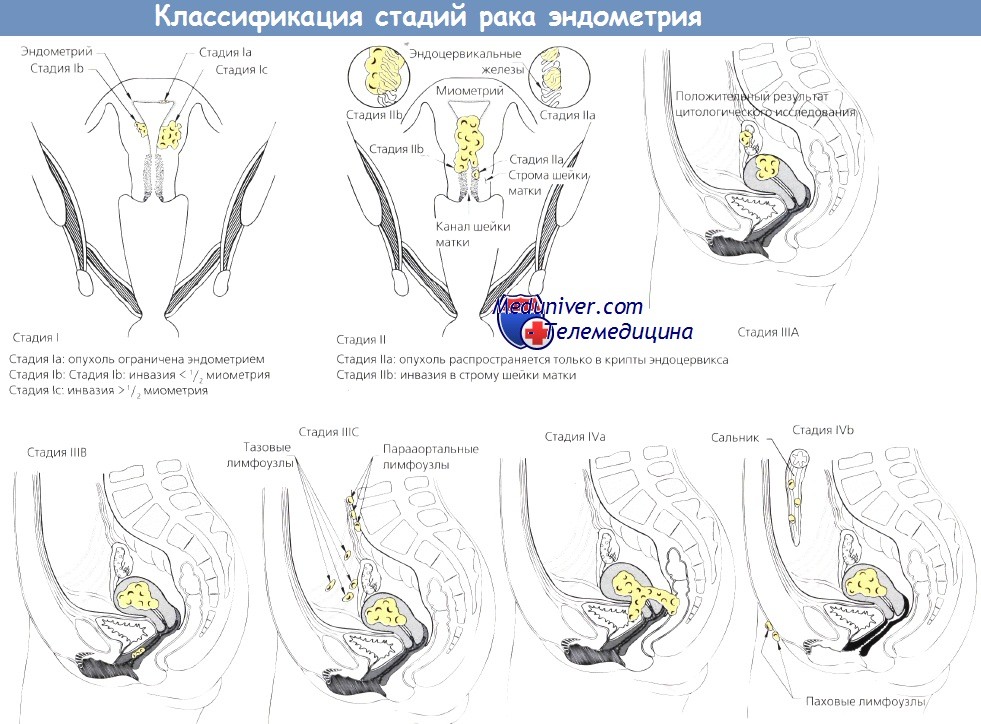
— Также рекомендуем «Метастазирование рака эндометрия в лимфоузлы и ее прогноз»
Оглавление темы «Аденокарцинома матки»:
- Секреторная аденокарцинома эндометрия
- Степень дифференцировки рака эндометрия и ее прогноз
- Стадии рака эндометрия и их прогноз
- Инвазия рака эндометрия в миометрий и ее прогноз
- Цитология смывов брюшной полости при раке эндометрия и ее прогноз
- Метастазирование рака эндометрия в лимфоузлы и ее прогноз
- Метастазирование рака эндометрия в придатки матки и ее прогноз
- Молекулярные маркеры рака эндометрия и ее прогноз
- Прогностические факторы рака эндометрия
- Лечение рака эндометрия и ее эффективность
Рак желудка – это четвертое по частоте онкологическое
заболевание в мире с общей пятилетней выживаемостью 25%. Из-за высокой агрессивности
опухоли, большая доля пациентов сталкивается с перитонеальным канцероматозом.
Он развивается у 40% пациентов – практически у каждого второго, и связан с
плохим прогнозом – пятилетняя выживаемость составляет не более 5%. Средняя
продолжительность жизни при этом составляет около 6 месяцев.
При выявлении рака желудка, канцероматоз брюшины
обнаруживается у 5-20% пациентов. И хотя хирургия является стандартом лечения
пациентов с раком желудка, выявление опухолевых очагов на брюшине ставит под
сомнение целесообразность операции.
Для улучшения результатов лечения были предложены несколько
опций – циторедуктивная хирургия + HIPEC, неоадъювантная химиотерапия (до операции),
интраперитонеальная химиотерапия.
Прежде чем перейти к возможностям лечения, я хочу остановиться на причинах
развития канцероматоза брюшины при раке желудка.
Для объяснения распространения опухолевых клеток по брюшине
и их разрастании в перитонеальные метастазы, была предложена следующая теория.
Существует 3 основных пути:
- Опухоль распространяется на серозную (внешнюю) оболочку желудка. В таких случаях раковые клетки могут отделяться спонтанно, либо в результате хирургической травмы. Японскими исследователями было показано, что при изначально отрицательных результатам, опухолевые клетки появляются в брюшной полости после операции примерно в половине случаев.
- Во многих случаях рак желудка распространяется по лимфатическим путям. Именно поэтому во время операции обязательно выполняется лимфодиссекция – удаляются лимфоузлы, потенциально содержащие метастазы. Пересечение лимфатических сосудов может приводить к излитию лимфы и опухолевых клеток в брюшную полость
- Другой путь распространения рака желудка – через кровь. Большая кровопотеря во время операции ухудшает отдаленные результаты
Циторедуктивная хирургия и HIPEC при канцероматозе рака желудка
На сегодняшний день существует несколько исследований и
центров, в котором практикуется подобная стратегия лечения. К сожалению, эти
данные получены у пациентов с небольшим распространением опухоли и заведомо
более благоприятным прогнозом. Поэтому они не могут быть применены ко всем
пациентам с раком желудка, страдающим канцероматозом брюшины.
Но положительный момент в том, что отобранные пациенты могут
получить преимущества от такого подхода. В исследованиях показано, что в
среднем пациенты живут дольше – 15 месяцев. При этом каждый пятый пациент живет
5 лет и дольше. Основными условиями успешного лечения является низкий индекс
перитонеального канцероматоза – опухолевые импланты обнаруживаются только в
небольшом количестве участков брюшной полости, и выполненная полная
циторедукция – опухолевые очаги отсутствуют после проведенной операции не
обнаруживаются. Остаточная опухоль в брюшной полости резко ухудшает прогноз –
пациенты живут 6-8 месяцев, поэтому операция не приносит эффекта.
 Сколько живут пациенты с канцероматозом при раке желудка в случае полной циторедукции (синяя линия), остаточных опухолях менее 2.5 мм (желтая), более 2.5 мм — красная линия. По горизонтальной оси — продолжитьельность жизни в годах. По вертикальной — доля пациентов, которые живы в определенный момент времени
Сколько живут пациенты с канцероматозом при раке желудка в случае полной циторедукции (синяя линия), остаточных опухолях менее 2.5 мм (желтая), более 2.5 мм — красная линия. По горизонтальной оси — продолжитьельность жизни в годах. По вертикальной — доля пациентов, которые живы в определенный момент времени
Внутрибрюшная химиотерапия при раке желудка
Большинство исследований в этой области были проведены в странах Азии. В них сравнивались эффективность добавления внутрибрюшной химиотерапии после операции и HIPEC по сравнению только с операцией и HIPEC. Анализ этих исследований не показывает улучшения общей выживаемости у пациентов, которым добавлялась интраперитонеальная химиотерапия. При этом чаще возникают осложнения – нейтропения (снижение количества лейкоцитов) и абсцессы в брюшной полости (отграниченные скопления гноя, требующие активного лечения и потенциально угрожающие жизни).
Рак желудка с позитивными смывами из брюшной полости
Во многих ведущих центрах в России и в мире обязательным
этапом перед операцией при раке желудка является взятие смывов из брюшной
полости. Этот анализ проводится во время лапароскопии и под наркозом. Бывает,
что опухолевые клетки обнаруживаются при отсутствии канцероматоза брюшины. Этот
факт говорит о плохом прогнозе – такие пациенты живут в среднем столько же,
сколько пациенты с канцероматозом брюшины. Из-за этого тактика лечения таких
пациентов может отличаться – в некоторых центрах не рассматривают операцию,
т.к. удаление желудка ухудшает качество жизни и переносимость химиотерапии. В
других клиниках проводят предоперационную химиотерапию, а затем операцию –
удаление желудка и HIPEC.
Существующие на сегодня данные говорят в пользу операции и HIPEC – такие пациенты живут дольше.
В заключение хотелось бы сказать, что стандартом лечения при
канцероматозе рака желудка остается системная химиотерапия. Операции,
внутрибрюшная химиотерапия и HIPEC остаются экспериментальными опциями, которые могут помочь
только некоторым пациентам. Окончательно решение о выборе той или иной
стратегии лечения должен принять пациент совместно с докторам, взвесив все «за»
и «против».
Один из страшных диагнозов, который с каждым годом выявляется у людей всё чаще, это рак желудка. Он представляет собой опухоль основного пищеварительного органа, которая состоит из злокачественных клеток, образовавшихся в подслизистом или слизистом его слое. Не выявленное своевременно заболевание в короткие сроки уносит жизнь человека. Только проведённая вовремя диагностика рака желудка, состоящая из целого комплекса обследований, может помочь быстро поставить правильный диагноз и провести адекватный курс лечения.
Раковое поражение стенок желудка на начальных этапах своего развития так же, как и любая другая онкология, ярко выраженных изменений в самочувствии человека не вызывает. Определённые симптомы рака желудка начинают появляться на второй стадии онкопроцесса.
Специалисты отмечают следующие самые первые признаки, по которым можно предположить, что в главном органе ЖКТ происходит образование злокачественной опухоли:
- желудочная диспепсия, выражающаяся такими негативными ощущениями, как постоянное и беспричинное вздутие живота, отрыжка или изжога, периодически возникающее подташнивание, перемежающееся временами со рвотными позывами;
- ухудшение аппетита, выраженное в непереносимости какого-либо продукта, обычно мяса;
- депрессивное состояние, постоянная вялость, ярко выраженное снижение работоспособности и проблемы со сном;
- ни чем не спровоцированный подъём температуры тела до субфебрильных (37–38°C) отметок;
- резкое похудение.
А вот боли при раке желудка появляются далеко не сразу. Первое время онкобольные испытывают только незначительные тянущие ощущения в районе эпигастрия или области поджелудочной (немного выше пупка), которые возникают вне зависимости от приёма пищи, но достаточно быстро проходят.
Если размеры злокачественного образования становятся достаточно большими, то есть опухоль начинает занимать практически всю внутреннюю поверхность пищеварительного органа, его объём уменьшается, что вызывает у больного человека быстрое наступление насыщения. Когда новообразование развивается в непосредственной близости от выходного сфинктера в кишечник, больной мучается от постоянной тяжести в животе, связанной с невозможностью прохождения через него пищевого комка, а опухоль, загораживающая соединение с пищеводом, приводит к появлению затруднения в глотательном рефлексе.
Все вышеперечисленные симптомы рака желудка, связанные с нарушением пищеварения, способствуют изменению в естественном функционировании пищеварительного тракта. Это в свою очередь вызывает ухудшение метаболизма, следствием чего становится появление некоторых внешних признаков. Основные из них это неприятный, резкий запах изо рта и постоянная обложенность языка плотным налётом желтого или сероватого цвета.
Необходимо помнить! Не стоит сразу паниковать при появлении подобной симптоматики, так как она может сопровождать и другие, менее опасные патологии ЖКТ. В первую очередь стоит обратиться к специалисту и пройти соответствующие диагностические исследования, которые помогут выявить истинную первопричину тревожной симптоматики. Затягивать с посещением гастроэнтеролога в такой ситуации категорически не рекомендуется, так как возможная онкология основного пищеварительного органа всегда склонна к стремительному развитию.
Ранняя диагностика рака желудка
Очень важно распознать развитие в основном пищеварительном органе злокачественного опухолевого процесса как можно раньше. Это имеет принципиальное значение, связанное с благоприятностью прогнозов данного заболевания – 90% 5-летняя выживаемость отмечается только в том случае, когда онкология желудка выявлена и прооперирована своевременно. На поздних же стадиях, исходя из статистических данных, она не поднимается выше 40%.
Специфическая симптоматика, сопровождающая только начинающую развиваться опухоль желудка, отсутствует. Патологическое состояние, развивающееся непосредственно на фоне протекающих в ЖКТ недугов, хронического гастрита или язвы, носящих доброкачественный характер, достаточно долго сохраняет их основные проявления. Очень часто невозможно на начальном этапе заболевания поставить диагноз рак желудка. Связано это с латентным протеканием болезни, так развитие её проходит очень медленно. В самых редких случаях о возникновении недуга может свидетельствовать непроизвольно начавшееся внутреннее кровотечение из нижних отделов ЖКТ.
Ранняя диагностика рака желудка возможна при непосредственном проведении рентгеноскопии. Эта методика благодаря своей простоте и доступности в настоящее время применяется для профилактических исследований. Чтобы получить наиболее точные результаты, для его проведения используют крупнокадровую гастро флюорографию, а сделанные при её помощи снимки анализируются двумя независимыми специалистами.
Основными тревожными признаками, считающимися на начальной стадии рака желудка подозрительными, являются:
- утолщение слизистого слоя и перестройка его рельефа на небольших участках, имеющих ограничение по площади. Их складки всегда располагаются хаотично;
- повторяющееся неоднократно на рентгеновском снимке бариевое депо (скопления выпитой пациентом перед исследованием взвеси) между утолщённых складок. Эта картина заметна даже тогда, когда между ними ещё нет явно выраженного углубления;
- частичная сглаженность выступающих возвышений слизистой, шероховатость их поверхности, отмечающаяся на небольших участках, а также зазубренность в этих местах контура желудка.
Если специалистами на рентгенограмме обнаруживаются подобные подозрительные признаки, пациенту проводят гастроскопию, которая в обязательном порядке выполняется с прицельной биопсией.
Эндоскопическая же диагностика рака желудка на ранних стадиях является достаточно непростой задачей, однако она также даёт неплохие результаты. В 18% наблюдений при помощи только этого исследования врачи с уверенностью смогли обнаружить озлокачествление слизистой желудка на начальной стадии, в 59% —заподозрить его и в 30% выявить макроскопическую картину, характерную скорее для доброкачественного процесса.
При оценке результатов, полученных во время эндоскопического исследования, раннее онкологическое заболевание желудка классифицируют по следующей картине, представленной в таблице:
| ОСНОВНЫЕ ТИПЫ ОПУХОЛИ В ЖЕЛУДКЕ | ФОРМЫ | ХАРАКТЕРИСТИКА |
| Выбухающий или выступающий | Полиповидная | Рак желудка, имеющий такую форму, выглядит как полип, сидящий на широком основании. Дефект обнаруживается при полном заполнении главного органа ЖКТ бариевой взвесью. Обычно такие полипы в желудке имеют диаметр не более 1 см и округлую или неправильно-овальную форму. Контуры его нечёткие и местами с неровными краями. Окружающая полип слизистая площадью примерно 5 см имеет изменённый рельеф, который представлен неравномерными возвышениями. |
| Бляшковидная | Дефекты, обнаруженные после тугого наполнения желудка бариевой взвесью, выглядят округлыми, не имеющими структуры выпячивания, расположившимися на рельефе слизистой. В редких случаях обнаруживается единичный дефект, имеющий чёткие и ровные границы. В центре него обычно заметно более или менее глубокое депо бария, указывающее на изъязвление поверхности опухоли. В диаметре бляшковидный рак редко достигает 2 см. | |
| Инвазивный | Блюдцеобразная | Такая форма злокачественного новообразования встречается в основном пищеварительном органе чаще всего. Основной причиной её появления становится прогрессирующее изъявление опухоли. Дефект в этом случае представляет собой округлый вырост, в некоторых случаях достигающий достаточно крупных размеров и способный прорастать в соседние органы |
| Поверхностный | Изъязвлённая (язвенно-инфильтративная) | Изъязвленный рак желудка диагностируется также очень часто, более чем в половине случаев озлокачествления пищеварительного органа. Объединяет он различные по генезу опухолевидные изъязвлённые патологии желудка, относящиеся к первично-язвенной форме. Они являются следствием прогрессирования хронической язвы или блюдцеобразного рака |
Методически правильно проведённые эндоскопическое и рентгенологическое исследования позволяют у 40-50% пациентов заподозрить раковое новообразование желудка на самой ранней стадии.
Основания для проведения диагностики
Несмотря на то, что такая опасная патология, как рак желудка, в последние годы выявляется всё чаще, многих людей интересует вопрос о том, зачем специалисты рекомендуют проходить плановые ежегодные исследования, называемые в медицинской терминологии скринингом. Объясняется это достаточно просто. Любые онкологические заболевания на ранних стадиях протекают практически бессимптомно или имеют смазанные признаки, ни в коей мере не указывающие на появление злокачественного новообразования.
Только благодаря проведению ранней диагностики имеется вероятность того, что с большой долей вероятности в основном пищеварительном органе будет обнаружена только появившаяся опухоль, а лечение рака желудка, выявленного на ранних стадиях, в 90% случаев даёт положительные результаты. Необходимо помнить и о том, что основанием для таких исследований, как гастроскопия, эндоскопия и рентгенография пищеварительных органов, позволяющих своевременно обнаружить опасную патологию ЖКТ, является появление диспепсической желудочной симптоматики.
Важно! Если неожиданно стали мучить ничем не объяснимые дискомфорт и болезненные ощущения в эпигастрии, потеря аппетита, часто повышающаяся до субфебрильных отметок температура и постоянная слабость, стоит немедленно обратиться к специалисту. Не стоит забывать, что такие симптомы являются прямым основанием для прохождения диагностика, так как они могут свидетельствовать о развитии в желудке злокачественного образования.
Методы диагностики рака желудка
Как уже говорилось, раннее выявление развития в основном пищеварительном органе злокачественного новообразования является очень важным, так как только в этом случае у 70 пациентов из 100 появляются реальные шансы на полное выздоровление. Именно поэтому специалисты рекомендуют людям из группы риска проходить скрининг. При раке желудка такое плановое ежегодное исследование, заключающееся в проведении гастроскопии, может спасти большое количество жизней.
Сама процедура не требует какой-либо специальной подготовки, проводится амбулаторно и занимает по времени не более 15 минут. В то же самое время её значение в выявлении предраковых и раковых состояний главного органа ЖКТ неоценимо. Если по её результатам у специалиста появится подозрение на развитие у человека, даже не имеющего на данный момент подозрительной симптоматики, злокачественного образования, ему будет назначена специальная диагностика рака желудка.
Она состоит из целого комплекса мероприятий, которые направлены на то, чтобы не только выявить основное заболевание, но и определить спровоцировавшие его появление причины.
Такое исследование желудка состоит из 4-х основных методов:
- Клинический. Он заключается в сборе анамнеза пациента и составления истории болезни.
- Физикальный. Включает в себя аускультацию (выслушивание возникающих в желудке звуков) и пальпацию (прощупывание больного органа). На ранних стадиях развития патологического состояния в основном пищеварительном органе с помощью этого метода можно идентифицировать отдаленные признаки заболевания. Стоит отметить, что пальпация проводится в четырёх позициях: стоя, лежа на правом боку, на левом боку и на спине.
- Лабораторный. Первым делом у больного человека проводят анализ крови на онкомаркеры. Материалом для онкомаркеров (онкомаркеры — специфические белки, которые вырабатывают только раковые клетки) служит сыворотка крови из вены. Процедуру выполняют натощак, последний приём пищи должен быть не позже чем за 8 часов до забора крови. Больные, к которым была применена радикальная терапия, прохождения этого исследования необходимо повторять через каждые три месяца. Исходя из его результатов, специалист может подтвердить или опровергнуть наличие злокачественных клеток.
- Инструментальный. Он назначается в последнюю очередь и включает в себя рентгенологическое исследование, фиброгастродуоденоскопию с биопсией для детального осмотра слизистой и взятия образца ткани на гистологию, магнитно-резонансную и компьютерную томографии.
Применение для выявления начального этапа озлокачествления основного пищеварительного органа именно этих методик позволяет обнаружить рак желудка на самых ранних стадиях. Это даёт пациентам шанс на полное выздоровление или продление жизни на максимально возможный при данном заболевании срок. Именно поэтому специалисты рекомендуют проходить их всем людям, находящимся в группе риска или имеющим предраковое состояние системы ЖКТ.
Анализы и лабораторные исследования
Онкология желудка – очень опасное состояние, при котором шансы на выздоровление или максимальное продление жизни человека напрямую зависят от своевременности его выявления. Эта патология очень трудно диагностируется на ранних стадиях и имеет настолько неспецифичные и смазанные симптомы, что поставить диагноз только по ним невозможно.
Для подтверждения болезни врачи в первую очередь всегда назначают ряд лабораторных обследований:
- общий и биохимический анализ крови при раке желудка используются в качестве дополнительных обследований, так как они не позволяют получить четкую картину болезни. Это связано с совпадениями некоторых кровяных показателей при злокачественном новообразовании и гастрите. В случае возникновения подозрений на развитие в основном пищеварительном органе процесса озлокачествления по ним в основном оценивают общее состояние человека. Несмотря на это данные лабораторные исследования имеют некоторое значение в области диагностики. Например, наблюдается сильно пониженный гемоглобин при раке желудка, так как имеются скрытые кровотечения. При распаде опухоли увеличивается показатель СОЭ, на ранних этапах длительное время он может находиться в пределах нормы. Часто у больных наблюдается стойкий лекоцитоз, при наличии метастаз в костном мозге, этот показатель в анализе крови при раке желудка увеличивается в значительной степени. Также при сдаче крови при раке желудка наблюдается снижение содержания в ней белка, повышена глобулиновая и снижена альбуминовая фракция, увеличивается количество антитромбина. После выполнения общего и биохимического анализа крови, берут анализ на раковый антиген.
- определение онкомаркеров является специфическим анализом, так как эти вещества являются продуктами, вырабатываемыми нормальными тканями в ответ на процесс жизнедеятельности опухоли. Для их обнаружения применяется не только анализ крови на онкомаркеры, но и исследование мочи онкобольного;
- исследование желудочного сока считается достаточно информативным методом, с помощью которого специалист как получает сведения о секреции и кислотности главного органа ЖКТ, так и проводит цитологический анализ его смывов, показывающий наличие мутировавших клеток. Также с его помощью обнаруживаются скрытые кровотечения;
- выявление показателей свертывающей системы крови необходимо для проверки такого её показателя, как тромбообразование. При любой форме рака желудка оно бывает усиленным, поэтому повышение ПТИ (протромбинового индекса), ТВ (тромбинового времени) и АЧТВ (активированного частичного тромбопластинового времени) указывает на развитие в желудке злокачественного процесса;
- исследование кала на скрытую кровь также является обязательным, так как благодаря ему выявляются даже минимальные кровопотери, возникшие в нижних отделах ЖКТ. Если у больного присутствует рвота, рвотные массы также обследуют на этот показатель.
Необходим при подозрении на развитие в желудке злокачественного процесса и генетический анализ. С его помощью обнаруживают мутированный ген CDH1, который свидетельствует о наследственной предрасположенности человека к раку желудка. Такой метод лабораторной диагностики применяют у пациентов, в семьях которых отмечались случаи развития злокачественного новообразования в главном органе ЖКТ.
Диагностика рака желудка с метастазами 4 стадии
Запущенный этап развития заболевания характеризуется прорастанием опухоли во все слои пищеварительного органа, а также распространением мутировавших клеток по организму. Для того, чтобы выявить злокачественное поражение желудка на поздней стадии, помимо основных необходимы и дополнительные методы диагностики. Среди них основным является лапароскопия, проводимая под непосредственным контролем УЗИ.
Данное диагностическое исследование является малоинвазивной операцией, выполняемой под анестезией. Она проводится через проколы в брюшной стенке, в которые вводят камеру. При помощи этого способа у специалиста появляется возможность обнаружить прорастание опухоли в близлежащие ткани и распространение метастазов в печень и брюшину.
Обычно такая диагностика рака желудка 4 стадии позволяет специалисту выявить у пациента следующие неприятные признаки:
- мутировавшие клеточные структуры находятся в непосредственной близости от соседних органов;
- новообразование распространилось на близлежащие лимфоузлы;
- опухолевый процесс начинает развиваться в рядом расположенных внутренних органах.
Метастазы при 4 стадии данного патологического состояния могут распространяться не только через лимфу, поражая лимфатические узлы, но и гематогенным (через кровеносное русло) или имплантационным (при близком контакте внутренних органов) путями.
Дифференциальная диагностика рака желудка
В связи с тем, что выявление злокачественного новообразования в основном пищеварительном органе всегда затрудняется сходством его клинических признаков с некоторыми заболеваниями внутренних органов, всегда должна проводиться дифференциальная диагностика рака желудка. Она позволяет исключить некоторые предраковые заболевания, к которым относятся язва, полипы атрофический и хронический гастриты. Это необходимо в связи с тем, что все они имеют сходные признаки.
Для правильного выявления патологического состояния основное значение имеет адекватно собранный анамнез и полное обследование не только ЖКТ, но и других органов.
Дифференциальная диагностика рака желудка проводится с применением следующих методов обследования:
- эндоскопия с одновременным взятием биопсии;
- гастробиопсия;
- рентгенологическое исследование;
- развёрнутый анализ крови.
После того, как специалист диагностировал поразившую человека патологию, он подбирает адекватную тактику лечения. Этот недуг, несомненно, очень опасен и процент полного излечения пациентов достаточно низкий, но все неблагополучные прогнозы относятся непосредственно к тем людям, которые своё здоровье и жизнь доверяют явным шарлатанам или специалистам с минимальным опытом и низкой квалификацией.
Стоит помнить о том, что от злокачественных процессов, протекающих в основном пищеварительном органе, можно или полностью избавиться, или продлить и облегчить жизнь онкобольного. Для этого необходимо совсем немного – найти опытного онколога, который способен оказать результативную помощь на любой стадии заболевания.
Информативное видео
Будьте здоровы!

