Пищеводные анастомозы при раке желудка
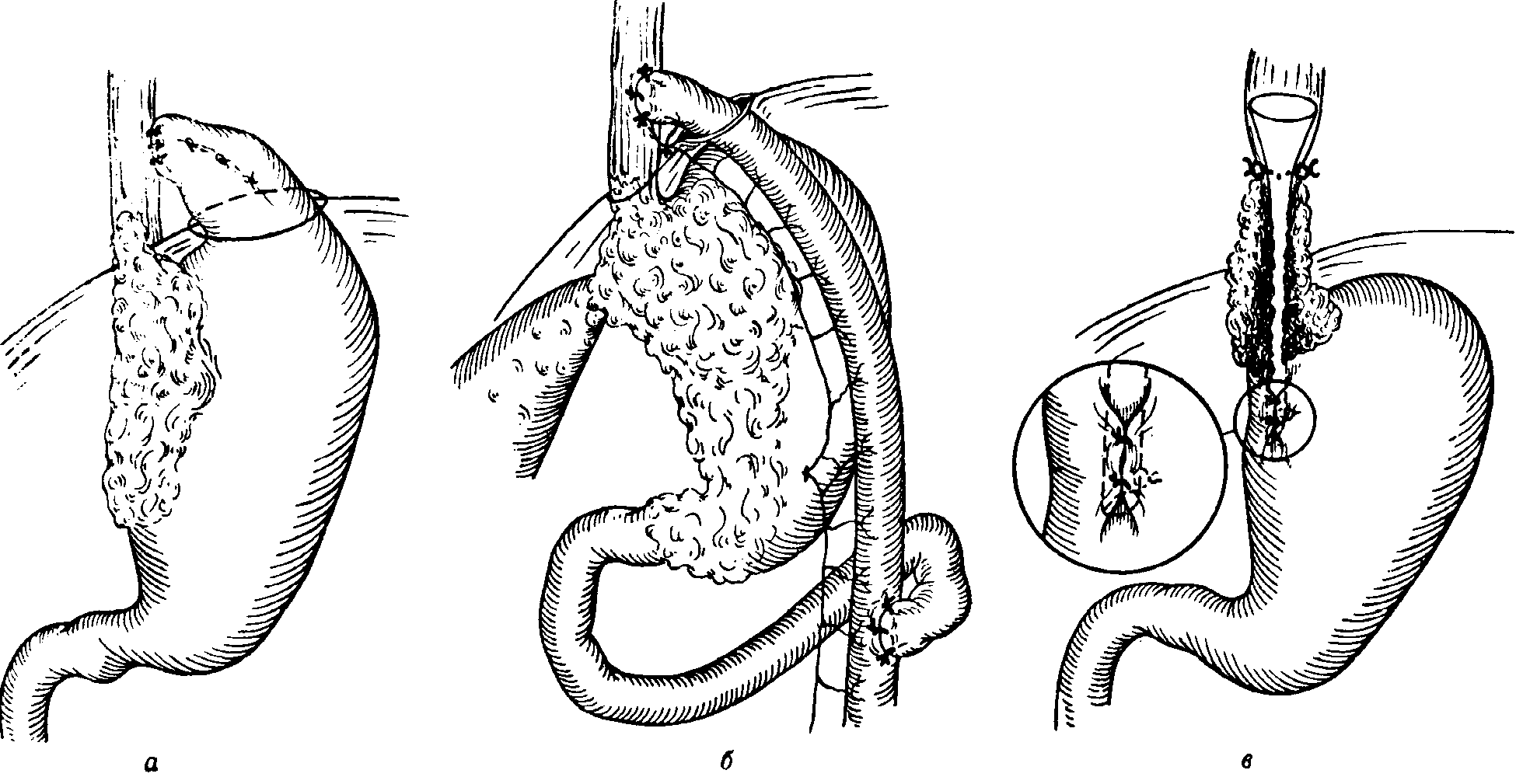

Рис.
3-169.
Паллиативные вмешательства при полностью
стенозирующих просвет нерезецируемых
опухолях кар-дии. а)
Обходной анастомоз между пищеводом и
дном желудка; б)
анастомоз между пищеводом и У-образной
петлей тонкой кишки по
Roux;
в) введение
синтетической трубки через стенозированный
опухолью пищевод
операций наилучшее восполнение этой
функции осуществляется по методу
Seoи его сотрудников(1952).При этой операции
используются участки толстой и
подвздошной кишок, которые вставляются
между пищеводом и двенадцатиперстной
кишкой. Это вмешательство имеет те
недостатки, что продолжительность
операции намного увеличивается и
возрастает возможность нарушения
стерильности. Опыт показывает, что
резервуарная функция развивается
раньше или позже в отделе кишки, идущей
от пищевода. На протяжении нескольких
лет просвет тонкой кишки может увеличиться
в несколько раз.
На практике можно считать, что любая
реконструктивная операция является
хорошей, при которой достаточно
используется и улучшается резорбционная
поверхность тонкой кишки, а также
препятствуется возможность возникновения
регургитации щелочного содержимого
кишки в пищевод. Эти два условия в
основном выполняются при тех оперативных
вмешательствах, когда между пищеводом
и двенадцатиперстной кишкой в
изоперистальтическом направлении
помещают петлю кишки (тонкой кишки,
подвздошно-толсто-кишечный сегмент).
К этому следует добавить, что вставляемая
часть петли кишки должна быть достаточной
длины. Наряду с этим бывает, что проходят
многие годы после операции и больные,
у которых двенадцатиперстная кишка и
первые сантиметры тонкой кишки не
служат резорб-ционной поверхностью,
несмотря на это находятся в отличном
состоянии.
В литературе можно встретить большое
число описаний состояния «отсутствующей
емкости желудка» после гастрэктомии.
Автор этих строк считает себя вправе,
исходя из собственного опыта, на основе
более чем 180операций,
высказать мнение о том, что больные
даже после тотальной гастрэктомии
могут благополучно существовать и быть
работоспособными, если нет рецидива
канцероматозного процесса и реконструкция
пищеварительного тракта выполнена по
всем правилам.
Во время операции у больного, страдающего
полной и частичной непроходимостью
пищи по пищеводу вследствие ракового
процесса, радикальная операция может
оказаться невыполнимой и возникает
вопрос об иноперабильнос-ти. Следует
во всех случаях все же пытаться
восстановить проходимость пищи. Из
большого числа имеющихся методов, о
которых будет сказано дальше; надо
выбирать наиболее подходящие для
каждого данного конкретного случая.
Паллиативная резекция кардии
Может оказаться, что кардия поражена
первичным капцероматозным процессом,
который, однако, занимает небольшую
поверхность и не
связан с окружающими тканями, но имеются
уже отдаленные метастазы. В таких
случаях наиболее подходящим паллиативным
вмешательством является резекция
карциномы, нарушавшей пассаж пищи. При
этом, само собой разумеется, что удаляется
большой и малый сальник, а также
селезенка. Методика осуществления
паллиативной резекции и реконструкции
описана на стр. 214.
Обходной анастомоз между пищеводом и желудком
При отсутствии
поражения опухолевым процессом дна
желудка и верхней трети большой кривизны
выводят дно желудка через отдельно
наложенное вблизи от хиатуса пищевода
отверстие в грудную полость и накладывают
эзофаго-фундостомию по типу «бок в бок»
(рис.
3-169(1).
Обходной анастомоз между пищеводом и y-образной тонкокишечной петлей по Roux
Наложение обходного анастомоза с
использованием петли тонкой кишки по
Rouxвозможно даж^
ч^гда, когда весь желудок поражен
карциномой и на его поверхности нет
свободного от опухоли места. Этот
обходной анастомоз может обеспечить
прохождение пищи в тех критических
ситуациях, когда такие паллиативные
меры, как введение синтетической трубки
в просвет пищевода или гастростомия
невозможны(рис. 3-1696).
Петлю тонкой кишки формируют,
какэто-иЗло-жено на стр. 191.При этом петля кишки протягивается
вверх, в грудную клетку, к пищеводу,
часто даже впереди поперечноободочной
кишки и желудка через отдельное отверстие
в диафрагме. Можно не опасаться, что в
послеоперационный
период возникнет расширение желудка
или толстой кишки, которое могло бы
вызвать сдавливание петли по
Rouxи нарушить
прохождение по ней пищи. Такому расширению
препятствует опухолевая инфильтрация
и делает его практически невозможным.
Проведенная через прорезанное в
диафрагме круглое отверстие тонкая
кишка протягивается вверх в грудную
полость. Между боком расширенного
пищевода и концом петли тонкой кишки
по Rouxнакладывается анастомоз по типу «бок
в конец». Для наложения анастомоза
пищевод вскрывается в поперечном
направлении, а швы накладываются по
методике, как это изложено на стр.
193.
Нередко бывает, однако, проще пересечь
в пределах здоровых тканей пищевод в
поперечном направлении, дистальную
культю зашить, а анастомоз наложить по
изложенной выше методике между оральным
концом и петлей по Roux.
Протягивание синтетической трубки через сужение пищевода, вызванное раковой опухолью
Для введения в суженный опухолевым
процессом пищевод синтетической трубки
должно быть достаточное, свободное от
опухоли место в стенке желудка для
гастротомии. После вскрытия просвета
желудка через это отверстие и кардию
проводят узкий буж или соответствующий
зонд, конец которого при его продвижении
вверх выйдет из полости рта. К выведенному
из полости рта концу бужа или зонда
анестезиолог прикрепляет синтетическую
трубку, которая затем, как это описано
на стр. 207,протягивается
через суженный карциномой пищевод.
Нижний конец трубки прикрепляется
1—2швами к малой кривизне желудка(рис. 3-169в).Гастротомический разрез
зашивается двухрядным швом.
172
Соседние файлы в папке 0912
- #
- #
- #
- #
- #
- #
- #
- #
- #
- #
- #
Изобретение относится к медицине, онкологии, может быть использовано при лечении рака желудка в зоне пищеводных анастомозов. При паллиативном лечении рецидива рака желудка на первом этапе выполняют аргоноплазменную коагуляцию рецидивной опухоли с проведением 2-8 сеансов реканализации 2 раза в неделю с интервалом 3-4 дня. Используют следующие параметры коагуляции: мощность высокочастотного тока 60-80 Вт, скорость подачи аргона 2,0-2,2 л/мин, объем вводимого газа в течение одного сеанса — не более 2 л, продолжительность каждой апликации не более 3 с. При продолженном росте опухоли на втором этапе сеансы проводят на протяжении всей жизни пациента с интервалом 2-4 недели при тех же параметрах коагуляции. Способ позволяет стойко восстановить просвет анастомоза, проводить реканализацию в амбулаторных условиях, минимизировать риск опасных для жизни осложнений.
Рецидив рака желудка в зоне пищеводно-желудочного и пищеводно-кишечного анастомозов возникает у 9,4-18,4% больных [Странадко Е.Ф. О рецидиве рака в области пищеводно-кишечного и пищеводно-желудочного анастомозов. // Сов. медицина. — 1979. — 8. — С.38-42; Щепотин И.Б., Киркилевский С.И., Окулов Л.В., Задорожный А.А. Индивидуализированный подход к лечению рецидивов рака желудка. // Клин. хирургия. — 1989. — 5 (569). — С.17-19; Zieren H.U., Muller J.M., Rawalski A., Pichlmaier J. Wert schematisierter Nachsorgeuntersuchungen nach Resekdon eines Magenkarzinoms. //DMW: Dtsch. Med. Wochenschr. — 1995. — 120, №10. — С.315-320], причем 60% опухолей диагностируются в 1-й год после операции, являясь следствием неадекватности ее объема [Пирогов А.И., Плотников В.И., Гаджиев К.М., Давыдов М.И. Рецидив рака в анастомозе после гастрэктомии и проксимальной резекции желудка. //Хирургия. -1980. — 8. — С.69-74]. Даже в специализированных клиниках только у 45% пациентов повторные вмешательства носят радикальный характер, обеспечивая 5-летнюю выживаемость после их выполнения на уровне 26,4% и приближаясь по своей эффективности к результатам хирургического удаления первичной опухоли [Тер-Аванесов М.Д., Давыдов М.И., Стилиди И.С. и др. Хирургическое лечение рецидивов кардиоэзофагеального рака. // В сб.: V Ежегодная Российская онкологическая конференция, 27-29 ноября 2001 г. — Москва. — 2001. — С.75-76]. У остальных больных выполняются шунтирующие операции или накладываются эзофагогастро(-еюно)стомы либо лечение ограничивается симптоматической терапией. Летальность после паллиативной хирургии составляет 26,6%, средняя продолжительность жизни пациентов — около 7 месяцев, а при симптоматической терапии — 3-4 месяца [Тер-Аванесов М.Д., Давыдов М.И., Стилиди И.С. и др. Хирургическое лечение рецидивов кардиоэзофагеального рака//В сб.: V Ежегодная Российская онкологическая конференция, 27-29 ноября 2001 г. — Москва. — 2001. — С.75-76; Щепотин И.Б., Киркилевский С.И., Окулов Л.В., Задорожный А.А. Индивидуализированный подход к лечению рецидивов рака желудка//Клин. хирургия. — 1989. — 5 (569). — С.17-19]. Таким образом, рассчитывать на относительно успешное лечение может лишь весьма ограниченный контингент больных.
Основная причина смерти оперированных больных — генерализация опухолевого процесса. Пациенты, получающие симптоматическую терапию, погибают в большинстве своем от выраженного нарушения гомеостаза в организме из-за нарастающей дисфагии, обусловленной злокачественным стенозом анастомоза. Эти обстоятельства определяют актуальность проблемы разработки альтернативных хирургическому паллиативных методов лечения, не уступающих по эффективности оперативному пособию, но без характерных для него фатальных осложнений.
Учитывая, что как первичные, так и рецидивные опухоли этой локализации резистентны к лучевой и химиотерапии, наиболее перспективным представляется эндоскопический метод, обеспечивающий возможность использования различных способов термической абляции очагов злокачественного стеноза. Применение высокоэнергетического лазерного излучения, основанного на принципе фотокоагуляции и испарения опухолевой ткани, позволяет в процессе нескольких эндоскопических сеансов реканализировать анастомоз в 93% случаев, но клинический эффект устранения дисфагии отмечают только 74% больных [Spinelli P., Mancini A., Dal Fante M. // Semin. Surg. Oncol — 1995. — Vol.11. — P.307-318]. Вместе с тем, эта методика имеет такие недостатки, как задымление рабочего поля, выраженный отек тканей в зоне действия теплового луча, трудность определения осевой линии анастомоза при выраженном стенозе его просвета, невозможность контроля глубины термического ожога, недооценка которых может привести к таким грозным осложнениям, как кровотечение и перфорация, встречающееся в 2-6% случаев [Mitty R.D., Cave D.R., Birkett D.H. One-stage retrograde approach to ND:YAG laser palliation of esophageal carcinoma.//Endoscopy. — 1996. — Vol.28, No4. — P.350-355; Bisgaard Т., Wojdemann M., Heindorff H. et al. Nonsurgical treatment of esophageal perforations after endoscopic palliation in advanced esophageal cancer.//Endoscopy. — 1997. — 29. — P.155-159]. Предлагаемое в литературе комбинированное использование таких методов лечения как бужирование, баллонная дилатация, лазерная фотокоагуляция и эндопротезирование пищеводных анастомозов позволяет повысить эффективность восстановления перорального питания до 86,8%, но при этом тяжелые осложнения возникают в 15% случаев с летальным исходом у 6% больных [De Palma G.D., Sivero L., Galloro G. et al. La palliazione endoscopica della disfagia secondaria a recidiva dell’area anastomotica dopo resezione esofagea e gastrectomia totale per carcinoma. // Minerva chir. — 1998. — 53, №10. — P.781-785]. Существенными недостатками саморасправляющихся стентов является довольно частая их миграция за пределы пищеводных анастомозов [Garsia A., Costilla S., Magadan V. et al. Palliative treatment of esophagel strictures with covered and uncovered selfexpanding metallic stents. // Abstr. 10th European Congress of Radiology — ECR’97. Vienna. Austria. March 2-7. 1997. — Amsterdam. 1997. — P.122] и обрастание стента опухолью [Toikkanen V.J., Nemlander A.T., Ramo O.J. et al. Expandable metallic stents in the management of malignant oesophageal obstruction. // Ann. chir. et gyneacol. — 2000. — 89, №1. — P.20-23].
В конце 90-х годов прошлого столетия в клиническую практику внедрен метод аргоноплазменной коагуляции, принцип действия которого основан на передаче энергии тока высокой частоты от источника к рабочему полю бесконтактным способом при посредстве электропроводящего газа — аргона (аргоновая плазма), что позволяет получать гомогенные зоны коагуляции и десикации (высушивания) при контролируемой глубине термического повреждения тканей, не превышающей 3 мм, что значительного снижает риск перфорации полого органа [Грунд К.Е., Циндель К., Фарин Г. Применение метода аргоноплазменной коагуляции (АРС) в «гибкой» эндоскопии. // Немецкий еженедельный медицинский журнал. — 1997. — 122. — С.432-438]. Хотя метод и получил распространение в онкологии, но в доступной литературе мы не нашли работ, раскрывающих его возможности в паллиативном лечении рецидивов рака желудка, возникающих в области пищеводных соустий.
Наиболее близким к заявленному способу является метод лазерной фотокоагуляции, обеспечивающий в большинстве случаев реканализацию злокачественных стенозов пищеводных анастомозов [Spinelli P., Mancini A., Dal Fante M. // Semin. Surg. Oncol. — 1995. — Vol.11. — P.307-318]. Вместе с тем, вышеотмеченные недостатки метода при достаточно высоком риске опасных для жизни осложнений, а также необходимость проведения сеансов лечения в условиях стационара, дороговизна оборудования и мероприятий по соблюдению техники безопасности его эксплуатации существенно ограничивают широкое применение термальных лазеров в клинической практике.
Техническим результатом предлагаемого способа паллиативного лечения рецидива рака желудка в зоне пищеводных анастомозов является: 1) стойкое восстановление просвета анастомоза путем деструкции опухоли с обеспечением возможности перорального питания на протяжении всей жизни больного; 2) осуществление возможности проведения лечебных процедур в амбулаторных условиях на основе минимизации риска опасных для жизни осложнений. Это достигается за счет двухэтапного применения метода эндоскопической аргоноплазменной коагуляции.
Для аргоноплазменной коагуляции применялось оборудование фирмы ERBE, состоящее из блока контроля и управления аргонопитанием — АРС 300, генератора высокочастотного тока ICC 300 и гибкого зонда диаметром 2,3 мм, обеспечивающего передачу энергии тока к обрабатываемой поверхности. Доставка зонда к рецидивной опухоли осуществлялась через инструментальные каналы фиброэндоскопов фирмы Olympus серии OES моделей XQ30, Е и видеоэндоскопа V70. Использовались следующие рабочие параметры коагуляции: мощность тока 60-80 Вт, скорость подачи аргона 2,0-2,2 л/мин, объем вводимого газа в течении одного сеанса не превышал 2 л с периодической его эвакуацией в целях профилактики перерастяжения полых органов, продолжительность каждой аппликации — не более 3 секунд.
Лечебные сеансы, в зависимости от тяжести состояния пациентов, проводились в стационаре или в амбулаторных условиях. За 30 минут до эндоскопической процедуры, в целях снижения перистальтической активности, больным подкожно вводилось 0,5 мл 0,1% раствора атропина. В качестве местной анестезии глоточного кольца применялся 10% раствор лидокаина.
Процесс лечения состоял из двух этапов. На первом — аргоноплазменная коагуляция рецидивной опухоли осуществлялась в «интенсивном» режиме: сеансы проводились 2 раза в неделю с интервалами в 3-4 дня. Если просвет анастомоза позволял провести эндоскоп, то лечебное пособие начиналось от каудального края рецидива по направлению к краниальному (ретроградно). При диаметре стеноза меньшем, чем диаметр эндоскопа, разрушение опухоли осуществлялось ортоградно. По достижению позитивных результатов — деструкции опухоли, ликвидации стеноза и восстановления глотательной функции — больной переводился на диспансерное наблюдение, в ходе которого 1 раз в 3-4 недели выполнялась контрольная эндоскопия с обязательным забором материала на морфологическое исследование. При обнаружение очагов продолженного роста опухоли проводился второй этап паллиативного лечения, предусматривающий фактически пожизненное выполнение сеансов аргоноплазменной коагуляции в «поддерживающем» режиме, осуществляемых с интервалом в 2-4 недели, в зависимости от темпа роста местного рецидива.
По разработанной методике в клинике ГУН НИИ онкологии им. проф. Н.Н.Петрова Минздрава России с 2000 по 2003 годы проведено паллиативное лечение 32 больных с рецидивами рака желудка в зонах пищеводных анастомозов. Мужчин было 25, женщин — 7. Возраст больных находился в диапазоне от 42 до 78 лет, в среднем — 59,7.
Жалобы на дисфагию различной степени выраженности предъявляли 30 больных. При инструментальном обследовании у каждого четвертого пациента выявлены отдаленные метастазы. Гистологическое строение рецидива соответствовало первичной опухоли: в 26 случаях установлена аденокарцинома и в 6 — перстневидноклеточный рак. У 9 больных (после проксимальной резекции желудка) рецидив рака диагностирован в зоне эзофагогастроанастомоза, у 23 (после гастрэктомии) — в области эзофагоэнтероанастомоза. Все рецидивы возникли в первые 3 года после операции. Наибольшее их число диагностировано в 1-ый год наблюдения — у 20 (62,5%) больных, в сроки от 1 до 2 лет — у 7 (21,9%) пациентов и от 2 до 3 лет — у 5 (15,6%) больных.
Размеры образования до 3 см были у 14 (43,7%) пациентов, от 3 до 6 см — у 15 (46,9%) и только у 3 (9,4%) больных рецидив распространялся вдоль пищевода на расстояние от 6 до 9 см.
7 (21,9%) рецидивов были экзофитной формы, 15 (46,9%) — эндофитной и 10 (31,2%) — имели смешанную форму роста. У 11 пациентов опухоль охватывала до половины окружности анастомоза, но в два раза чаще (в 21 случае) — поражала 3/4 окружности или имела циркулярный характер. Выявленный рецидив не вызывал сужения просвета анастомоза лишь у 2 больных. У 10 пациентов анастомоз был стенозирован до диаметра 9 мм, у 5 больных — от 8 до 6 мм и в 15 случаях просвет искусственного соустья составлял лишь 5-3 мм.
В общей сложности выполнено 330 сеансов эндоскопической аргоноплазменной коагуляции: 138 (41,8%) — на первом и 192 (58,2%) — на втором этапе, необходимость в проведении которого возникла у 24 больных. В период «интенсивного» курса проводилось от 1 до 8 сеансов эндоскопического вмешательства (в среднем — 4,3), при этом 79 (57,2%) сеансов произведены в условиях стационара и 59 (42,8%) — в амбулаторных условиях.
Непосредственные результаты оценивались по следующим критериям: «хороший» — полная местная деструкция рецидива с устранением стеноза, либо восстановлением просвета анастомоза до диаметра не менее 12 мм (наблюдался в 25 случаях); «удовлетворительный» — достигнут частичный эффект, проявившийся в разрушении более 50% объема опухоли с восстановлением просвета анастомоза до 9-11 мм (установлен в 7 случаях). Таким образом, в ходе первого этапа лечения у всех 32 больных отмечен положительный эффект. Период стабилизации процесса составил в среднем 55 дней.
Максимальное число выполненных «поддерживающих» сеансов у одного больного было 18 (в среднем — 8,1), при этом в большинстве случаев они осуществлялись амбулаторно — 158 (82,3%) и только 34 (17,7%) — в стационаре.
Безопасность метода подтверждена как отсутствием местных осложнений в виде интенсивных кровотечений или перфораций стенок органа, так и хорошей переносимостью сеансов лечения больными без кризисных ситуаций со стороны сердечно-сосудистой системы.
Максимальный срок наблюдения составил 14 месяцев. За прошедший период умерло 18 пациентов — все от генерализации опухолевого процесса, при этом только у одного из них не удалось сохранить глотательную функцию на уровне, необходимом для поддержания гомеостаза в организме, так как тяжесть состояния пациента не позволяла выполнять процедуры эндоскопической реканализации. 6 месяцев пережили 25 больных, 9 месяцев — 11 больных и 12 месяцев — 4 пациента. Средняя продолжительность жизни составила 8 месяцев. 14 больных живы и продолжают получать паллиативное лечение по разработанной программе в амбулаторных условиях.
Таким образом, изобретательский уровень предлагаемого способа паллиативного лечения рецидива рака желудка в зонах пищеводных анастомозов подтверждается тем, что во всех случаях полностью (78,1%) или частично (21,9%) достигнут регресс опухоли при отсутствии опасных для жизни осложнений и со стойким поддержанием перорального питания на протяжении всей жизни у 96,9% пациентов, что превышает аналогичные показатели при методике лечения с использованием термальных лазеров. Средняя продолжительность жизни пациентов, составившая на момент оценки 8 месяцев, также оказалась несколько выше, чем после паллиативных хирургических вмешательств.
В качестве примеров и для подтверждения условия «промышленная применимость» приводим следующие клинические наблюдения.
Пример 1. Больной Д.А.А., 63 г. Жалобы на дисфагию твердой пищи. Клинический диагноз: Рак желудка. 19.11.2002 г. операция — гастрэктомия. 28.04.2003 г. — рецидив в зоне эзофагоэнтероанастомоза протяженностью 4 см и стенозом просвета до 5 мм в диаметре. При гистологическом исследовании — аденокарцинома. С 04.05.2003 г. по 23.05.2003 г. в условиях стационара проведено 5 сеансов эндоскопической аргоноплазменной коагуляции рецидивной опухоли в «интенсивном» режиме. Осложнений нет. Результат — просвет анастомоза реканализирован до диаметра 13 мм, дисфагия устранена. Период стабилизации — 41 день. С 03.07.2003 г. по 25.03.2004 г., в связи с продолженным ростом опухоли, в амбулаторных условиях произведено 12 сеансов эндоскопической аргоноплазменной коагуляции в «поддерживающем» режиме. Осложнений нет. Жалоб на дисфагию не предъявляет.
Пример 2. Больная Б.Г.Ф., 67 лет. Жалобы на дисфагию твердой пищи. Клинический диагноз: Рак кардиального отдела желудка. 18.02.2001 г. операция — экстирпация желудка с резекцией нижнегрудного отдела пищевода. 28.01.2003 г. — рецидив в зоне эзофагоэнтероанастомоза протяженностью 5 см и стенозом просвета до 6 мм в диаметре. При гистологическом исследовании — аденокарцинома. С 28.01.2003 г. по 25.02.2003 г. в амбулаторных условиях проведено 7 сеансов эндоскопической аргоноплазменной коагуляции рецидивной опухоли в «интенсивном» режиме. Осложнений нет. Результат — просвет анастомоза реканализирован до диаметра 12 мм, дисфагия устранена. Период стабилизации — 56 дней. С 22.04.2003 г. по 21.11.2003 г., в связи с продолженньм ростом опухоли, в амбулаторных условиях произведено 10 сеансов эндоскопической аргоноплазменной коагуляции в «поддерживающем» режиме. Осложнений нет. 22.12.2003 г. (через 11 месяцев после начала паллиативного лечения) больная умерла вследствии генерализации опухолевого процесса при сохраненной возможности перорального питания.
Пример 3. Больной П.Н.П., 44 г. Жалобы на дисфагию твердой и полутвердой пищи. Клинический диагноз: Кардиоэзофагеальный рак. 29.10.2002 г. операция — проксимальная резекция желудка и нижнее грудного отдела пищевода. 25.02.2003 г. — рецидив в зоне эзофагогастроанастомоза протяженностью 6,5 см и стенозом просвета до 4 мм в диаметре. При гистологическом исследовании — аденокарцинома. С 25.02.2003 г. по 24.03.2003 г. в условиях стационара проведено 6 сеансов эндоскопической аргоноплазменной коагуляции опухоли в «интенсивном» режиме. Осложнений нет. Результат — просвет анастомоза реканализирован до диаметра 13 мм, дисфагия устранена. Период стабилизации — 64 дня. С 27.05.2003 г. по 15.10.2003 г., в связи с продолженным ростом опухоли, в амбулаторных условиях произведено 8 сеансов эндоскопической аргоноплазменной коагуляции в «поддерживающем» режиме. Осложнений нет. 10.11.2003 г. (через 8 месяцев после начала паллиативного лечения) больной умер вследствии генерализации опухолевого процесса при сохраненной возможности перорального питания.
Способ паллиативного лечения рецидива рака желудка в зоне пищеводных анастомозов, включающий применение внутрипросветной хирургии, отличающийся тем, что на первом этапе выполняют аргоноплазменную коагуляцию рецидивной опухоли с проведением 2-8 сеансов реканализации 2 раза в неделю с интервалом 3-4 дня при следующих параметрах коагуляции: мощность высокочастотного тока 60-80 Вт, скорость подачи аргона 2,0-2,2 л/мин, объем вводимого газа в течение одного сеанса — не более 2 л и продолжительность каждой аппликации — не более 3 с, в случаях продолженного роста рецидивной опухоли, регистрируемого при контрольных эндоскопиях, на втором этапе лечения проводят сеансы аргоноплазменной коагуляции на протяжении всей жизни пациента с интервалом в 2-4 недели при тех же параметрах коагуляции.


