Цитологическая диагностика рака желудка
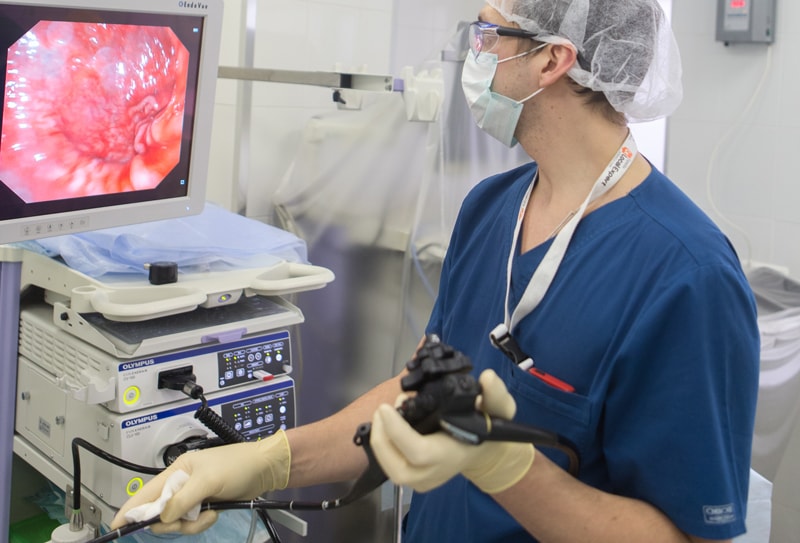
В числе методов ранней диагностики рака желудка в последние годы все чаще упоминается цитологический. Наши наблюдения безусловно подтверждают высказывание Н. А. Краевского, что «…в ряде случаев этот безопасный метод, позволяющий быстро получить тканевый субстрат и так же быстро его обработать, может оказать неоценимую услугу клинике». Принципиально новым шагом в цитологической диагностике заболеваний желудка является в последние годы широкое применение эндоскопических инструментов из волоконной оптики и метода прицельного получения материала для этого исследования.
До настоящего времени нет единой классификации цитологической картины, обнаруживаемой при патологии различных органов, в том числе желудка. Наиболее широкое распространение получила классификация Papanicolau и Cooper (1947), которые в зависимости от степени изменений клеток распределили их на пять классов. К I классу они отнесли нормальные клетки без признаков атипии, ко II — клетки с нерезкими изменениями без признаков озлокачествления, к III — клетки с более отчетливыми изменениями, уже напоминающие злокачественные, но без убедительных данных, к IV — клетки, характеризующиеся явными признаками малигнизации при небольшом количестве патологических элементов в мазке, к V классу — определенно злокачественные клетки. Однако одним из существенных недостатков этой классификации является отсутствие четкой морфологической характеристики каждого класса, что позволяет довольно свободно трактовать обнаруженные изменения клеток.
Накопив определенный опыт в области цитологических исследований желудка, опираясь на результаты сопоставления характера изменений клеток с данными цитологического исследования слизистой оболочки желудка, определения содержания ДНК в ядрах эпителиальных клеток и данных кариометрии, мы решили восполнить пробел в указанной классификации.
Опыт проведенной работы показал, что распределить разнообразные изменения клеток, которые обнаруживались при исследовании препаратов, представляет иногда значительные трудности. Поэтому мы полагаем, что целесообразно ввести подразделение на I—II, II—III, III—IV классы, подразумевая наличие при этом клеток, относящихся как к одному, так и к другому классу. Первая цифра отражает преобладание в препаратах клеток данного класса. При наличии клеток III—IV класса следует говорить о подозрении на рак.
Как показывает опыт, успех цитологической диагностики рака желудка зависит от двух главных причин: получения в достаточном количестве и хорошей сохранности эпителиальных клеток слизистой оболочки с места поражения и правильного «х классифицирования на «злокачественные» и «доброкачественные». В большинстве случаев диагноз рака желудка может быть уверенно поставлен на основании выработанных практикой цитологических критериев злокачественности. В ряде же случаев либо возможен ложноотрицательный ответ либо высказано подозрение на рак. Основываясь на личном опыте, можно сделать вывод, что причины, в результате -которых ставится неправильный (ложноотрицательный) диагноз, разнообразны и нередко сочетаются. В частности, это технические трудности для прицельного получения материала с целью его цитологического изучения (опухоли пилорического, кардиального, субкардиального отделов желудка). Гистологическое строение опухоли и стадия болезни не оказались при прицельном получении материала факторами, определяющими успех цитологической диагностики рака.
Можно ли улучшить результаты диагностики, свести к минимуму количества ложноотрицательных ответов. Да, можно. С этой целью показано динамическое цитологическое исследование в процессе лечения или в диагностически неясных случаях и получение материала из различных участков поражения слизистой оболочки. Так, по нашим наблюдениям, из 57 больных раком желудка, у которых производилось многократное биопсирование, у 48 раковые клетки были обнаружены только в отдельных препаратах и лишь у 7 больных выявлены во всех препаратах. Следовательно, в большинстве случаев точный цитологический диагноз был определен множественным биопсированием измененных участков слизистой оболочки желудка. Разумеется, при прицельном получении материала со слизистой желудка важное значение имеют квалификация гастроскописта и опыт лаборанта, готовящего цитологические препараты из биоптатов.
Большой практический и теоретический интерес представляют больные, у которых при цитологическом исследовании материала, полученного из желудка, можно высказать лишь подозрение на рак. При анализе собственных наблюдений мы пришли к выводу, что в этих случаях на первый план выступают другие причины по сравнению с группой больных с отрицательным результатом цитологического исследования. Не имеют существенного значения локализация злокачественного процесса и его размеры, стадия болезни, макроскопическое строение карциномы. Оказалось, что неуверенные заключения связаны со следующими причинами: недостаточное для оценки количество материала, плохое его качество — много разрушенных клеток, в небольшом числе случаев были недооценены изменения клеток и почти в 1/3 возникали значительные трудности при определении характера изменений клеток. Таким образом, сложности в определении характера изменений клеток не только связаны с чисто техническими причинами, но и зависят от затруднений при классификации клеток на доброкачественные и злокачественные. Изучение цитологических препаратов, приготовленных из соскобов с края опухоли при несмешанных формах наиболее часто встречающегося рака желудка, помогло понять последнее обстоятельство.
При аденокарциноме цитологическая картина выглядит пестрой, полиморфной. Клетки располагаются в пластах с плохо различимыми межклеточными границами, в виде комплексов лежат раздельно. Клетки и ядра в большинстве случаев увеличены в размерах, у клеток с хорошо сохранившейся цитоплазмой можно отметить неправильную, причудливую форму, напоминающую иногда цилиндрический эпителий. В некоторых случаях из-за выраженной вакуолизации цитоплазмы клетки приобрели форму перстневидных. Редко встречаются двухъядерные или фагоцитирующие клетки. Ядра чаще всего округло-овальной формы с неровными контурами, нередко без цитоплазмы («голые»). Хроматин мелкоточечный, сетчатый, глыбчатый. В некоторых ядрах определяются крупные и мелкие ядрышки (1—3, редко больше), вакуоли, очень редко митозы, явления кариорексиса. В ряде случаев встречаются клетки, которые, несмотря на признаки атипии, нельзя с полной уверенностью отнести к раковым.
При солидном раке увеличенные в размерах клетки располагаются в виде скоплений, комплексов, лежат раздельно, могут быть представлены «голыми» ядрами. Межклеточные границы обычно не определяются, лежащие отдельно клетки напоминают иногда цилиндрический эпителий. Отчетливо определяются анизоцитоз и анизокариоз. Ядра, чаще всего увеличенные в размерах, имеют преимущественно округло-овальную форму, содержат мелкоточечный, сетчатый или глыбчатый хроматин. В ядрах определяются разной величины ядрышки (1—4).
В случаях слизистого рака явления клеточной и ядерной атипии выражены несколько меньше, чем в предыдущих двух случаях. В препаратах довольно редко встречаются крупные клетки с большими ядрами, занимающие почти всю цитоплазму, либо «перстневидные» клетки. В то же время можно видеть пласты малоизмененных клеток.
При недифферецированном раке цитологическая картина отличается значительной пестротой. Клетки разнообразной величины и формы, в большинстве своем увеличенные в размерах, располагаются в пластах, комплексах, лежат раздельно. Отмечаются вакуолизация цитоплазмы, явления фагоцитоза. Хорошо видны ядерный полиморфизм, ядрышки, увеличенные в числе и размерах. При всех перечисленных гистологических формах рака встречаются клетки, которые можно отнести лишь к подозрительным.
Значительный полиморфизм цитологической картины в пределах одной гистологической формы рака, когда в препарате встречаются морфологически неизмененные клетки, клетки с нерезко выраженными признаками атипии и полностью недифференцированные, трудно объяснить одной причиной. Ответ следует, по-видимому, искать в стадийности развития клеток при канцерогенезе, отсутствии стабильности структуры рака, различном функциональном состоянии клеток в разных участках опухоли. На вопрос, существуют ли пути для преодоления этих диагностических трудностей, можно ответить положительно. В частности, в настоящее время с помощью математических методов можно почти в 100% случаев разграничить доброкачественные и злокачественные процессы по цитологическим данным. Большое будущее, очевидно, принадлежит использованию в диагностических целях количественного определения содержания ДНК в ядрах эпителиальных клеток слизистой оболочки желудка.
Все сказанное позволяет сделать практический вывод, что получение в достаточном количестве и хорошего качества материала из места поражения, а также применение в ряде случаев специальных методов исследования дает возможность повысить число правильных ответов почти до 95—98%, тогда как в настоящее время оно составляет около 80—85%.
Особое значение цитологическое исследование приобретает в диагностике начальных форм рака желудка. Цитодиагностика ранних стадий рака основана на том хорошо известном факте, что при развитии злокачественной опухоли в первую очередь появляются изменения клеток, а затем уже и структуры ткани. При цитологической диагностике начального рака желудка мы опирались на общепринятые критерии злокачественности клетки. Достигнутые при этом результаты свидетельствуют о том, что в случаях «раннего» рака, в том числе рака in situ, имеются уже вполне морфологически сформировавшиеся раковые клетки, и общепринятые признаки злокачественности клеток являются вполне надежными для их распознавания. Необходимо помнить, что обязательный учет клинических данных и комплексное лабораторно-инструментальное обследование больного значительно повышают качество диагностики. Приводим следующее наблюдение.
Больной А., 63 лет, поступил в клинику с жалобами на периодические боли в подложечной области, возникающие без видимой причины, отрыжку воздухом. Впервые язва желудка в области привратника была обнаружена 27 лет назад, когда больной обратился к врачу по поводу болей в животе. После проведенного лечения хорошее самочувствие сохранялось до прошлого года, когда вновь появились боли в подложечной области. К врачам не обращался. Периоды улучшения сменялись ухудшениями самочувствия. При рентгенологическом обследовании в феврале этого года обнаружена язва пилорического канала.
При поступлении состояние удовлетворительное. Питание понижено. Пальпация живота безболезненна, печень и селезенка не прощупываются. Анализ крови без изменений. При рентгеноскопии желудка обнаружена язва пилорического канала размерам 0,3х0,3 см. При гастроскопии в теле желудка несколько утолщенные складки, слизистая оболочка отечная, гиперемированная. Антральный отдел широкий, в препилорическом отделе по передней стенке выявляется язва продольной формы размером 1,2х0,4 см. Дно ее покрыто желтым геморрагическим налетам. Края неровные, бугристые, уплощенные Отверстие пилорического канала деформировано. Слизистая оболочка в этом участке резко отечная. Заключение: хроническая язва препилорического отдела желудка в стадии обострения.
Цитологическое исследование: обнаружены преимущественно крупные «голые» гипохромные ядра неправильной формы с большими причудливыми ядрышками. Хроматин сетчатый. Заключение: рак.
Гистологическое исследование: очаговый атрофический гастрит и поверхностный гастрит в пилорическом отделе. Признаков злокачественного роста в изученном материале не найдено. Однако, несмотря на данные цитологического исследования, с учетом отрицательных результатов других исследований, достаточной убежденности в правильности диагноза у врачей не было. После курса консервативного лечения больной был обследован повторно.
Рентгеноскопия желудка: натощак содержит жидкость, количество которой значительно увеличивается к концу исследования. Отмечается резко выраженная деформация препнлорического и пилорического отделов желудка,, которые подтянуты кверху и фиксированы. Пиларический канал сужен с ригидными контурами. В области сужения видна плоская язвенная «ниша» диаметром 0,8 см. Отмечается нарушение эвакуации из желудка. Через 24 ч около половины принятой бариевой взвеси определяется в желудке. Заключение: язва привратника с резко выраженной деформацией и сужением его; нарушение эвакуации содержимого желудка. Исключить опухолевое поражение или малигнизацию желудка в пилорическом канале не представляется возможным.
При гастроскопии в пилорическом отделе виден участок отечной, эрозивной и бугристой слизистой оболочки, ригидной при биопсии. Перистальтика в этом отделе не прослеживается, привратник резко отечный, деформированный, суженный. Заключение: картина карциномы препилорического отдела желудка. Цитологическое исследование: картина рака желудка. Гастрсбиопсия — слизистый рак желудка.
Больной переведен в хирургическую клинику, где произведена резекция желудка. При гистологическом исследовании резецированного желудка обнаружен слизистый рак в крае язвы, распространяющийся до мышечного слоя желудка.
Диагностика рака желудка тесно связана с вопросами послеоперационного прогноза. До последнего времени в этом отношении ясность была только ,в случаях далеко зашедшего развития рака. Что же касалось других стадий рака, то спорных пунктов для прогноза не существовало. Однако работы последних лет позволяют надеяться, что с помощью современных методов диагностики можно прогнозировать исход лечения и до оперативного вмешательства. Так, сравнивая содержание ДНК в опухолевых клетках в зависимости от глубины распространения опухоли в стенке желудка, можно предположить, что изучение содержания ДНК в цитологических препаратах отражает в некоторой степени глубину прорастания опухолью стенки желудка. Это особенно важно при определении стадии развития опухоли.
Исследование на онкомаркеры на рак желудка
Диагностировать рак желудка без применения сложных и не всегда легко переносимых исследований, к сожалению, пока невозможно. Хотя распространённой практикой «диспансеризации» уже стало исследование онкомаркеров. К сожалению, этот метод трудно отнести к высокочувствительным (чувствительность этих тестов не превышает 50%). И все же повышение значений СА 72-4, РЭА, СА 19-9 служит сигналом к обязательному углубленному обследованию и исследованию увеличенного показателя в динамике.
Большее значение онкомаркеры имеют при оценке распространенности процесса и при возникновении рецидива заболевания после успешного лечения.
Симптомы
Для ранних стадий рака желудка характерно обилие паранеопластических симптомов, часто маскирующих развитие опухоли и уводящих в сторону от правильного диагноза.
- Один из самых ярких симптомов — черный акантоз, при котором развивается сопровождающаяся ворсинчато-бородавчатыми разрастаниями темная пигментация кожи подмышечных впадин и других крупных кожных складок. Иногда черный акантоз на несколько лет опережает проявления самой опухоли.
- Полимиозит, дерматомиозит, кольцевидная эритема, пемфигоид, не уступающий лечению тяжелый себорейный кератоз также требуют углубленного обследования с обязательным проведением эндоскопии желудка.
- Бывают случаи, когда выработка клетками опухоли глюкокортикоидных гормонов, которые в норме синтезируются надпочечниками, вызывает даже формирование т.н. эктопического синдрома Кушинга. При нем жировая ткань откладывается преимущественно на лице и животе (так называемый матронизм), повышается артериальное давление, развивается склонность к переломам костей и акне.
- Частым паранеопластическим проявлением рака желудка, впрочем, как и многих других опухолей является мигрирующий тромбофлебит (синдром Труссо).
- Тяжелее всего заподозрить развитие рака желудка, когда у пожилых людей вдруг начинает быстро прогрессировать деменция, или появляются нарушение координации движений, изменение походки, нарушение равновесия.

Ситуация усугубляется сходством клинической, рентгенологической и эндоскопической картины при изъязвленных опухолях и язвенной болезни. Поэтому самым чувствительным способом диагностики считается эзофагогастродуоденоскопия (ЭГДС, гастроскопия) с множественной биопсией, обязательной у пациентов, относящихся к группе риска. ЭГДС позволяет одновременно:
- выполнить биопсию и провести дальнейшее гистологическое и цитологическое исследование с целью морфологической верификации новообразования и диагностики;
- осуществить лечебные манипуляции по коагуляции полипа с его удалением при небольших размерах (до 2 см);
- остановить кровотечение;
- провести зонд для кормления и т.д.
При угрозе кровотечения используется менее травмирующая браш-биопсия. В сомнительных случаях назначают повторную биопсию через 8-12 недель. Но даже этот способ диагностики дает правильный ответ только в 90% случаев и может дать ложно отрицательный результат при инфильтративном росте опухоли (такой рак называют скирр).
Кроме рака в желудке могут развиваться и опухоли из других клеток, требующие совершенно иных подходов к лечению (саркома, лимфома). Единственный способ разобраться в этом — множественные биопсии при проведении ЭГДС. Для выявления измененных участков тканей, не обнаруживаемых при обычном осмотре, используют т.н. хромогастроскопию. Этот метод позволяет проводить диагностику опухолей на ранних стадиях благодаря тому, что при окрашивании слизистой оболочки желудка по время процедуры специальными красителями (конго-рот/метиленовым синим, индигокамином) и даже раствором Люголя опухолевые ткани выглядят иначе, чем здоровые.
Когда необходимо проведение ЭГДС (гастроскопии)?
Существуют заболевания, считающиеся предраковыми, при которых необходимо периодическое обследование независимо от наличия симптомов. К ним относят:
- хронический атрофический гастрит с т.н. кишечной метаплазией особенно при наличии хеликобактерной инфекции;
- язвенная болезнь желудка;
- пищевод Баррета;
- дефицит витамина В12 (пернициозная анемия);
- аденоматозные полипы желудка;
- гипертрофическая гастропатия.
Операции на желудке в связи с доброкачественными новообразованиями, перенесенные более 10-лет назад, и отягощенная наследственность также относятся к ситуациям, требующим пристального наблюдения.
Вы должны регулярно наблюдаться с обязательным регулярным проведением ЭГДС, если у ваших родственников диагностировались:
- рак органов желудочно-кишечного тракта,
- семейный аденоматозный полипоз толстой кишки,
- синдром Гарднера,
- синдром Пейтца-Егерса,
- семейный ювенильный полипоз,
- синдром Ли Фраумени.
С развитием генетики стали известны некоторые гены, определенные мутации которых при особых условиях приводят к раку желудка.
Существуют и регионы, в которых, видимо в результате особенностей питания или экологии, заболеваемость существенно выше средних показателей (Япония, некоторые страны Европы, Скандинавия, Южная и Центральная Америка, Китай, Корея, страны бывшего СССР). Людям, длительно живущим в этих районах, надо внимательнее относиться к своему здоровью и периодически проводить ЭГДС. Сигналом к обязательному обследованию может послужить такой показатель как концентрация пепсиногена сыворотки крови (в норме — меньше 70 нг/мл) и соотношение его фракций (ПГ1/ПГ2).
При невозможности проведения ЭГДС, например, из-за сопутствующих заболеваний, может быть проведена полипозиционная рентгенография с двойным контрастированием бариевой взвесью и воздухом. Этот метод обладает, правда, гораздо меньшей чувствительностью при ранних стадиях заболевания и не дает возможности морфологической верификации. Дополнительно используют МСКТ и УЗИ, однако точность последнего исследования даже при опытном исследователе очень зависит от технических возможностей аппарата, особенностей телосложения и правильности подготовки пациента.
Лапароскопическая диагностика желудка
При подозрении на распространение опухоли по брюшной полости возможно проведение диагностической лапароскопии и лапароскопического УЗИ, позволяющих подробно изучить процесс в непосредственной близости.
Этот метод позволяет осмотреть поверхности печени, передней стенки желудка, париетальной (выстилающей стенки брюшной полости) и висцеральной (покрывающей органы) брюшины с проведением при необходимости биопсии. В некоторых случаях эти данные принципиально важны для выбора лечения.

Прогноз при раке желудка
Прогноз зависит от количества пораженных лимфатических узлов и уровня поражения лимфатических коллекторов, глубины прорастания опухоли в стенку желудка, стадии процесса, типа роста и типа самой опухоли. По данным МНИОИ им. П.А.Герцена 5-летняя выживаемость при диагностике рака желудка на ранней стадии и быстро начатом лечении достигает 85-90%. В случае более позднего выявления ещё резектабельной опухоли — 11-54%, и даже в случае выявления рака на IV стадии лечение позволяет обеспечить 7% выживаемость больных в течение 5 лет.
Цены в Европейской клинике на диагностику рака желудка
- Гастроскопия — 19 400 руб.
- Рентгеноконтрастное исследование пищевода и желудка — 16 700 руб.
- Ультразвуковое исследование брюшной полости — 5 100 руб.
- Диагностическая лапароскопия — 43 900 руб.
Но речь ведь не только о продлении жизни. Цель лечения в большинстве даже далеко зашедших случаев в улучшении её качества, избавлении человека от множества тягостных симптомов, в том числе болей, обеспечении ему возможности вести обычный образ жизни, заниматься важными для него делами, общаться с близкими.
Современные методы лечения рака желудка, применяемые в Европейской клинике, позволяют проводить лечение с минимальными сроками госпитализации и использованием малоинвазивных методик, улучшающих не только прогноз для жизни, но и качество самой жизни наших пациентов.
Запись
на консультацию
круглосуточно


