Что такое холестероз желчного пузыря у детей
Л.А. ХАРИТОНОВА, профессор кафедры педиатрии и инфекционных болезней факультета усовершенствования врачей, доктор медицинских наук
Т.М. ЮДИНА, ассистент кафедры педиатрии и инфекционных болезней факультета усовершенствования врачей
Российский государственный медицинский университет, Москва
Холестероз желчного пузыря (ХЖП) — заболевание, характеризующееся нарушением обмена холестерина с преимущественным его отложением в стенке желчного пузыря, впервые описано более полутора века назад. К сожалению, эта патология еще недостаточно изучена. В литературе встречаются лишь единичные публикации, посвященные ХЖП у детей.
Этиология пока не установлена
Холестероз выявляют начиная с детского возраста до глубокой старости. Большинcтво авторов считают, что пик заболеваемости приходится на 30—39 лет. Частота обнаружения ХЖП, по результатам холецистэктомий, варьирует в широком диапазоне — от 2 до 40%. Одни авторы отмечают более высокую частоту встречаемости ХЖП у женщин (19:1), чем у мужчин, другие, напротив, считают, что заболевание у лиц мужского пола встречается в 2,5—3,0 раза чаще.
Проведенные нами исследования в области изучения желчнокаменной болезни показали, что практически у трети детей холелитиаз сочетается с ХЖП. Однако до проведения холецистэктомии ХЖП диагностируется только у 10% детей. Подобный факт заслуживает внимания, поскольку и холелитиаз, и холестероз, начинаясь в детстве, могут проявляться в последующие годы по мере накопления причинно-значимых факторов, обусловливающих их манифестацию.
Этиология и патогенез ХЖП до настоящего времени не установлены. Существуют две точки зрения о чрезмерном накоплении липидов в стенке желчного пузыря. Согласно одной, предложенной R. Virchov, и поддержанной L. Aschoff, а также большинством исследователей, избыточное накопление липидов происходит вследcтвие поступления их из желчи. Напротив, В.Naunyn (1921 г.) и его последователи трактовали ХЖП как результат депонирования липидов в стенке пузыря за счет активного их транспорта из кровяного русла. В эксперименте установлено, что источником избыточного количества липидов в клетке стенки ЖП являются модифицированные липопротеиды низкой плотности (мЛНП). Их изменение обусловливается ацетилированием, окислением, гидролизированием и и др. Процесс модификации ЛНП осущес-твляется под влиянием эндотелиальных и гладкомышечных клеток, макрофагов в стенке желчного пузыря, желчи, крови.
«Скеведжер-рецепторы», а по-русски… мусорщики
В результате мЛНП начинают взаимодействовать с такими рецепторами макрофага, как «скеведжер-рецепторы» (удаляющие мусор). Последние перестают регулировать чрезмерное накопление липидов в клетке и элиминировать их. Макрофаги переполняются липидами, теряют свою подвижность, трансформируются в «пенистые клетки», которые скапливаются по ходу лимфатических сосудов. «Пенистые клетки» находятся в слизистой оболочке желчного пузыря, а при прогрессировании патологического процесса проникают в подслизистый и мышечный слои. Формируется диффузно-сетчатая форма ХЖП, а в случае избирательного накопления «пенистых клеток» — полипозная форма заболевания.
Не исключается, что макрофаги подслизистого слоя стенки желчного пузыря могут иметь иные дефекты, обусловливающие, с одной стороны, усиленное поступление липидов из перенасыщенной холестерином желчи, с другой — нарушение элиминации их из клетки. Так, при изменении обменных процессов в желчном пузыре имеет место диспротеинемия, характеризующаяся уменьшением количества альбуминов и увеличением всех глобулиновых фракций. Эти изменения обусловливаются, с одной стороны, функциональными нарушениями печени, а с другой — морфологическими изменениями слизистой оболочки желчных путей.
Это часто — диагностическая находка
У детей с ХЖП нами было установлено повышение общего белка сыворотки крови. Повышение уровня общего белка наблюдалось преимущественно за счет бета-глобулиновой фракции. На этом фоне отмечалось незначительное снижение фракции альфа-глобулинов.
Известно, что к бета-глобулинам относятся важнейшие белковые переносчики липидов и белковые переносчики полисахаридов. Важное значение липопротеинов состоит в том, что они удерживают в растворе нерастворимые в воде жиры и липоиды и обеспечивают тем самым их перенос кровью. Около 75% всех жиров и липоидов плазмы входят в состав липопротеинов. Небольшие количества липопротеинов обнаруживаются и в альфа-1 — фракции глобулинов, однако большинство их принадлежит к бета-глобулинам, самый главный из них — бета-1-липопротеин, молекула которого на 77% состоит из липидов.
Вполне вероятно, что у детей с ХЖП повышение компонентов, удерживающих в плазме крови нерастворимые жиры и липоиды, является своеобразной компенсаторной реакцией, позволяющей предотвратить гиперхолестеринемию, а в последующем и гиперхолестеринхолию и тем самым «отдаляет» формирование пенистых клеток — основного морфологического маркера ХЖП.
Дискуссионным остается также вопрос о самостоятельности клинической картины ХЖП. Одни авторы считают, что ХЖП, не имея собственных симптомов, проявляется лишь при развитии холецистита, желчнокаменной болезни, дискинезиях желчевыводящих путей. Другие относят к симптомам собственно ХЖП коликообразные боли в правом подреберье и эпигастрии, беспокоящие больных в течение длительного времени.
ХЖП в детском возрасте чаще является диагностической находкой. Клиническая картина не имеет специфических признаков: в большинстве случаев (60,5%) заболевание протекает бессимптомно и обнаруживается лишь при выполнении ультразвукового исследования желчного пузыря. Диспепсические явления в виде тошноты, метеоризма, жидкого стула наблюдаются лишь у четверти больных детей (25,6%). Крайне редко определяются тянущие, ноющие боли в эпигастрии и правом подреберье (11,6%); острые боли (2,4%).
Диагностика очень сложна
Диагностика ХЖП как у взрослых, так и у детей, представляет особые трудности. Установлены однонаправленные изменения показателей липидограммы сыворотки крови как при ХЖП, так и при желчнокаменной болезни. Тем не менее патогномоничными признаками для ХЖП у детей являются: диспротеинемия (снижение альфа- и повышение бета-глобулинов), изменения липидного комплекса в виде повышения триглицеридов, липопротеидов низкой (ЛПНП), очень низкой плотности (ЛПОНП) и снижения липопротеидов высокой плотности (ЛПВП) в биохимических исследованиях сыворотки крови. Однако центральное место в диагностике ХЖП у детей занимают инструментальные методы исследования.
В последние годы получил широкое распространение метод эндоскопического ультразвукового исследования (УЗИ), который стал альтернативным неинвазивным методом диагностики заболеваний панкреатобилиарной зоны и вошел в золотой стандарт предоперационного обследования. Метод позволяет с высокой точностью обнаружить патологические изменения в органах гепатобилиарной зоны.
Мнения педиатров склонялись к операции
Долгие годы единственным методом лечения при ХЖП у детей считалась холецистэктомия. Объяснением этому служили трудности интерпретации выявленных патологических изменений стенки желчного пузыря, в связи с чем мнение педиатра склонялось в сторону оперативного вмешательства.
В настоящее время успехи в изучении этиологии и патогенеза ХЖП позволяют пересмотреть необходимость обязательного оперативного вмешательства при обнаружении признаков ХЖП. Особенно это касается тех случаев, когда заболевание диагностируется в детском возрасте. Известно, что удаление желчного пузыря у ребенка не только приводит к выключению его буферной функции, но и лишает больного гормонопродуцирующей способности желчного пузыря. Последнее определяет качество продуцируемой печенью желчи. Все это приводит к необходимости пожизненного приема урсодеоксихолевой кислоты (УДХК) после холецистэктомии.
В литературе имеются многочисленные данные об успешном применении препаратов желчных кислот для лечения холестероза у взрослых. Обоснованием для их применения при ХЖП послужили известные механизмы их действия. Прием УДХК восстанавливает нарушенный метаболизм холестерина, снижая содержание ЛПНП и повышая ЛПВП, а также снижает индекс насыщения желчи холестерином. Применение препаратов УДХК при ХЖП у взрослых приводит к улучшению клинической симптоматики, регрессу патологических изменений в стенке желчного пузыря и нормализации липидного обмена.
Предпочтительнее фитотерапия
Следует отметить, что в настоящее время монотерапия УДХК не применяется, т.к. при длительном лечении увеличивается риск развития побочных эффектов, главным из которых является гепатотоксический эффект. В этом плане заслуживают внимания препараты растительного происхождения. Назначаются гепатопротекторы комбинированного действия, повышающие устойчивость печени к патологическим воздействиям, усиливающие ее детоксикационную функцию путем активации ферментных систем, включая цитохром Р450, и других микросомальных энзимов.
Препаратами выбора у детей являются флавониды из расторопши пятнистой, где основным действующим веществом является силибинин. Последний взаимодействует со свободными радикалами, переводя их в менее токсичные соединения, прерывает процесс перекисного окисления липидов, предотвращает разрушение клеточных структур, а также стабилизирует клеточные мембраны, ускоряет регенерацию гепатоцитов, замедляет проникновение в клетку некоторых токсичных веществ. Примером таких ЛС может быть Гепабене, назначаемый во время еды, три раза в день.
Следующей группой ЛС, необходимой при лечении ХЖП, является назначение гиполипидемических препаратов. К основным средствам, оказывающим гиполипидемическое действие, относят: вещества, связывающие желчные кислоты (секвестранты желчных кислот — холестерамин и др.); никотиновую кислоту и ее производные; статины; фибраты, производные фиброевой кислоты; другие гиполипидемические лекарственные средства; препараты растительного происхождения.
Основное действие препаратов никотиновой кислоты заключается в угнетении секреции ЛПОНП и снижении образования ЛПНП с одновременным повышением ЛПВП (ксантинола никотинат, никотиновая кислота). Препараты эффективны при гиперхолестерин- и гипертриглицеридемии.
Фибраты (производные фиброевой кислоты) уменьшают транспорт холестерина и триглицеридов липопротеинами, усиливают распад холестерина. Группа статинов ингибирует выработку ГМГ-КоА-редуктазы, катализирующей начальные и промежуточные стадии синтеза холестерина, тем самым обеспечивается их гиполипидемическое действие. Однако применение всех этих групп препаратов ограничено у детей до 18 лет.
Листья артишока самые полезные
В детской практике наиболее целесообразным является применение гиполипидемических средств растительного происхождения, содержащих биофлавоноиды, биогенные амины, инулин, обладающих одновременно липотропным, антисептическим и гепатопротективным действиями. Наиболее эффективным среди них являются лекарственные средства из листьев артишока, обладающие желчегонным и гепатопротективным действиями.
Препараты увеличивает выработку коферментов гепатоцитами и оказывают влияние на метаболизм липидов, холестерина и кетоновых тел, стимулируют биосинтез белков и фосфолипидов. Преимуществом перед аналогами является возможность применения их у детей раннего возраста за счет наличия детской официнальной формы в каплях. Хорошо переносятся и могут назначаться детям с первого года жизни.
В случаях, когда ХЖП протекает на фоне дисфункций желчного пузыря и сфинктера Одди, в терапию подключают холеспазмолитики (при гипертонусе), при гипотонии — холекинетики.
В настоящее время используют препараты нового поколения, в частности, мебеверин, с изолированным спазмолитическим действием на различные отделы желчевыводящих путей. Действие мебеверина напоминает биологические эффекты холецистокинина. Мебеверин, являясь блокатором быстрых натриевых каналов клеточной мембраны миоцита, купирует патологический спазм и препятствует развитию атонии гладкой мускулатуры. Отсутствие рефлекторной гипотонии позволяет применять препарат у детей с гипер- и гипомоторной дисфункциями желчного пузыря. Препарат безопасен, обладает пролонгированным действием и принимается два раза в сутки.
В статье представлен алгоритм ведения пациентов детского возраста с холестерозом желчного пузыря в зависимости от клинической симптоматики и данных объективных методов диагностики. Приведены результаты консервативной терапии у 15-летней больной с полипозно-сетчатой формой холестероза желчного пузыря.
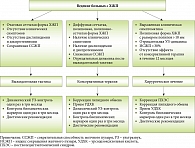
Рис. 1. Тактика ведения больных с холестерозом желчного пузыря
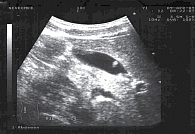
Рис. 2. Данные трансабдоминального УЗ-сканирования брюшной полости больной А.

Рис. 3. Данные трансабдоминального УЗ-сканирования брюшной полости больной А. через шесть месяцев после консервативной терапии
Введение
Холестероз желчного пузыря (ХЖП) – обменное заболевание, характеризующееся диффузным или очаговым накоплением в стенке желчного пузыря холестерина. Впервые ХЖП был описан полтора века назад.
В литературе встречается несколько синонимичных названий ХЖП, характеризующих внешний вид внутренней оболочки желчного пузыря при данной патологии: малиновый, земляничный, рыбьечешуйчатый, крапчатый и др. Термин «холестероз», предложенный в 1925 г. N. Mendez-Sanches, в настоящее время чаще других используется в научной литературе [1, 2].
Длительное время ХЖП считали редким и трудно диагностируемым заболеванием у взрослых, казуистикой – у детей. В доступной литературе до недавнего времени встречались лишь единичные описания ХЖП в детском возрасте. Все они являлись секционной находкой при исследовании ткани желчных пузырей, удаленных по поводу желчнокаменной болезни [3]. В последние годы, вследствие широкого внедрения в практику высокоинформативных методов исследования, в частности ультрасонографии, а также активного изучения нарушений липидного обмена, ХЖП стали выявлять значительно чаще [2, 4]. В педиатрической практике остается нерешенным ряд вопросов, касающихся не только причин развития данного заболевания, но и современных возможностей его лечения [5, 6].
Методы лечения
До настоящего времени единственным методом лечения детей с ХЖП считалась холецистэктомия [3]. Как правило, педиатры склонялись к оперативному вмешательству, поскольку возникали сложности в интерпретации выявленных патологических изменений стенки желчного пузыря [5, 6]. Появление ультразвуковых аппаратов с высокой разрешающей способностью позволило не только проводить дифференциальную диагностику с другими заболеваниями, но и выявлять ХЖП на ранних стадиях, прослеживать динамику его течения у детей [6]. Это потребовало разработки новых подходов к тактике ведения и оптимальных методов лечения таких больных.
Алгоритм ведения детей с ХЖП, разработанный нами на основании результатов многолетних исследований, приведен на рис. 1.
Выжидательная тактика предполагает несколько основных этапов:
динамическое ультразвуковое наблюдение с оценкой патологических изменений в стенке желчного пузыря и определение его сократительной способности;
контроль биохимических показателей белкового (альфа- и бета-глобулинов) и липидного спектра с определением уровней общего холестерина (ОХС), липопротеинов низкой (ЛПНП), очень низкой (ЛПОНП) и высокой (ЛПВП) плотности, триглицеридов (ТГ);
диетические рекомендации.
При наличии отрицательной клинической и ультразвуковой динамики (появление выраженных болей, увеличение количества и размеров полипов (более 10 мм)), а также в отсутствие положительного эффекта от консервативной терапии в течение 12 месяцев необходимо решать вопрос о проведении холецистэктомии.
Поскольку, по мнению многих авторов, ХЖП – проявление липидного дистресс-синдрома, наиболее оправданной тактикой его лечения на современном этапе считается консервативная терапия [7].
В литературе имеются многочисленные данные об успешном применении препаратов желчных кислот для лечения ХЖП у взрослых [1, 2, 4]. Обоснованием для их применения послужили сведения о том, что урсодезоксихолевая кислота (УДХК) восстанавливает нарушенный метаболизм ХС, снижает содержание ЛПНП и повышает уровень ЛПВП. Применение препаратов УДХК при ХЖП у взрослых приводит к улучшению клинической картины, регрессу патологических изменений в стенке желчного пузыря и нормализации липидного обмена.
Данных об эффективности консервативного лечения ХЖП у детей в литературе нет. Результаты нашего исследования, проведенного на кафедре педиатрии с инфекционными болезнями у детей РНИМУ им. Н.И. Пирогова в течение 2008–2014 гг., также свидетельствуют об эффективности терапии препаратами УДХК в отношении клинических проявлений, нормализации ультразвуковых и биохимических маркеров ХЖП.
Клинический случай
Родители 15-летней больной А. обратились к гастроэнтерологу по месту жительства с жалобами на появление у девочки чувства тяжести в правом подреберье после еды. Из анамнеза известно, что в течение нескольких месяцев ее беспокоили тяжесть в правом подреберье после приема пищи, тошнота, иногда рвота. Болей в животе, нарушений стула не отмечалось. При ультразвуковом исследовании брюшной полости выявлены гиперэхогенные образования, которые были приняты за конкременты желчного пузыря. С диагнозом желчнокаменной болезни (?) пациентку направили на консультацию на кафедру педиатрии с инфекционными болезнями у детей РНИМУ им. Н.И. Пирогова.
Анамнез жизни. Девочка от второй беременности (первая – «замершая» беременность на сроке восемь недель), протекавшей на фоне угрозы прерывания, повышения уровня тестостерона до 5,2 нмоль/л (норма до 2,7 нмоль/л), ОХС до 7,5 ммоль/л (норма до 4,6 ммоль/л). С седьмую по 32-ю неделю беременности мать принимала метилпреднизолон 8 мг/сут.
Роды срочные, самостоятельные. Масса тела при рождении – 3850 г, длина 52 см, выписана из роддома на четвертые сутки. На грудном вскармливании находилась до двух месяцев. Росла и развивалась соответственно возрасту. Привита по возрасту. Перенесенные заболевания: острая респираторная вирусная инфекция, ветряная оспа, краснуха, скарлатина. Аллергический анамнез не отягощен.
Мать девочки, 53 года, страдает ожирением 2-й степени и сахарным диабетом 2-го типа. Отец, 55 лет, страдает ишемической болезнью сердца, атеросклерозом, облитерирующим эндартериитом, в возрасте 40 лет перенес острый инфаркт миокарда. Бабушка по линии матери 76 лет – сахарный диабет 2-го типа, гипертоническая болезнь. Дедушка по линии отца умер в возрасте 55 лет от обширного инфаркта миокарда.
Данные объективного исследования. Состояние удовлетворительное, рост 170 см, вес 72 кг. Физическое развитие высокое, дисгармоничное за счет избытка массы тела. Телосложение правильное. Кожные покровы смуглые, чистые. Лимфоузлы не увеличены. Видимые слизистые оболочки чистые, розовые. Подкожно-жировая клетчатка выражена избыточно, распределена равномерно, по женскому типу. Костно-мышечная система без видимой патологии. Дыхание везикулярное, проводится во все отделы легких, хрипов нет. Тоны сердца звучные, ритмичные, шумы отсутствуют. Язык влажный, слегка обложен беловатым налетом. Живот обычной формы, симметричен, не вздут, при пальпации безболезненный во всех отделах. Нижний край печени +1 см от края реберной дуги по правой средней ключичной линии, гладкий, эластичный, безболезненный. Селезенка не пальпируется. Мочеиспускание регулярное, безболезненное. Стул оформленный, ежедневный, без видимых примесей.
Общие анализы мочи и крови без отклонений от нормы.
Биохимическое исследование сыворотки крови:
общий белок – 76 г/л;
альбумины – 55%; глобулины – 45% (альфа-1 – 5,0%, альфа-2 – 9,2%, бета – 17,2%, гамма – 13,5%);
мочевина – 5,2 ммоль/л;
креатинин – 65 ммоль/л; глюкоза – 5,3 ммоль/л;
ОХС – 5,4 ммоль/л;
ЛПНП – 3,3 ммоль/л;
ЛПВП – 1,4 ммоль/л;
ЛПОНП – 0,7 ммоль/л;
коэффициент атерогенности (КА) – 2,9;
ТГ – 1,52 ммоль/л;
билирубин общий – 6,8 мкмоль/л;
щелочная фосфатаза (ЩФ) – 275 Ед/л (норма до 300 Ед/л);
аспартатаминотрансфераза (АСТ) – 26 Ед/л;
аланинаминотрансфераза (АЛТ) – 34 Ед/л;
лактатдегидрогеназа (ЛДГ) – 180 Ед/л (норма до 225 Ед/л);
альфа-амилаза – 144 Ед/л (норма до 220 Ед/л).
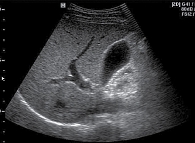
Трансабдоминальное ультразвуковое исследование брюшной полости. Размеры печени не увеличены, эхогенность печени слегка повышена, структура однородная. Желчный пузырь – 62 × 25 мм, стенки уплотнены, неравномерно утолщены, с множественными включениями, толщина передней стенки 2,2–3,5 мм на различных участках. На передней стенке желчного пузыря определяется неподвижное гиперэхогенное неоднородное по структуре образование без акустической тени и признаков васкуляризации размером до 4,0 мм. В просвете желчного пузыря рыхлый осадок. Сократительная способность – 28% (снижена) (рис. 2).
На основании жалоб, анамнеза, данных объективного осмотра, результатов лабораторных и инструментальных методов исследования был поставлен диагноз «холестероз желчного пузыря, полипозно-сетчатая форма, со снижением функции опорожнения».
Больной было назначено лечение:
диета № 5;
Урсосан по четыре капсулы в день (одна утром, три на ночь) в течение шести месяцев;
Фламин по одной таблетке три раза в день + Энтеросан по одной капсуле три раза в день + Гепатосан по одной капсуле три раза в день по схеме: один месяц прием – один месяц перерыв;
после этого Одестон по одной таблетке три раза в день + Фитомуцил по одному пакетику три раза в день в течение месяца.
Через шесть месяцев на фоне непрерывно проводимой терапии отмечалась положительная динамика: ощущения тяжести в правом подреберье после приема пищи исчезли, нормализовались показатели биохимического обмена, произошло нивелирование ультразвуковых признаков холестероза.
Результаты биохимического исследования сыворотки крови:
общий белок – 70 г/л;
альбумины – 62%; глобулины – 38% (альфа-1 – 5,2%, альфа-2 – 9,2%, бета – 11,1%, гамма – 12,5%);
мочевина – 5,2 ммоль/л;
креатинин – 65 ммоль/л; глюкоза – 4,9 ммоль/л;
ОХС – 4,7 ммоль/л;
ЛПНП – 2,6 ммоль/л;
ЛПВП – 1,6 ммоль/л;
ЛПОНП – 0,5 ммоль/л;
КА – 1,9;
ТГ – 1,08 ммоль/л;
билирубин общий – 6,7 мкмоль/л;
ЩФ – 200 Ед/л (норма до 300 Ед/л);
АСТ – 20 Ед/л;
АЛТ – 27 Ед/л;
ЛДГ – 169 Ед/л (норма до 225 Ед/л);
альфа-амилаза – 145 Ед/л (норма до 220 Ед/л).
Ультразвуковое исследование брюшной полости: размеры печени не увеличены, эхогенность печени нормальная, структура однородная. Желчный пузырь – 59 × 23 мм, стенки немного уплотнены, равномерные, толщина передней стенки 1,8 мм. Эхопозитивных образований в просвете желчного пузыря не выявлено. Сократительная способность – 47% (норма) (рис. 3).
При обследовании девочки через три, шесть и 12 месяцев после окончания терапии патологических изменений в стенке желчного пузыря не выявлено, показатели липидного обмена соответствовали возрастной норме.
Выводы
Оптимальным методом лечения ХЖП у детей является консервативная терапия с применением УДХК в стандартной дозе с соблюдением диетических рекомендаций.
Дети хорошо переносят лечение препаратами УДХК, в том числе в сочетаниях с другими лекарственными средствами.
С помощью консервативной терапии можно не только добиться нивелирования ультразвуковых признаков холестероза, но и нормализовать липидный обмен.
Оперативное лечение показано лишь в случае желчной колики.

