Транслюминальная хирургия желчного пузыря


Эндоскопическая транслюминальная хирургия через естественные отверстия: хирургия без шрамов – новая цель развития малоинвазивной хирургии (N.O.T.E.S. операции)

Пучков К.В., Пучков Д.К. ХИРУРГИЯ ЖЕЛЧНОКАМЕННОЙ БОЛЕЗНИ: лапароскопия, минилапароскопия, единый порт, трансанальный доступ, симультанные операции.-М.:ИД «МЕДПРАКТИКА-М», 2017, 312 с.
Всего несколько лет назад использование хирургического доступа через естественные отверстия было лишь заоблачной перспективой — отсутствие швов на коже брюшной стенки и устранение послеоперационной боли.
Впервые концепция хирургии через естественные физиологические отверстия организма была описана американским гастроэнтерологом Anthony Kalloo из университета имени John Hopkins в Балтиморе (США).
Методика, позволяющая избежать послеоперационных рубцов, вызвала значительный интерес по всему миру. Сотни исследовательских групп из разных стран пытаются в экспериментальных условиях изучить технические аспекты и безопасность транслюминальных операций выполняемых через желудок, ободочную кишку, мочевой пузырь и влагалище. Впервые результаты трансжелудочной аппендэктомии, выполненной в клинических условиях, были доложены гастроэнтерологами Nageshwar Reddy и Venkat Rao из Азиатского института гастроэнтерологии, Хайдарабад (Индия) в 2004.
Трансвагинальный доступ
Трансвагинальный доступ в настоящее время является наиболее часто используемым при транслюминальных операциях у человека. Это обусловлено тем, что доступ к брюшной полости через кольпотомию широко использовался гинекологами в течение длительного времени. Этот подход известен с первого века нашей эры и был описан греческим гинекологом Соранусом из Эфеса, который успешно выполнял трансвагинальную гистерэктомию.
Русский гинеколог Дмитрий Оскарович Отт описал использование заднего свода влагалища как удобного доступа для выполнения интраабдоминальных диагностических и лечебных процедур. Технику своего метода Отт подробно изложил в нескольких статьях, вышедших в России и за рубежом в 1901–1908 гг.
По мнению G. S. Litynski (1996) первым использовал лапароскопию в гинекологической практике хирург из Нью-Йорка Albert Decker, освоивший метод для других целей еще в 1928 г.
В России первым влагалищный доступ для эндоскопии малого таза с диагностической и лечебной целью применил Н.М.Дорофеев. В 1960 г. он выполнил рассечение спаек в области малого таза при кульдоскопии.
В общей хирургии трансвагинальный подход также не является новым. Особенно в лапароскопической хирургии, позволяющей выполнять большие операции при минимальных разрезах брюшной полости, часто возникает необходимость удалять фрагменты тканей через так называемые минилапаротомные разрезы, которые в некоторых случаях расширяются до нескольких сантиметров. Таким образом, с начала использования лапароскопических методик авторы из разных стран описали извлечение различных органов (ободочная кишка, селезенка, желчный пузырь) через разрез влагалища.
Безопасность и эффективность данного доступа для удаления фрагментов из брюшной полости доказана многолетним опытом, кроме того опасения в отношении возможного отрицательного влияния на сексуальную функцию, а именно диспареунии, были опровергнуты результатами ретроспективного анализа больших групп пациентов.
Автором первого сообщения о выполнении лапароскопической холецистэктомии при помощи лапароскопа, введенного через влагалище после гистерэктомии, был аргентинский гинеколог Daniel Alberto Tsin из клиники Mont Sinai (Нью-Йорк, США).
В данных условиях трансвагинальный путь кажется наиболее удобным подходом для продвижения хирургии через естественные отверстия из экспериментальной области в клиническую практику.
В течение нескольких месяцев с начала 2007 года множество исследовательских групп из разных стран опубликовали данные об успешно выполненных операциях трансвагинальной холецистэктомии с применением исключительно эндоскопической техники, или с использованием тонких «иголочных» эндоскопов, или с применением комбинированной методики, когда лапароскопические инструменты используются для диссекции тканей.
На новую технологию быстро обратили внимание и в России. Первая трансвагинальная холецистэктомия с лапароскопической ассистенцией была выполнена в апреле 2008 года. Уже через год, в 2009 году, на ХII съезде Российского общества эндоскопических хирургов (РОЭХ) наибольший опыт операций по технологии N.O.T.E.S. представил проф. К.В.Пучков. Автор сообщил о 52 лапароскопических холецистэктомиях с трансвагинальной ассистенцией и извлечением препарата.
Ряд авторов описали использование жестких эндоскопов и инструментов, вводимых через задний свод влагалища, одновременно с трансумбиликальными инструментами при выполнении комбинированных операций. Данный подход особенно привлекателен, так как не требует приобретения специальных устройств и сложного обучения манипуляциям с гибкими эндоскопами. Действительно, несмотря на существующие хирургические методики, опыт, накопленный на настоящий момент, демонстрирует, что трансвагинальный подход удаления желчного пузыря эффективен, безопасен и сопровождается хорошими ранними и отдаленными результатами. Следует снова обратиться к гинекологическому опыту – результатам Датского мультицентрового исследования, посвященного изучению частоты сексуальной дисфункции после тотальной гистерэктомии по сравнению с субтотальной операцией, при которой влагалище остается интактным. Авторы данного исследования спустя один год после операции не обнаружили статистически значимых различий между двумя группами и пришли к выводу, что не анатомические факторы могут в большей степени влиять на формирование сексуальной дисфункции.
Тщательный отбор пациентов по психологическим и физическим параметрам имеет важное значение для исключения женщин с сопутствующими сексуальными расстройствами и/или гинекологическими заболеваниями, особенно эндометриозом, который может привести к послеоперационным осложнениям.
Мои публикации по теме NOTES- хирургия:
- Научные труды ХII Всероссийского съезда эндоскопических хирургов // Эндоскопическая хирургия. – 2009. — №1. – С. 197 – 203.
- Материалы ХIII cъезда РОЭХ // Альманах Института хирургии им. А.В.Вишневского. – 2010. — Т5. — №1. — С. 53 – 62.
Задать вопросы или записаться на консультацию
 «Когда вы пишете письмо, знайте: оно попадает мне на мою личную электронную почту. На все ваши письма я отвечаю всегда только сам. Я помню, что вы доверяете мне самое ценное — свое здоровье, свою судьбу, свою семью, своих близких и делаю все возможное, чтобы оправдать ваше доверие.
«Когда вы пишете письмо, знайте: оно попадает мне на мою личную электронную почту. На все ваши письма я отвечаю всегда только сам. Я помню, что вы доверяете мне самое ценное — свое здоровье, свою судьбу, свою семью, своих близких и делаю все возможное, чтобы оправдать ваше доверие.
Каждый день я по нескольку часов отвечаю на ваши письма.
Направляя мне письмо с вопросом, вы можете быть уверены, что я внимательно изучу вашу ситуацию, при необходимости запрошу дополнительные медицинские документы.
Огромный клинический опыт и десятки тысяч успешных операций помогут мне разобраться в вашей проблеме даже на расстоянии. Многим пациентам требуется не хирургическая помощь, а правильно подобранное консервативное лечение, в то время как другие нуждаются в срочной операции. И в том, и в другом случае я намечаю тактику действий и при необходимости порекомендую прохождение дополнительных обследований или неотложную госпитализацию. Важно помнить, что некоторым больным для успешной операции требуется предварительное лечение сопутствующих заболеваний и правильная предоперационная подготовка.
В письме обязательно (!) укажите возраст, основные жалобы, место проживания, контактный телефон и адрес электронной почты для прямой связи.
Чтобы я мог детально ответить на все ваши вопросы, прошу высылать вместе с вашим запросом сканированные заключения УЗИ, КТ, МРТ и консультаций других специалистов. После изучения вашего случая, я направлю вам либо подробный ответ, либо письмо с дополнительными вопросами. В любом случае я постараюсь вам помочь и оправдать ваше доверие, которое является для меня наивысшей ценностью.
Искренне ваш,
хирург Константин Пучков»
Швейцарская клиника в Москве ¦ ХИРУРГИЯ ¦ Трансвагинальная холецистэктомия по N.O.T.E.S
Сначала во Франции, в 2007 году, а потом и в России, начали использовать новую уникальную методику по удалению желчного пузыря. При ее использовании не нужны проколы передней брюшной стенки, не остаются послеоперационные швы и рубцы. Методика называется трансвагинальной холецистэктомией по технологии N.O.T.E.S.
Доступ к больному органу при трансвагинальной холецистэктомии по технологии N.O.T.E.S. выполняется через разрез в заднем своде влагалища (длина разреза — 1 сантиметр), потом проводят холецистэктомию. Так же, как если бы выполнялась лапароскопическая операция. Потом желчный пузырь извлекают из брюшной полости тоже через разрез в заднем своде влагалища.
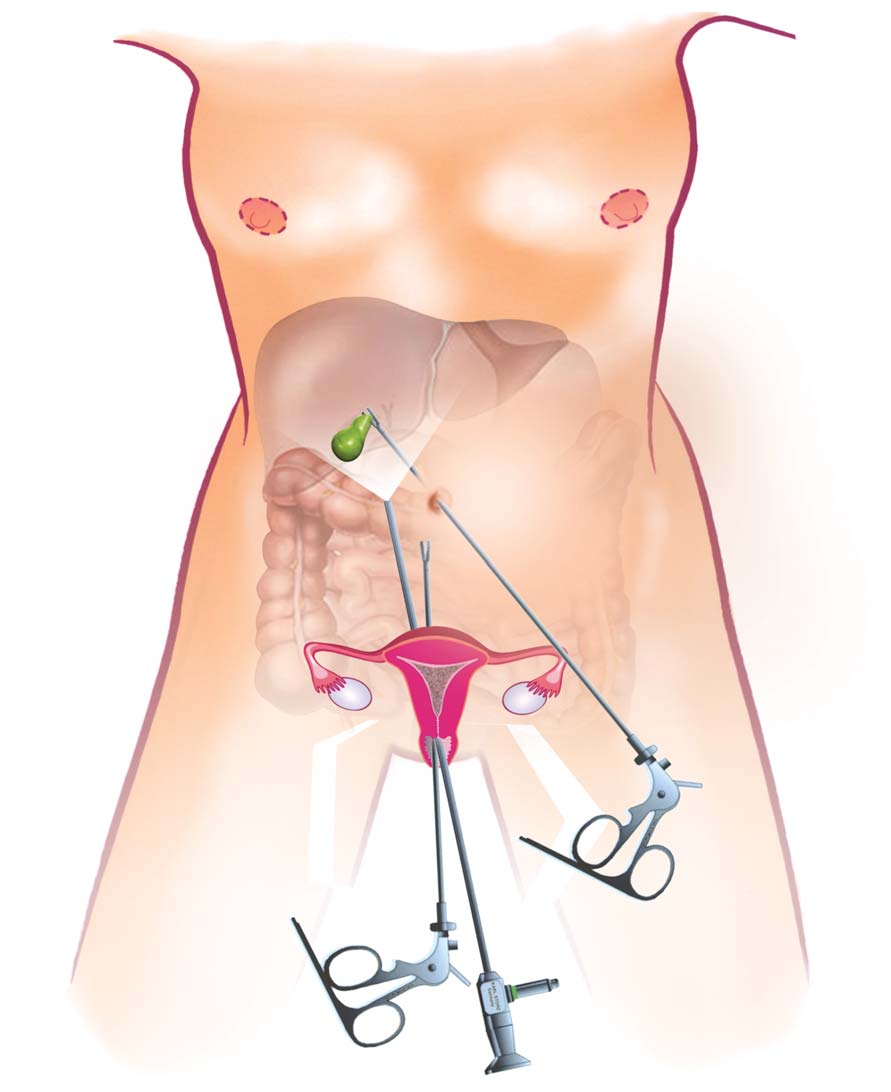
Новейшая технология лапароскопической холецистэктомии по технологии N.O.T.E.S. имеет преимущества, которые заключаются в:
- отсутствии боли после операции;
- максимальной двигательной активности;
- госпитализации всего лишь на один день;
- превосходном косметическом эффекте.
Единственное ограничение операции лапароскопической холецистэктомии при лечении ЖКБ по технологии N.O.T.E.S. (NOTES) заключается в половом покое на протяжении одного месяца после проведения операции. При трансвагинальной холецистэктомии не затрагиваются женские половые органы (матка, придатки и так далее), не оказывается влияния на их работу. Специалисты Швейцарской университетской клиники выполнили уже более ста трансвагинальных холецистэктомий, которые имеют отличный результат.
Видео о Транслюминальном удалении желчного пузыря. Операцию по удалению желчного пузыря через влагалище на программе » Жить здорово» проводит профессор Пучков К.В.
Уникальность однопортовой лапароскопической холецистэктомии, проводимой через один прокол, который выполняется в области около пупка, по технологии S.I.L.S. Пациентам, уже перенесшим операции на органах, расположенных в малом тазу, проведение лечения ЖКБ трансвагинальным доступом по технологии N.O.T.E.S. (NOTES) не подходит. В США, начиная с 2008 года, а потом и в России, стали использовать еще одну уникальную методику малоинвазивной холецистэктомии. Методика заключается в удалении желчного пузыря через один прокол в области около пупка по технологии S.I.L.S.
Новейший метод лапароскопической холецистэктомии выполняется при помощи специального устройства (порта), которое произведено из специального мягкого пластика. Устройство вводят сквозь единственный прокол, расположенный в околопупочной области. Через мягкий операционный пор, диаметр которого равен 23-24 миллиметрам, вводят лапароскопические инструменты и лапароскоп, диаметр которого 5 миллиметров. По окончанию операции устройство и желчный пузырь извлекают из брюшной полости. Накладывают косметический шов на маленькую рану, расположенную в пупочной области.
Метод малоинвазивной холецистэктомии через один прокол в области около пупка по технологии S.I.L.S. имеет преимущества перед традиционным лапароскопическим доступом:
- уменьшается число проколов на брюшной стенке;
- снижается болевой синдром после операции;
- наступает быстрая реабилитация пациента после операции;
- получается идеальный косметический эффект.
А по максимуму преимущества метода S.I.L.S. раскрываются в том случае, когда хирургу нужно извлечь большие и множественные камни в желчном пузыре. Если выполняется обычная лапароскопия, то хирургу нужно расширить прокол в области пупка чтобы извлечь больной орган.
У профессора Пучкова накоплен уникальный опыт по выполнению более 6 тысяч операций по лечению желчнокаменной болезни. Они выполнялись лапароскопическим способом с использованием различных методик, начиная с 1994 года и по настоящее время. Чтобы сделать оптимальный выбор метода по проведению малоинвазивной лапароскопической операции для лечения ЖКБ и ее осложнений разработали специальную программу и официально зарегистрировали ее в Роспатенте.
Использование этой программы и применение разработанных нами алгоритмов по диагностике и лечению, поможет лапароскопическому хирургу избежать интраоперационные осложнения и найти достойный выход из любой самой сложной хирургической ситуации.
Желчнокаменная болезнь
Народные средства при желчнокаменной болезни
Консервативное лечение желчнокаменной болезни
Хирургическое лечение заболеваний желчного пузыря
Записаться на консультацию в Швейцарскую клинику можно:
- по телефону: +7 925 191 56 65
- заполнить:ЗАПРОС В КЛИНИКУ
- по электронной почте: surgery@rusmedserv.com
- адрес клиники: г. Москва, ул. Николоямская, д.19, стр.1
(495) 506-61-01 — информация о швейцарской клинике в Москве
ЗАПРОС в КЛИНИКУ
Транслюминальная (N.O.T.E.S.) хирургия естественных отверстий включает целый ряд эндоскопических хирургических процедур, потенциально являющихся менее инвазивными, чем традиционные лапароскопические вмешательства. Эта хирургическая техника позволяет выполнять операции на органах брюшной полости, не делая разрезы кожных покровов передней брюшной стенки. Эндоскоп вводится в абдоминальную полость через естественные отверстия организма — влагалище, уретру, анус. Соответственно, внутренний разрез выполняется в заднем своде влагалища, желудке, мочевом пузыре или толстой кишке. Впервые эта методика использовалась для выполнения диагностических и лечебных процедур у животных и относительно недавно стала применяться при операциях у человека. Одновременно шло развитие несколько иной методики — единого лапароскопического доступа (ЕЛД).
В этой методике для выполнения операции на брюшной полости используется всего 1 разрез, чаще всего в пупке или над лобком [1]. В настоящее время можно встретить все больше публикаций, оценивающих эффективность данных методик, в том числе транслюминальных (N.O.T.E.S.) минилапароскопически ассистированных операций (ТМА) [2—5]. Несомненно, одной из наиболее часто встречаемых операций естественных отверстий и ЕЛД хирургии является холецистэктомия (ХЭ). В данный момент насчитывается около 150 публикаций, описывающих выполнение транслюминальной (N.O.T.E.S.) минилапароскопически ассистированной ХЭ, а также операции через единственный прокол передней брюшной стенки [1, 3, 4, 6, 7, 8—15].
За исключением очевидных косметических результатов, реальные преимущества транслюминальной и однопрокольной хирургии не совсем понятны. Выполнение самой операции обусловливает необходимость уверенных навыков в эндоскопической абдоминальной хирургии, обучение — большего времени, чем традиционная лапароскопия. Перед хирургами встают несколько принципиальных вопросов: действительно ли уровень послеоперационной боли ниже, чем после традиционной лапараскопической холецистэктомии (ЛХЭ). Приводит ли использование этих технологий к сокращению сроков пребывания больных в стационаре? Снижается ли длительность хирургического вмешательства? В качестве одного из шагов для разрешения данных вопросов мы приводим данные проспективного исследования, сравнивающего результаты выполнения транслюминальной (N.O.T.E.S.) минилапароскопически ассистированной, ЕЛД и традиционной ЛХЭ.
Цель — изучить результаты применения 3 различных методик в лечении неосложненной желчнокаменной болезни (ЖКБ) и полипоза желчного пузыря (ЖП).
Представляем проспективное исследование, включающее 147 пациентов, разделенных на три группы. 1-я группа (группа А) включала 51 пациента (31 женщину и 20 мужчин), которому выполнена традиционная (3-портовая) ЛХЭ. 2-я группа (группа В) включала 47 пациентов (33 женщины и 14 мужчин), которым выполнена ЕЛД ХЭ. 3-я группа (группа С) включала 49 пациенток, которым выполнена транслюминальная (N.O.T.E.S.) минилапароскопически ассистированная ХЭ. Все операции выполнены в период с 15 ноября 2010 г. по 1 декабря 2012 г. Показанием к операции послужили в группе А в 44 случаях — хронический калькулезный холецистит, в 2 случаях — бессимптомное камненосительство и в 5 — полипоз ЖП; в группе В в 43 случаях — хронический калькулезный холецистит, в 1 случае — бессимптомное камненосительство, в 3 — полипоз ЖП; в группе С в 43 случаях выполнена операция по поводу хронического калькулезного холецистита, в 3 случаях имелось бессимптомное камненосительство и в 3 — полипоз ЖП. Из 51 пациента в группе А у 2 (3,9%) были ранее перенесенные операции на органах брюшной полости, в группе В из 47 — у 4 (8,5%) и в группе С из 49 — у 2 (4%). Все операции выполнены под общей анестезией, одним хирургом с использованием жесткой оптики и инструментов.
Всем пациентам в обязательном порядке в предоперационном периоде выполнено ультразвуковое исследование (УЗИ) органов брюшной полости и малого таза. Во время УЗИ определяли размеры ЖП, толщину стенки, наличие или отсутствие перивезикального воспаления, размеры конкрементов, их количество, а также размеры полипа ЖП (табл. 1). С целью верификации диагноза в обязательном порядке проводили дуплексное сканирование полипа. В случае если во время исследования выявлялись косвенные признаки холедохолитиаза, мы рекомендовали выполнить эндоскопическое УЗИ для окончательной постановки диагноза. В группе С все пациентки в обязательном порядке были осмотрены гинекологом.
С целью верификации диагноза в обязательном порядке проводили дуплексное сканирование полипа. В случае если во время исследования выявлялись косвенные признаки холедохолитиаза, мы рекомендовали выполнить эндоскопическое УЗИ для окончательной постановки диагноза. В группе С все пациентки в обязательном порядке были осмотрены гинекологом.
Критерии включения в исследование: хронический калькулезный холецистит, бессимптомное камненосительство и/или полипоз ЖП, при котором требуется хирургическое лечение; для женщин в возрасте от 18 лет обязательны роды в анамнезе.
Критерии исключения: анестезиологический риск 3 и 4; острый холецистит; желтуха в анамнезе или УЗ-картина холедохолитиаза; явления острого панкреатита или перенесенный панкреонекроз; индекс массы тела более 40 кг/м2; воспалительные заболевания половых органов.
Послеоперационную абдоминальную боль регистрировали через 2, 4, 6, 12, 24, 48 и 72 ч после операции во время кашля, до приема анальгетиков. Для оценки послеоперационной боли использовали цифровую оценочную шкалу (NRS).
Техника выполнения хирургических вмешательств. Во всех группах операцию выполняли с наложением карбоксиперитонеума, нагнетаемое давление не превышало 15 мм рт.ст. Непосредственно перед разрезом в качестве антибиотикопрофилактики пациентам вводили однократно 2 мл цефтриаксона. При выполнении всех операций в месте разреза передней брюшной стенки производили предварительную инфильтрацию раствором наропина. После введения лапароскопа одним из первых этапов операции было распыление 40 мл наропина на оба купола диафрагмы с целью купирования френикус-симптома в раннем послеоперационном периоде.
Традиционную ЛХЭ выполняли с использованием 3 портов, расположенных стандартно (10-миллиметровый порт над пупком, 5-миллиметровый — в эпигастрии, 5-миллиметровый — в правом мезогастрии по среднеключичной линии). ЕЛД-вмешательства выполняли с применением SILS-порта («Covidien», США), S-порт и Endocone («Storz», Германия), которые вводили трансумбиликально с использованием открытой техники. Транслюминальную (N.O.T.E.S.) минилапароскопически ассистированную ХЭ выполняли следующим образом: после наложения карбоксиперитонеума по внутреннему краю пупка вводили 5-миллиметровый троакар и жесткий 30-градусный эндоскоп. Следующим этапом вводили удлиненный 10-миллиметровый троакар через задний свод влагалища в брюшную полость под контролем лапароскопа. Затем меняли 5-миллиметровый эндоскоп на 10-миллиметровый. Как только камера менялась, головной конец стола поднимался. В 5-миллиметровый порт вводили диссектор, дополнительно вводили 3-миллиметровый инструмент в правое подреберье.
Ушивали все разрезы на передней брюшной стенке, размеры которых более 5 мм. Прокол заднего свода влагалища также ушивали одиночными узловыми швами. Все операции завершены без установки страхового дренажа.
Выполнены все 147 ХЭ, при этом не было ни одной конверсии на традиционную ЛХЭ или открытую ХЭ. В табл. 2 представлены демографические различия между сравниваемыми группами.
представлены демографические различия между сравниваемыми группами.
В исследовании принимали участие 113 женщин и 34 мужчины, в группе A были 31 женщина и 20 мужчин, в группе В — 33 женщины и 14 мужчин, в группе С — 49 женщин. Средний возраст пациентов в группе А был 48,3 года (от 25 до 68 года), в группе В — 42,7 года (от 24 до 70 лет) и в группе С — 33,4 года (от 24 до 53 лет). Индекс массы тела (ИМТ) в группе А — 30,3 кг/м2, в группе В — 24,9 кг/м2 и в группе С — 26,8 кг/м2.
В каждой из исследуемых групп были пациенты с ранее перенесенными операциями на органах брюшной полости. В группе А (ЛХЭ) у 1 пациентки в анамнезе была открытая консервативная миомэктомия, у 1 пациента — разрыв пищевода с выполнением лапароторакотомического доступа. В группе В (ЕЛД) у пациенток были в одном случае — лапароскопическая аднексэктомия, в другом — энуклеация матки. У одного пациента — нижнесрединная лапаротомия, аппендэктомия, у другого — лапаротомия, как и у 3 пациенток в группе С (ТМА).
Результаты операции и послеоперационного периода представлены в табл. 3. Средняя длительность операции в исследуемых группах составила: в группе А (ЛХЭ) — 37,2 (20—63) мин, в группе В (ЕЛД) — 38,5 (28—71) мин и в группе С (ТМА) — 42,1 (31—70) мин. В группе А в 1 случае потребовалось введение дополнительно порта в правом подреберье, в 2 случаях дополнительное введение 5-миллиметрового порта в эпигастрии потребовалось в группе С (ТМА). В группе А нам пришлось использовать 1 трансабдоминальный «марионеточный» шов в 3 (5,88%) случаях и 2 шва в 1 (1,95%) случае. Трансабдоминальные «марионеточные» швы использованы во всех операциях ЕЛД, однако в 1 (2,12%) случае нам пришлось использовать 2 подобных шва. Использование «марионеточных» швов в группе С (ТМА) показало, что в 31 (63,2%) случае тракция ЖП с последующей диссекцией оказалась возможна благодаря введению лишь 1 шва, в 18 (36,8%) случаях было использовано 2 шва. Средняя кровопотеря составила 15 мл в группе А, 35 мл в группе В и 20 мл в группе С. В ходе вмешательства мы столкнулись со спаечным процессом в брюшной полости. В группе А (ЛХЭ) в 19 случаях к ЖП была подпаяна прядь большого сальника, в 1 случае мы выявили множественные плоские спайки между правой долей печени и диафрагмы, большим сальником и толстой кишкой. В группе В (ЕЛД) в 3 случаях к ЖП была подпаяна прядь большого сальника, в 2 случаях большой сальник был припаян к передней брюшной стенке. В группе С (ТМА) в 6 случаях к ЖП была подпаяна прядь большого сальника, в 7 — множественные перивезикальные спайки и у 1 пациентки имелся спаечный процесс в малом тазу. Среди пациентов группы А (ЛХЭ) у 2 имелись особенности расположения ЖП, а именно: внутрипеченочная локализация, в группе В (ЕЛД) такая локализация имелась у 3 пациентов. Средняя продолжительность пребывания в стационаре составила в группе А (ЛХЭ) 38,3 ч, в группе В (ЕЛД) — 24,3 ч, в группе С (ТМА) — 26,4 ч. Все пациенты еженедельно в течение 30 дней со дня операции проходили послеоперационное обследование, включающее УЗИ органов брюшной полости, а пациентки группы С также проходили осмотр гинеколога. Тошнота в послеоперационном периоде отмечена у небольшого числа пациентов во всех группах. Однако существенных различий между ними не наблюдалось. Анализируя уровень боли в послеоперационном периоде, мы отметили значительные различия через 12 ч после операции: в группе А (ЛХЭ) среднее значение составило 2,3, в то время как в группе В (ЕЛД) — 1,1. Кроме того, после 24 ч пациенты в группе В (ЕЛД) практически не ощущали боли и готовы были покинуть стационар, в группе А (ЛХЭ) среднее значение было 1,7. Пациенты группы С (ТМА) не требовали обезболивающих препаратов. Во всех группах не отмечено интра- и послеоперационных осложнений.
Средняя длительность операции в исследуемых группах составила: в группе А (ЛХЭ) — 37,2 (20—63) мин, в группе В (ЕЛД) — 38,5 (28—71) мин и в группе С (ТМА) — 42,1 (31—70) мин. В группе А в 1 случае потребовалось введение дополнительно порта в правом подреберье, в 2 случаях дополнительное введение 5-миллиметрового порта в эпигастрии потребовалось в группе С (ТМА). В группе А нам пришлось использовать 1 трансабдоминальный «марионеточный» шов в 3 (5,88%) случаях и 2 шва в 1 (1,95%) случае. Трансабдоминальные «марионеточные» швы использованы во всех операциях ЕЛД, однако в 1 (2,12%) случае нам пришлось использовать 2 подобных шва. Использование «марионеточных» швов в группе С (ТМА) показало, что в 31 (63,2%) случае тракция ЖП с последующей диссекцией оказалась возможна благодаря введению лишь 1 шва, в 18 (36,8%) случаях было использовано 2 шва. Средняя кровопотеря составила 15 мл в группе А, 35 мл в группе В и 20 мл в группе С. В ходе вмешательства мы столкнулись со спаечным процессом в брюшной полости. В группе А (ЛХЭ) в 19 случаях к ЖП была подпаяна прядь большого сальника, в 1 случае мы выявили множественные плоские спайки между правой долей печени и диафрагмы, большим сальником и толстой кишкой. В группе В (ЕЛД) в 3 случаях к ЖП была подпаяна прядь большого сальника, в 2 случаях большой сальник был припаян к передней брюшной стенке. В группе С (ТМА) в 6 случаях к ЖП была подпаяна прядь большого сальника, в 7 — множественные перивезикальные спайки и у 1 пациентки имелся спаечный процесс в малом тазу. Среди пациентов группы А (ЛХЭ) у 2 имелись особенности расположения ЖП, а именно: внутрипеченочная локализация, в группе В (ЕЛД) такая локализация имелась у 3 пациентов. Средняя продолжительность пребывания в стационаре составила в группе А (ЛХЭ) 38,3 ч, в группе В (ЕЛД) — 24,3 ч, в группе С (ТМА) — 26,4 ч. Все пациенты еженедельно в течение 30 дней со дня операции проходили послеоперационное обследование, включающее УЗИ органов брюшной полости, а пациентки группы С также проходили осмотр гинеколога. Тошнота в послеоперационном периоде отмечена у небольшого числа пациентов во всех группах. Однако существенных различий между ними не наблюдалось. Анализируя уровень боли в послеоперационном периоде, мы отметили значительные различия через 12 ч после операции: в группе А (ЛХЭ) среднее значение составило 2,3, в то время как в группе В (ЕЛД) — 1,1. Кроме того, после 24 ч пациенты в группе В (ЕЛД) практически не ощущали боли и готовы были покинуть стационар, в группе А (ЛХЭ) среднее значение было 1,7. Пациенты группы С (ТМА) не требовали обезболивающих препаратов. Во всех группах не отмечено интра- и послеоперационных осложнений.
Важным преимуществом лапароскопической хирургии является сохранение целостности передней брюшной стенки, снижение операционной травмы и уменьшение числа осложнений. Постоянное развитие миниинвазивного направления в лапароскопической хирургии привело к снижению операционной травмы путем уменьшения размеров троакаров, используемых во время хирургического вмешательства [16], что в свою очередь приводит к снижению послеоперационного дискомфорта [17], вероятности развития спаек [18] и послеоперационных грыж [19, 20]. Следующим шагом было использование 3 рабочих троакаров вместо 4, а также применение миниинструментов [21, 22]. Стало понятно, что лапароскопические и миниинвазивные методы были шагом в направлении к транслюминальной хирургии через естественные отверстия, позволившей выполнять хирургические вмешательства без видимых шрамов. В настоящее время мы можем проследить буквально взрывную эволюцию транслюминальной хирургии, что привело к появлению гибридных методик выполнения операций [4, 5]. Кроме того, инновационные эндоскопические инструменты дали реальный импульс к развитию хирургии единого доступа [4, 5, 13]. Тем не менее преимущества этих методик, даже очевидные, еще не всеми признаны.
Результаты нашего исследования показали, что не существует больших различий по длительности хирургического вмешательства. Незначительное увеличение продолжительности операции в группах В (ЕЛД) и группе С (ТМА) связано, по нашему мнению, с несколькими моментами. Мы считаем необходимым выполнение скрупулезной диссекции треугольника Кало в процессе выполнения ЕЛД или транслюминальной (N.O.T.E.S.) минилапароскопически ассистированной ХЭ с целью достижения безопасной визуализации его структур — «critical view of safety (CVS) dissection» (см. рисунок). Рисунок 1. Безопасная визуализация структур треугольника Кало. Стóит отметить, что игнорирование данного строгого правила неминуемо приводит к увеличению числа случаев повреждения желчевыводящих путей [23—27]. Следующим моментом, повлиявшим на окончательное время хирургического вмешательства, стал спаечный процесс в брюшной полости. В 1 случае в группе А (ЛХЭ) у пациента, перенесшего разрыв пищевода, нам пришлось ввести дополнительный порт в правом подреберье для осуществления безопасной диссекции структур печеночно-дуоденальной связки. Во время выполнения традиционной ХЭ в 7 случаях большой сальник «укутывал» ЖП, что у 3 (5,88%) пациентов обусловливало необходимость наложения 1 трансабдоминального шва, а у одного (1,95%) пациента — 2 швов. В группе В (ЕЛД) в 3 (6,38%) случаях мы сталкивались с прядью большого сальника, припаянного к ЖП, что потребовало введения в 1 (2,12%) случае наложения 2 «марионеточных» швов. В группе С (ТМА) в 7 (14,28%) случаях интраоперационно мы выявляли спаечный процесс в верхнем этаже брюшной полости, что в свою очередь потребовало введения дополнительного 5-миллиметрового порта во время 2 (4,08%) операций. Пациенткам группы С (ТМА) в 18 (36,8%) случаях из 49 во время операции мы накладывали 2 трансабдоминальных шва; показанием к этому послужили в 4 (8,16%) случаях камень диаметром около 17 мм (использование второго шва позволило «расправить» ЖП и провести диссекцию структур печеночно-двенадцатиперстной связки); в 8 (16,3%) случаях размеры ЖП превышали 130×90 мм и использование шва позволило провести безопасное выделение ЖП из ложа, в 6 (12,24%) случаях ЖП был «укутан» сальником.
Рисунок 1. Безопасная визуализация структур треугольника Кало. Стóит отметить, что игнорирование данного строгого правила неминуемо приводит к увеличению числа случаев повреждения желчевыводящих путей [23—27]. Следующим моментом, повлиявшим на окончательное время хирургического вмешательства, стал спаечный процесс в брюшной полости. В 1 случае в группе А (ЛХЭ) у пациента, перенесшего разрыв пищевода, нам пришлось ввести дополнительный порт в правом подреберье для осуществления безопасной диссекции структур печеночно-дуоденальной связки. Во время выполнения традиционной ХЭ в 7 случаях большой сальник «укутывал» ЖП, что у 3 (5,88%) пациентов обусловливало необходимость наложения 1 трансабдоминального шва, а у одного (1,95%) пациента — 2 швов. В группе В (ЕЛД) в 3 (6,38%) случаях мы сталкивались с прядью большого сальника, припаянного к ЖП, что потребовало введения в 1 (2,12%) случае наложения 2 «марионеточных» швов. В группе С (ТМА) в 7 (14,28%) случаях интраоперационно мы выявляли спаечный процесс в верхнем этаже брюшной полости, что в свою очередь потребовало введения дополнительного 5-миллиметрового порта во время 2 (4,08%) операций. Пациенткам группы С (ТМА) в 18 (36,8%) случаях из 49 во время операции мы накладывали 2 трансабдоминальных шва; показанием к этому послужили в 4 (8,16%) случаях камень диаметром около 17 мм (использование второго шва позволило «расправить» ЖП и провести диссекцию структур печеночно-двенадцатиперстной связки); в 8 (16,3%) случаях размеры ЖП превышали 130×90 мм и использование шва позволило провести безопасное выделение ЖП из ложа, в 6 (12,24%) случаях ЖП был «укутан» сальником.
Следует отметить, что продолжительность пребывания в стационаре у пациентов группы В (ЕЛД) и С (ТМА) была практически на 12 ч короче, чем в группе традиционной ЛХЭ. В ретроспективном анализе 297 ЕЛД ХЭ сообщается о средней длительности пребывания в стационаре 1,5 дня [6]. Еще в одном проспективном исследовании длительность пребывания в стационаре достигала 2,7 дня [28]. Таким образом, стало понятно, что использование миниинвазивных методик позволяет сократить продолжительность пребывания пациентов в стационаре.
Анализируя уровни послеоперационной боли, мы не могли не отметить, что трансвагинальный доступ имеет явные преимущества, касающиеся уровня послеоперационной боли при кашле. Так, пациентки группы С (ТМА) высказали желание покинуть стационар уже через 16 ч после операции. М. Hensel и соавт. [10] указывают на значительное снижение уровня послеоперационной боли при сравнении методик транслюминальной и традиционной ЛХЭ.
Е. Tsimoyannis и соавт. [14] сообщили, что уровень послеоперационной боли после ЕЛД ХЭ значительно ниже, чем после традиционной ЛХЭ. Мы считаем необходимым использовать все возможные превентивные методы для борьбы с послеоперационной болью. Введение местного анестетика в проекции намеченного разреза, распыление анестетика на купол диафрагмы является обязательным условием «отличного» самочувствия пациентов [29—31].
В настоящее время вопрос о тактике лечения пациентов с бессимптомным камненосительством в мировой практике практически решен. Ретроспективный анализ показал, что у 80% больных раком ЖП ранее были выявлены конкременты в нем, обуславливая таким образом ЖКБ предраковым состоянием [32]. Риск развития рака значительно увеличивается у пациентов с размерами конкремента 3 см и более, причем у женщин больше, чем у мужчин [33, 34]. Кроме того, доказана безуспешность диссолюционной терапии или проведение ударной волновой литотрипсии [35], так как частота рецидивов очень высока. Таким образом, проведение ЛХЭ показано следующим пациентам:
— с повышенным риском развития рака ЖП. Показателем этого является «фарфоровый» ЖП, наличие конкрементов в ЖП диаметром 3 см и более, полип ЖП диаметром более 10 мм;
— с повышенным риском развития осложненной ЖКБ. Этот показатель характеризуется наличием конкрементов ЖП диаметром более 2 см, конкременты 3 см и более, прикрывающие пузырный проток или «нефункционирующий» ЖП;
— с сопутствующими хроническими системными заболеваниями.
Всем пациентам в обязательном порядке мы проводим УЗИ органов брюшной полости, в том числе с целью выявления бессимптомного холедохолитиаза. В последние годы многие авторы поддерживают идею о том, что риск развития холедохолитиаза зависит как от размеров конкрементов ЖП, так и от их числа. Чтобы определить, насколько УЗИ помогает в постановке диагноза холедохолитиаза, проведено проспективное исследование с целью проверки теории о том, увеличивается ли риск миграции конкремента в общий желчный проток с уменьшением размера конкремента и увеличением их числа [36].
В результате получены данные, что уменьшение размеров конкремента (5 мм и менее) и увеличение их числа являются фактором, увеличивающим риск развития бессимптомного холедохолитиаза. Анализируя результат данного исследования, рекомендуем проводить пациентам с такой формой ЖКБ эндоскопическое УЗИ для окончательной постановки диагноза.
Наше исследование доказало определенные преимущества методики ЕЛД и транслюминальной (N.O.T.E.S.) минилапароскопически ассистированной хирургии в отношении сроков пребывания больных в стационаре в послеоперационном периоде. Кроме того, мы выявили огромное преимущество транслюминальной хирургии по сравнению с обычной и ЕЛД ХЭ в плане ранней послеоперационной боли.
Наше критическое сравнение этих техник не выявило сложностей в их выполнении в руках опытного хирурга, не пренебрегая принципами безопасности.

