Хронический гастродуоденит после удаления желчного пузыря

Постхолецистэктомический синдром (ПХЭС) — состояние после операции удаления желчного пузыря (холецистэктомии) по поводу хронического калькулезного холецистита. ПХЭС — это условное обозначение различных нарушений, повторяющихся болей и диспепсических проявлений, которые возникают у больных после холецистэктомии.
Постхолецистэктомический синдром. Причины
-
 допущенные диагностические ошибки до операции и технические погрешности во время операции,
допущенные диагностические ошибки до операции и технические погрешности во время операции, - функциональные нарушения, связанные с удалением желчного пузыря,
- обострение существующих до операции заболеваний, в первую очередь, болезней поджелудочной железы,
- развитие новых состояний желудочно-кишечного тракта в связи с удалением желчного пузыря (желчный рефлюкс в желудок, послабления стула, нарушения процессов переваривания пищи).
Функциональные нарушения сфинктерного аппарата желчевыводящих путей
В настоящее время считается доказанным факт, что после удаления желчного пузыря наблюдается повышение тонуса сфинктера Одди, причиной которого является исключение регулирующей роли сфинктера желчного пузыря и мышечной активности желчного пузыря на сфинктер Одди.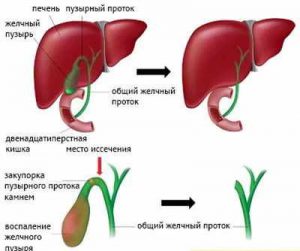
После удаления желчного пузыря включаются механизмы приспособления к работе желчевыводящих путей без желчного пузыря. Изменение моторной функции сфинктера Одди является одной из причин формирования острой или хронической боли в животе и диспепсического синдрома в послеоперационном периоде. Перестройка работы желчевыводящих путей после холецистэктомии может продолжаться до 1 года после операции.
Дисфункция сфинктера общего желчного протока и других сфинктеров желчевыводящей системы может приводить к повышению давления в протоках, застою желчи в них, что проявляется болями в правом подреберье или в подложечной области. Если преобладает дисфункция панкреатического протока, то появляется клиническая картина, характерная для панкреатита.
Разнообразие клинических проявлений ПХЭС затрудняет не только определение типа функциональных нарушений сфинктерного аппарата желчевыводящей системы, но затрудняет диагностику ПХЭС.
Нарушения печени, поджелудочной железы и кишечного тракта после холецистэктомии
Удаление желчного пузыря перестраивает процессы желчеобразования и желчевыделения.
- Отмечается увеличение образования желчи печенью, что является основной причиной поносов после холецистэктомии. Прием желчегонных препаратов в этих случаях нежелателен!
- Наиболее часто после удаления желчного пузыря страдает поджелудочная железа. При желчнокаменной болезни, дисфункции сфинктерного аппарата желчных путей, нарушении моторной функции желчного пузыря до операции формируется хронический билиарный пенкреатит (панкреатит, причиной которого является нарушения система желчеотделения).
- Иногда наблюдаются поражения протоковой системы, которые нарушают отток желчи – сужения, камни в протоках, увеличение лимфатических узлов, воспалительные заболевания в сфинктерно-протоковой системе.
Вследствие этого, обострения хронического панкреатита после удаления желчного пузыря встречаются достаточно часто — от 5 до 90 %. Такой разброс объясняется тем, что до операции не проведено достаточное обследование для оценки состояния поджелудочной железы, но в ряде случаев имеет место гипердиагностика хронического панкреатита.
В медицинской практике отмечается, что чем дольше существуют камни в желчном пузыре, тем чаще возникает хронический панкреатит.
В поджелудочной железе снижается объем секреции ферментов, развивается внешнесекреторная недостаточность функции поджелудочной железы, нарушаются процессы пищеварения. Холецистоэктомия, вовремя проведенная, способствует улучшению или нормализации показателей ферментативной функции поджелудочной железы.
После удаления желчного пузыря нередко нарушается функция 12-перстной кишки, что подтверждается появлением дуоденогастрального рефлюкса, т.е., заброс содержимого 12-перстной кишки в желудок, и вызывающего морфологические изменения в выходном отделе желудка и формирование хронического рефлюкс-гастрита (желчного).
После удаления желчного пузыря нарушается функция тонкой кишки (всасывания пищевых компонентов) и моторная функция толстой кишки (запоры, поносы).
Постхолецистэктомический синдром. Диагностика
Диагностика направлена на выявление различных заболеваний желудочно-кишечного тракта, которые пациент имел до операции, возникших после операции, возможные послеоперационные осложнения.
Диагноз устанавливается на основе:
- клинических проявлений болезни (жалоб пациента),
- объективных данных осмотра больного,
- лабораторных данных (биохимического исследования крови, клинического анализа крови, показателей обменных процессов – липидного, углеводного обменов, ферментативной функции поджелудочной железы, микрофлоры кишечного тракта),
- инструментальных методов обследования (ренгенологических, ультразвукового исследования гастродуоденоскопии),
- в более выраженных случаях – эндоскопической ретроградной холангиографии, компьютерной томографии, динамической сцинтиграфии.
Постхолецистэктомический синдром. Лечение и профилактика
В раннем послеоперационном периоде большое значение имеет лечебное питание, которое предусматривает часто дробное питание до 6 раз в день, небольшими порциями с ограничением жиров до 60-70 г в сутки.
С целью более быстрой адаптации пищеварительной системы к новым физиологическим условиям – функционирование без желчного пузыря, с учетом сопутствующих болезней рекомендуется более раннее расширение питания близкого к рациональному.
Постхолецистэктомический синдром. Лекарственная терапия по показаниям
С целью улучшения качества желчи, продуцируемой печенью, назначакются препараты урсодезоксихолевой кислоты (Урсосан, Урсофальк, Урсодез, Ливодекса, Эксхол, Холудексан, Урсодокса и др.). Доза продолжительность приема препарата определяется лечащим врачом.
Для связывания избытка желчи в кишечник и особенно наличие холагенной диареи назначаются сорбенты (Смекта) и антациды (Фосфалюгель, Маалокс, Алььагел и др.) по 1 пакету 3-4 раза в день через 1 час после еды в течение 7- 14 дней, режим приема и продолжительность определяется индивидуально.
При наличии боли в верхних отделах живота назначаются спазмолитики (например, Дюспаталин по 1 капсуле 2 раза в день, Дицетел по 50-100 мг 3 раза в день в течение 2-4 недель).
При наличии дуоденита, папиллита, появлении условно-патогенной флоры в посевах кала проводится 7-дневный курс антибактериальных препаратов. Препаратами выбора могут быть Эрцефурил, Интетрикс, Фуразолидон и др., реже антибиотики в общепринятых дозах.
При наличии сопутствующей патологии (панкреатит и др.) по показаниям назначаются ферментные препараты (Панкреатин, Мезим форте, Креон и др.).
Постхолецистэктомический синдром. Профилактика
Профилактика ПХЭС начинается уже в процессе подготовки к операции с целью выявления и своевременного лечения заболеваний гепатопанкреатодуоденальной зоны (заболеваний печени, панкреатита, дуоденита и эрозивно-язвенного процесса в 12-перстной кишке).
Особенно врача беспокоит состояние поджелудочной железы, и если до операции выявлен хронический панкреатит, необходимо провести курс лечения (антисекреторные препараты, спазмолитики, ферментные препараты, препараты урсодезоксихолевой кислоты). Эти мероприятия снижают риск возникновения обострений панкреатита в послеоперационный период в 2.5-3 раза.
Реабилитация
Опыт показывает, что признаки постхолецитэктомического синдрома чаще возникают в первый год наблюдения в период адаптации пищеварительного тракта в новых анатомических условиях.
Через 3-6 месяцев, хотя в настоящее время имеются сведении об успешном применении минеральных вод низкой минерализации после 10 дня после операции, показан прием минеральных вод, оптимальнее в условиях гастроэнтерологического питьевого курорта (Железноводск, Кашин, Дорохово, Карловы Вары и др.) с повторением курса минеральной воды в домашних условиях через полгода.
Диспансерное наблюдение пациентов проводится в течение первого года после операции.
 Билиарная (желчевыводящая) система включает желчные протоки и желчный пузырь. Важной клинической особенностью течения патологии билиарной системы является частое сочетание ее с другими заболеваниями органов пищеварения. В этом плане коморбидная пара «желчнокаменная болезнь — хронический гастрит» не является исключением.
Билиарная (желчевыводящая) система включает желчные протоки и желчный пузырь. Важной клинической особенностью течения патологии билиарной системы является частое сочетание ее с другими заболеваниями органов пищеварения. В этом плане коморбидная пара «желчнокаменная болезнь — хронический гастрит» не является исключением.
В настоящее время общепризнано, что желчнокаменная болезнь (холелитиаз) — многостадийный процесс, имеющий в своем развитии несколько последовательных этапов: от дискинезий желчного пузыря и сфинктерного аппарата желчевыводящих путей к хроническому бескаменному, затем — к хроническому калькулезному холециститу, последствиями хирургического лечения которого нередко является постхолецистэктомический синдром — симптомокомплекс, развивающийся после удаления желчного пузыря (холецистэктомии).
Хронический гастрит, как правило, сопутствует заболеваниям билиарной системы на каждом из этапов и, естественно, практически всегда имеет место при постхолецистэктомических расстройствах.
Тесные анатомические и функциональные взаимоотношения желчевыводящей системы и желудочно-кишечного тракта требуют выяснения общих механизмов формирования сочетанной патологии для дифференцированного подхода к выбору методов профилактики, терапии и реабилитации с учетом клинических особенностей течения каждого заболевания.
Особенно это имеет отношение к хирургическим вмешательствам, которые нередко являются единственно приемлемым способом лечения холелитиаза, поэтому изучение морфо-функциональных и клинико-патогенетических особенностей гастрита, ассоциированного с постхолецистэктомическими расстройствами, весьма актуально.
Несмотря на высокую частоту ассоциированного течения заболеваний билиарной системы и хронического гастрита, многие вопросы, касающиеся механизма развития гастрита и особенностей его течения, изучены недостаточно.
Дуоденогастральный рефлюкс
Именно дуоденогастральному рефлюксу придается основное значение в возникновении гастрита при заболеваниях желчевыводящей системы, включая постхолецистэктомический синдром. Однако сведения по этому вопросу противоречивы.
Ряд исследователей считает, что он является компенсаторно-приспособительным механизмом, поскольку закисление дуоденального содержимого при снижении его ощелачивающей способности может быть устранено только путем систематического заброса содержимого двенадцатиперстной кишки в желудок. Другие утверждают, что в результате постоянного и продолжительного рефлюкса прогрессируют деструктивные и дисрегенераторные изменения слизистой оболочки желудка, с ее структурной перестройкой по кишечному типу. Это сопровождается значительными изменениями переваривающей способности, снижением секреторной и моторной активности желудка.
Между тем, известно, что дуоденогастральный рефлюкс — явление физиологическое, встречается у здоровых лиц периодически при повышении моторной активности двенадцатиперстной кишки, однако при определенных условиях такой рефлюкс теряет свойства адаптационно-компенсаторного механизма и приобретает патологический характер. Установлено, что частота, продолжительность заброса и объем рефлюксата, поступающего в желудок, гораздо больше при нефункционирующем желчном пузыре, в связи с этим гастрит после удаления желчного пузыря большинством авторов именуется рефлюкс-гастритом. Тем самым подчеркивается роль рефлюкса как одного из важнейших эндогенных этиологических факторов хронического гастрита у данного контингента пациентов.
Однако есть и скептическое отношение к правомерности термина «рефлюкс-гастрит» при патологии билиарного тракта. Некоторые исследователи считают, что «истинный» рефлюкс-гастрит развивается у больных, перенесших операции на желудке, а у больных с неоперированным желудком при дуоденогастральном рефлюксе подобных изменений может и не быть.
Работ, специально посвященных изучению рефлюкс-гастрита при желчнокаменной болезни, а также влиянию хирургических вмешательств на его развитие и динамику, чрезвычайно мало. Между тем некоторые исследователи упоминают, что особенности хронического гастрита у пациентов с постхолецистэктомическим синдромом должны учитываться при оценке клинической картины и выборе адекватного метода их коррекции.
При заболеваниях желчевыводящей системы, включая желчнокаменную болезнь, по данным различных авторов, частота хронического гастрита колеблется от 68 до 83,4 %, а после удаления желчного пузыря достигает 100 %. По данным отечественной литературы, у пациентов, страдавших желчнокаменной болезнью, в 55 % наблюдений обнаружили неатрофический (поверхностный) гастрит, в 30 % — атрофический, в 15 % — гипертрофический; у 83 % больных хроническим калькулезным холециститом наблюдаются изменения слизистой оболочки желудка по типу энтеролизации преимущественно в антральном отделе желудка. По мнению некоторых исследователей, у больных после холецистэктомии наличие атрофии и метаплазии в антральном отделе желудка всех случаях можно рассматривать как проявление гастропатии химической (билиарной) природы вследствие дуоденогастральный рефлюкса.
Ряд исследователей считают типичными для морфологической картины рефлюкс-гастрита фовеолярную гиперплазию эпителия, определяя ее как экспансию слизистых клеток, а также отек и пролиферацию гладкомышечных клеток в собственной пластинке слизистой оболочки желудка на фоне умеренного воспаления. При рефлюкс-гастрите фовеолярная гиперплазия касается исключительно поверхностного эпителия и этим отличается от хеликобактерного гастрита, при котором развивается гиперплазия не только поверхностного, но и ямочного эпителия.
Патоморфологические изменения в желудке
Установлено, что выраженные изменения в слизистой оболочке желудка происходят при забросе всего дуоденального содержимого в желудок, а не отдельных компонентов. Экспериментально и клинически подтверждено повреждающее действие желчных кислот и их солей на слизистую оболочку.
По данным ряда исследователей возможно повреждающее действие трипсина на слизистую оболочку желудка в слабощелочной или нейтральной среде. Имеются сведения о повреждающем воздействии на слизистую желудка панкреатических ферментов и лизолецитина. Механизм действия желчных солей и лизолецитина на желудок до настоящего времени детально не изучен.
Заброс дуоденального содержимого в желудок, в пристеночной зоне которого рН постоянно составляет 1-1,5, сопровождается образованием нейтральных (недиссоциированых) желчных кислот за счет присоединения к их анионным группам ионов водорода. Лизолецитин, являясь мощным детергентом, «смывает» защитный слой слизи, покрывающий слизистую оболочку желудка. Нейтральные молекулы желчных кислот с рН 3,0—4,0 благодаря градиенту концентрации проникают через билипидные плазматические мембраны в межклеточное пространство покровно-эпителиального пласта вплоть до капиллярного ложа подслизистого слоя. Диффундируя в клетки эпителия желез, они угнетают в них слизеобразование, могут вызвать капиллярные кровотечения, острые дистрофические и эрозивные изменения слизистой желудка. Повышая скорость апоптоза эпителиальных элементов, желчные кислоты и их соли резко угнетают и пролиферативную активность клеток камбиальной зоны.
Аналогичные процессы происходят и в двенадцатиперстной кишке. Ввиду массивного поступления в кишку кислого желудочного содержимого при несостоятельности привратникового механизма в 12-перстной кишке возникает продолжительный сдвиг рН с 7,0-9,0 в межпищеварительный период до 1,5-3,0. В этих условиях значительная часть желчных кислот нейтрализуется и приобретает способность проникать в слизистую 12-перстной кишки.
После разрушения защитного барьера слизистая оболочка желудка теряет способность противостоять обратной диффузии ионов водорода. Желчные кислоты, попадая в просвет желудка вследствие дуоденогастрального рефлюкса, усиливают обратную диффузию ионов водорода в связи с их способностью переносить водородные ионы через биологические мембраны. Наибольшую агрессивность по отношению к слизистой желудка имеет тауродеоксихолевая кислота.
В слизистой оболочке желудка нарушается структура поверхностного и ямочного эпителия, учащаются некрозы обкладочных клеток. При этом регенерация слизистой оболочки происходит за счет увеличения количества клеток, продуцирующих слизь, и перестройки слизистой желудка по кишечному типу (энтеролизации), которая расценивается рядом авторов как предраковое состояние. Отмечается, что при рефлюкс-гастрите воспалительная инфильтрация либо минимальна либо вообще отсутствует, в собственной пластинке слизистой оболочки желудка много расширенных капилляров с утолщенными стенками и гладкомышечных клеток.
Хеликобактерии (Н.pylori — хеликобактер пилори) при рефлюкс-гастрите встречается значительно реже, чем при гастритах, не сопровождающихся рефлюксом, однако это относится в первую очередь к рефлюкс-гастриту, возникающему после операций на желудке. Анализ морфологической картины слизистой желудка позволил наряду с хеликобактерным и рефлюкс-гастритом выделить и гастрит смешанной этиологии, который возникает путем трансформации хеликобактерного гастрита в рефлюкс-гастрит под влиянием рефлюкса. Он характеризуется всеми морфологическими признаками рефлюкс-гастрита, однако отличается от него не только наличием хеликобактерий, но и большей воспалительной инфильтрацией и активностью. Выраженность обсеменения Н.pylori меньше, чем при хеликобактерном гастрите.
Таким образом, все морфологические характеристики рефлюкс-гастрита в основном относятся к гастриту оперированного желудка либо к хроническому гастриту при калькулезном холецистите. Детального описания слизистой оболочки желудка при ПХЭР не приводится, что, с учетом частого коморбидного течения гастрита и ПХЭР, должно служить поводом для изучения данной проблемы.
Функциональная активность желудка
Что касается особенностей функциональной активности желудка при заболеваниях желчевыводящей системы, то данные о кислотообразующей и моторной функции желудка противоречивы. По данным отечественной литературы было выявлено нарушения этих функций в виде снижения объема желудочной секреции и дебита свободной соляной кислоты в обе фазы сокоотделения, а также замедление эвакуации желудочного содержимого и гипотонию 12-перстной кишки. Данные нарушения находились в прямой зависимости от длительности заболевания — чем больший «стаж» был у хронического холецистита (в особенности с частыми рецидивами), тем в большей степени страдали функции желудка.
Ряд исследователей считают, что существовавшие до удаления желчного пузыря изменения секреторной функции желудка после операции усугубляют поражения желчевыводящих путей. При этом возможны следующие варианты: снижение секреции в сочетании с усилением моторики, стойкая секреторная недостаточность (гастрогенные поносы), либо (очень редко) повышение секреторной функции с возможным развитием язвенной болезни желудка и двенадцатиперстной кишки.
Холецистэктомия усугубляет функциональные нарушения желудка, более того, гипоацидный гастрит в сочетании с билиарной недостаточностью и ферментативной недостаточностью поджелудочной железы является причиной формирования синдрома нарушенного всасывания, нередко развивающегося после удаления желчного пузыря. При этом наибольшее снижение кислотообразующей функции желудка отмечается у больных с длительностью анамнеза ЖКБ свыше 10 лет. По данным отечественной литературы при проведении суточной рН-метрии желудка и пищевода у пациентов с заболеваниями желчного пузыря было выявлено преобладание гиперацидности (у 63 % человек), тогда как гипоацидность встречалась у 32 % больных, нормоцидность — у 5 %. В связи с этим для выбора адекватной терапии больным авторы рекомендуют мониторирование желудочной секреции.
Сведений о моторной функции желудка после удаления желчного пузыря крайне мало. По данным ряда исследователей у пациентов после удаления желчного пузыря, при развитии у них атрофического гастрита обнаруживалась акинезия желудка и гипокинезия двенадцатиперстной кишки; у абсолютного большинства пациентов выявлялись несколько вариантов нарушений моторики гастродуоденальной зоны после холецистэктомии:
- ускорение эвакуации из желудка с одновременным замедлением дуоденального транзита,
- сочетанное замедление эвакуации из желудка и ДПК,
- замедление эвакуации из желудка при нормальной эвакуации из ДПК,
- ускорение эвакуации из желудка при нормальной эвакуации из ДПК,
- замедление дуоденального транзита при нормальной моторной функции желудка.
Лишь у 8,2 % обследованных ими пациентов моторная функция гастродуоденальной зоны нарушена не была. Противоречивые данные о моторной функции желудка у больных после холецистэктомии требуют детального ее изучения в сопоставлении с морфологическими особенностями хронического гастрита и кислотообразующей функцией желудка.
Симптомы хронического гастрита
Совокупность и многообразие клинических проявлении хронического гастрита у больных, перенесших холецистэктомию, в литературе детально не охарактеризована. По мнению ряда исследователей дуоденогастральный рефлюкс и ассоциированный с ним рефлюкс-гастрит, сопутствующие желчнокаменной болезни, определенным образом отражаются на клинических проявлениях и характере течения заболевания.
Наиболее частыми симптомами рефлюкс-гастрита при желчнокаменной болезни являются постоянная, нередко жгучая, боль в эпигастральной области и левом подреберье, усиливающаяся после приема любого вида пищи, тошнота, горечь во рту, ухудшение аппетита, периодически — рвота желчью, приносящая облегчение. Указанные признаки не исчезают после приема антацидов и спазмолитиков, не корригируются диетой. Этими же исследователями было показано усиление проявлений вегетодистонии при обострении рефлюкс-гастрита.
Для больных желчнокаменной болезнью с сопутствующим рефлюкс-гастритом и хроническим панкреатитом характерны потеря в массе тела, развитие железодефицитной анемии. После удаления желчного пузыря клиника хронического гастрита редко выходит на первый план, как правило, доминируют функциональные нарушения печени, желчевыводящих путей и поджелудочной железы.


