Хирургическое лечение кардии желудка
Благодаря выраженной симптоматической картине, данную патологию выявляют на ранних стадиях. Отсутствие лечения приводит к медленному прогрессированию болезни и развитию тяжелых осложнений, среди которых — рак пищевода.
Наиболее оптимистические прогнозы связаны с ранним хирургическим лечением. Медикаментозная и консервативная терапия лишь на время устраняют проявления ахалазии кардии пищевода – однако, в ряде случаев, рецидив дает о себе знать уже через полгода.
Люди с таким диагнозом должны регулярно посещать гастроэнтеролога и ежегодно проводить необходимые обследования.
Методы диагностики ахалазии кардии пищевода — дифференциальная диагностика
Диагностика рассматриваемой болезни начинается с беседы с пациентом и его осмотра. Однако подобных мероприятий недостаточно для постановки точного диагноза.
Недостаточность кардии желудка по своей клинической картине схожа с иными патологиями желудочно-кишечного тракта:
- Сужением пищевода.
- Дивертикулярной болезнью.
- Наличием злокачественных и доброкачественных новообразований.
В обязательном порядке пациенту назначают пройти лабораторное исследование крови и мочи на предмет наличия воспалительных процессов, а также с целью определения некоторых других показателей.
Однако, чтобы достоверно убедиться в наличии ахалазии кардии пищевода, необходимо проводить инструментальное обследование:
-
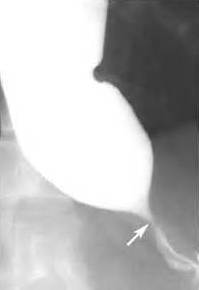 Рентгенография грудной клетки. Если указанная процедура выявила наличие затемненного участка пищевода, что содержит жидкость, назначают рентгенографию пищевода с предварительным приемом бариевой взвеси. Зачастую данная манипуляция сразу подтверждает указанный диагноз. Распознать недуг можно по т.н. симптому «перевернутого пламени свечи»: в нижней секции пищевод сужается, а сверху он расширен.
Рентгенография грудной клетки. Если указанная процедура выявила наличие затемненного участка пищевода, что содержит жидкость, назначают рентгенографию пищевода с предварительным приемом бариевой взвеси. Зачастую данная манипуляция сразу подтверждает указанный диагноз. Распознать недуг можно по т.н. симптому «перевернутого пламени свечи»: в нижней секции пищевод сужается, а сверху он расширен. - Эзофагоскопия. Помогает определить стадию развития патологии. На начальных этапах ярких изменений нет. На запущенных стадиях визуализируют большой просвет пищевода, а в некоторых случаях также присутствует слизь, жидкость, остатки пищи. Стенки пищевода толще нормы, иногда на них видны язвенные изменения, эрозии. По показаниям, в ходе рассматриваемой процедуры может быть проведена биопсия. Взятый материал в дальнейшем направляют на гистологическое исследование для исключения рака пищевода.
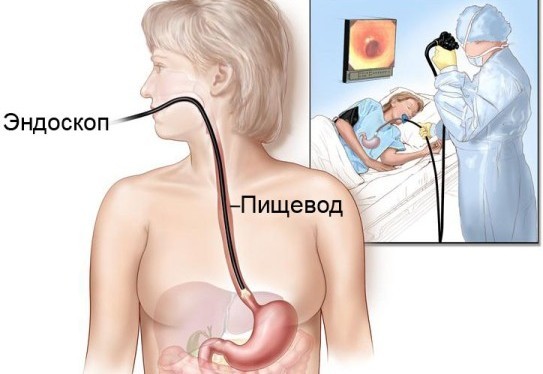 При ахалазии кардии эндоскоп всегда свободно проходит к желудку. Если этого не происходит, следует предположить у пациента иную патологию: онкозаболевание, сужение пищевода и пр.
При ахалазии кардии эндоскоп всегда свободно проходит к желудку. Если этого не происходит, следует предположить у пациента иную патологию: онкозаболевание, сужение пищевода и пр. - Эзофагоманометрия. Применяется для измерения перистальтики и внутрипищеводного давления. Манипуляции осуществляются в состоянии покоя и при глотании.
Лечение ахалазии кардии пищевода – терапия и народные средства
Лечебные мероприятия по устранению данной патологии носят комплексный характер. Хирургическое вмешательство сочетают с медикаментозной и консервативной терапией.
Кроме того, больным нужно пересмотреть свой образ жизни: питание должно быть дробным и щадящим, физические нагрузки — умеренными, а режим труда и отдыха — адекватным.
Полезными будут ежедневные прогулки на свежем воздухе, плавание в бассейне, дыхательная гимнастика, а также лечебная физкультура.
Для каждого пациента соответствующий специалист подбирает собственную программу упражнений: нагрузки на пресс при этом исключают.
Одно только лечение посредством приема лекарственных препаратов практикуют на начальных стадиях заболевания, когда выраженных дегенеративных изменений еще нет.
Однако, согласно статистическим данным, подобная терапия имеет успех лишь в 10% случаев. Зачастую ее применяют в отношении пожилых людей, которым противопоказано хирургическое вмешательство.
Основная задача медикаментов — устранение симптомов ахалазии кардии пищевода.
С этой целью назначают:
- Нитраты: Изосорбид, Нитросорбид, Динитрат. Данная группа препаратов способствует расслаблению мускулатуры пищевода, нормализации перистальтики. Не исключено появление побочных эффектов: пациенты могут жаловаться на слабость, головокружение, головную боль. Аналогичными свойствами обладают антагонисты кальция.
- Миотропные спазмолитики: Папаверин, Дротаверин, Платифиллин, Галидор. Их цель — ликвидация спазма сфинктера, что в нижней секции пищевода.
- Обезболивающие средства при выраженном болевом синдроме. Зачастую для данных целей применяют Новокаин.
- Седативные препараты: валериана, пустырник и пр. С их помощью удается расслабить мускулатуру гортани, а также улучшить психоэмоциональное состояние больного.
- Общеукрепляющая терапия: витамины, стероиды, раствор глюкозы.
Таблетизированная форма препаратов вызывает определенные сложности, связанные со спецификой рассматриваемой болезни. Для лучшего проталкивания лекарственных средств в желудок врачи рекомендуют принимать их вместе с едой, либо класть под язык и рассасывать.
Если ни один из вариантов не пригоден в силу симптоматических проявлений, прибегают к внутримышечному введению медикаментов.
Средства народной медицины в лечении недостаточности кардии желудка могут использоваться исключительно, как вспомогательная методика. С их помощью можно купировать проявления некоторых симптомов, а также укрепить защитные реакции организма.
Наиболее популярными в этой сфере являются следующие рецепты:
- Отвар, содержащий шиповник, листья крапивы, плоды боярышника, корень заманихи, родиолу розовую. Всех ингредиентов необходимо взять поровну, чтобы в общем получилось 1,5 ст.л. В полученную смесь добавляют 1 ч.л. зверобоя. Все это заливают 2 ст. кипятка и настаивают на паровой бане 15-20 мин. Полученный травяной чай следует принимать за полчаса до еды по 70 гр.
- Отвар из ромашки. Благоприятствует устранению воспалительных явлений в пищеводе. Аналогичными свойствами обладает также календула. Для приготовления отвара необходимо залить 2 ст.л. любой из указанных трав стаканом горячей воды и выстоять на паровой бане четверть часа.
- Настойка из корня женьшеня. Повышает защитные реакции организма. Указанное средство принимают ежедневно перед едой по 20 капель.

На начальных этапах развития ахалазии кардии, в целях лечения применяют инъекции ботулотоксина. Указанное вещество вводят посредством эндоскопа. Слизистую обкалывают в 4 местах. Каждая инъекция содержит 60 ЕД действующего вещества.
Эффект от подобной методики длится, в среднем, полгода, после чего процедуру повторяют — и так до конца жизни. Подобное лечение невыгодно для пациентов — инъекции стоят немалых денег, а постоянные обострения негативно сказываются на качестве жизни.
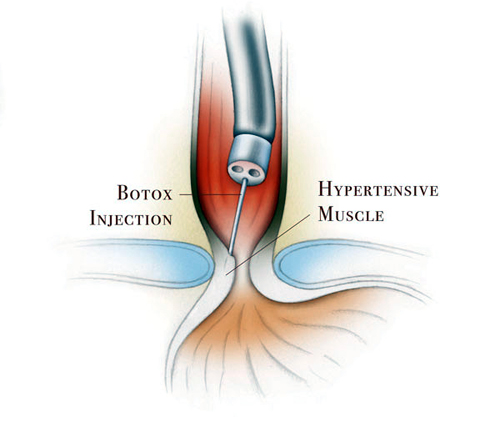
Инъекции ботулотоксина в лечении ахалазии кардии пищевода
Помимо всего прочего, на II и III стадии ахалазии кардии проводят малоинвазивную манипуляцию — пневмокардиодилатацию. Ее суть заключается в установке баллонного катетера либо бужа в просвет кардии.
Для достижения необходимого эффекта, требуется несколько сеансов с перерывами в 1-2 дня. С каждым последующим сеансом увеличивают диаметр баллона. Это способствует надрыву мышечной ткани, либо ее растяжению в суженном участке.
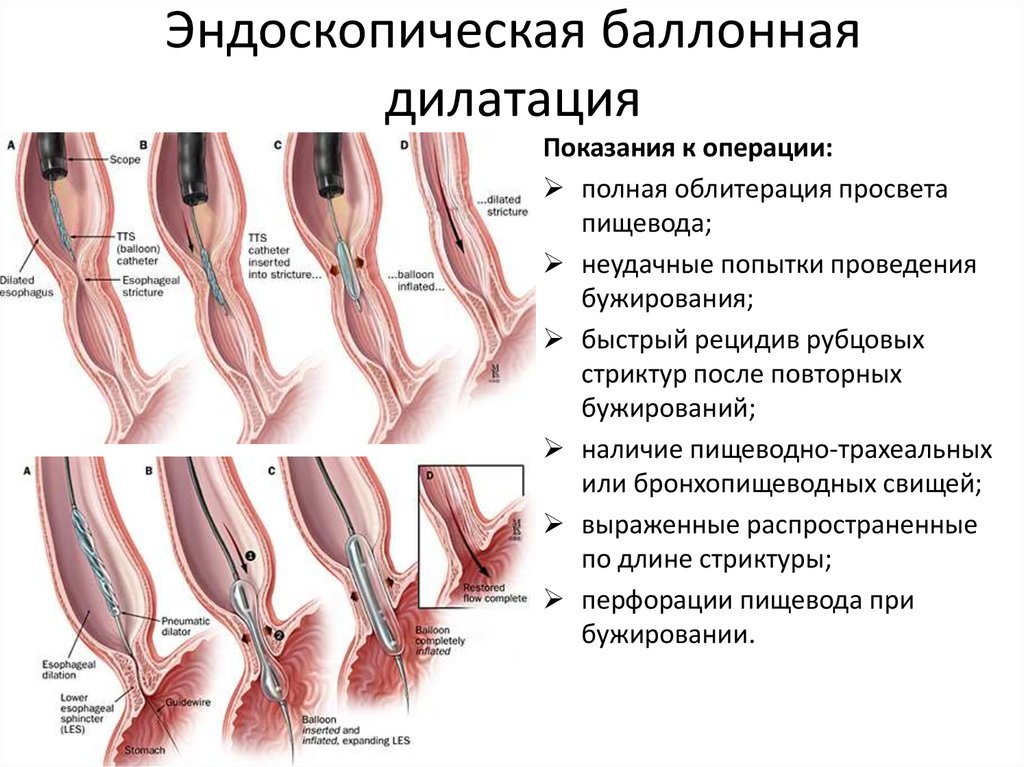
Перед указанной процедурой пациенту внутривенно вводят растворы димедрола и атропина, благодаря чему купируются рвотные позывы и минимизируются болевые ощущения.
У некоторых пациентов уже после первой процедуры отмечаются значительные улучшения.
Но пневмокардиодилатация может иметь негативные последствия, к которым относят:
- Трещины в районе пищевода либо его разрыв.
- Рубцовые изменения патологического сфинктера.
- Появление рефлюкс-эзофагита.
Нужна ли операция при недостаточности кардии желудка – показания к хирургическому вмешательству
Хирургическое лечение рассматриваемой патологии является наиболее эффективным: с его помощью можно избавиться от недуга на 8-10 лет.
Показанием для операции являются следующие состояния:
- Отсутствие эффекта от консервативной терапии и малоинвазивных вмешательств.
- Запущенные стадии болезни.
- Лечение детей.
Все виды операций по поводу недостаточности кардии пищевода можно разделить на 2 больших группы:

Фундопластика по Тупе
Миотомия по Геллеру через лапароскопический доступ. На передней стенке пищевода делают разрез продолжительность 8-10 см. Края оперируемого органа разводят в противоположные стороны, после чего хирург иссекает мышечный слой пищевода и желудка. Благодаря применению эндоскопа, доктор может визуализировать самые мелкие анатомические структуры в рабочем участке. Для минимизации риска развития послеоперационных обострений, доктор должен выполнить тщательную ревизию обнаженной слизистой оболочки. Если в этом есть необходимость, слизистую ушивают с обязательным ее прикрытием передней стенкой желудка. Подобную процедуру именуют фундопластикой, — она может осуществляться по нескольким методикам, и способствует предотвращению развития гастроэзофагеального рефлюкса.
- Операции по удалению нерабочих участков патологического сфинктера — резекционные методики. Подобные вмешательства зачастую проводят на запущенных стадиях недуга.
Возможные послеоперационные осложнения и их профилактика
После хирургического лечения рассматриваемой патологии, у пациента остаются небольшие разрезы на животе — следы лапороскопии.
В стационаре он остается 3-5 дней, а через 2-3 недели ему уже можно приступать к работе.
Первые пару месяцев следует придерживаться строгой диеты.
Операция по устранению ахалазии кардии чревата следующими осложнениями:
- Образование дивертикул и рубцов в области разреза мышечной оболочки патологического органа.
- Воспалительные явления в плевре, средостении и/или брюшине. Они могут быть вызваны травмированием слизистой оболочки во время операции, которое хирург упустил из виду. Чтобы избежать подобного обострения, следует тщательно осматривать слизистую и при выявлении поврежденных участков — производить их ушивание. Кроме того, с целью минимизации риска инфицирования оперируемого участка за 16 часов до операции пациенту начинают давать антибиотики.
- Развитие пептического рефлюкс-эзофагита. Избежать данного негативного последствия можно, максимально сохранив естественную анатомическую взаимосвязь между желудком, диафрагмой и пищеводом.
- Рецидив недостаточности кардии пищевода вследствие срастания его стенок. Избежать подобного явления можно посредством применения собственных тканей для укрытия хирургического дефекта стенки пищевода. Однако такая манипуляция является технически сложной, и не все доктора берутся за ее выполнение.
Изобретение относится к медицине, хирургии, может быть использовано для хирургической коррекции клапанной недостаточности кардии. Обнажают заднее средостение передним внеплевральным доступом. Рассекают переднюю часть пищеводно-диафрагмальной связки. Выводят в средостение 5 см передней стенки желудка. Фиксируют переднюю стенку желудка к передней и боковым дугам кольца пищеводного отверстия диафрагмы на протяжении 1,5 см с каждой стороны. Погружают переднюю стенку желудка под переходную зону пищевода в виде дупликатуры. Сшивают связку. Способ позволяет повысить функциональную надежность антирефлюксного клапана. 7 ил.
Изобретение относится к медицине и может быть использовано в грудной хирургии при коррекции клапанной недостаточности нормально расположенной кардии.
Запирательная функция кардии складывается из двух компонентов: сфинктерной, носителем которой являются кольцевидные пучки мышц в зоне пищеводно-желудочного перехода (ПЖП) и клапанной, принадлежащей клапану Губарева, образованному складками слизистой пищевода, выступающими в просвет желудка (1). Кардиальный сфинктер изначально слаб и, при отсутствии функции клапана Губарева, самостоятельно может сдерживать лишь небольшое давление желудочного содержимого. Нормальное функционирование клапана Губарева возможно при условии сохранения острого угла между левой стенкой пищевода и дном желудка (угол Гиса), а также толщины слизистой дистального отдела пищевода, достаточной для герметичного смыкания стенок пищевода на входе в желудок. Нарушение этих взаимоотношений приводит к утрате функции клапана, способного сдерживать желудочно-пищеводный рефлюкс (ЖПР) при более высоком давлении желудочного содержимого. Под действием кислой среды сфинктер вначале усиливает свой тонус и, какое то время, препятствует ЖПР. Но постепенно эпизодический ЖПР переходит в постоянный. В результате развивается рефлюкс-эзофагит (РЭ). Сфинктер ослабевает и теряет способность смыкаться. При ФЭГС исследовании он зияет.
Тяжелые клинические проявления этой патологии в виде загрудинных болей, мучительной изжоги, регургитации желудочного содержимого в горизонтальном положении, особенно во время сна, хронического кашля, астматического бронхита, анемии и множества других симптомов заставляют больного обратиться к врачу. Нередко сам рефлюкс-эзофагит остается незамеченным в дебрях многочисленных симптомов.
У 62% больных недостаточность запирательной функции кардии и РЭ обусловлены скользящими грыжами пищеводного отверстия диафрагмы (СГПОД), когда кардия находится в заднем средостении, а угол Гиса развернут до величины тупого (2). У остальных 38% — кардия дислоцируется под диафрагмой, а ее функция нарушена вследствие других причин: длительной неукратимой рвоты у беременных, длительного пребывания в пищеводе транснозального желудочного зонда, опухоли, резекции желудка и т.д. (3). В 1953 г. Lortat-Jacob и Robert выделили патологическое состояние, при котором пищеводно-желудочный угол (угол Гиса) оказывается развернутым, хотя при этом кардия и остается расположенной ниже диафрагмы (1.Цитата, с. 180).
Операции, направленные на устранение клапанной недостаточности кардии и ЖПР, складывались из различных оперативных приемов. Недостаточность кардии и РЭ, в подавляющем большинстве случаев, рассматривали как следствие СГПОД. Поэтому в операциях всегда предусматривались приемы устранения грыжи и фиксации желудка к различным анатомическим образованиям, находящимся под диафрагмой или к самой диафрагме.
Оперативные приемы, направленные непосредственно на устранение клапанной недостаточности кардии и ЖПР — антирефлюксные операции, зависели от понимания принадлежности клапанной функции. Их можно разделить на группы: 1) Сужение кольца пищеводного отверстия диафрагмы (КПОД) за счет сшивания ее ножек позади или впереди пищевода его или укорочения правой ножки диафрагмы выполняли хирурги, считавшие, что антирефлюксная функция принадлежит мышцам, образующим КПОД. Непременным условием, позволяющим как-то контролировать достаточность сужения, было наличие толстого желудочного зонда в пищеводе и свободное вхождение кончика указательного пальца хирурга между КПОД и стенкой пищевода. Зону пищеводно-желудочного перехода фиксировали к диафрагме снизу. Из трансплеврального доступа эту операцию выполнял Allison P. R. (4), из трансабдоминального — Harrington S.W.(5), Каунитц (6) и др. Операция не получила широкого признания, т.к. в отдаленные сроки хирурги наблюдали до 80% рецидивов РЭ и СГПОД (7). Многие хирурги, оперирующие СГПОД, используют этот прием и в настоящее время, но некоторые считают, что сужение КПОД не влияет на результаты операций и целесообразно только при лечении параэзофагеальных и СГПОД больших размеров (8); 2) усиление жомной функции кардиального сфинктера при помощи окутывания дном желудка дистального отдела пищевода — фундопликация по Ниссену (9) из трансабдоминального доступа. Шалимов А.А. и Полупан В.Н. описали и иллюстрировали схемами некоторые модификации этой операции (Тупе, Шалимова) в атласе операций на пищеводе, желудке и ДПК (10). Известны и более поздние модификации, выполняемые через плевральную полость (11) и через живот (12, 13). Большинство из них вобрали в себя все перечисленные выше хирургические приемы. Отличия от операции Ниссена заключаются в том, что окутывание пищевода дном желудка уменьшилось до 180 и 240 градусов окружности, а дно желудка проводилось спереди от пищевода (Dor) или сзади (Toupet), применена фиксация дна желудка к куполу диафрагмы и к правой ее ножке. Большое количество модификаций означает неудовлетворенность результатами первоначальной операции из-за осложнений, возникающих во время ее выполнения — разрыв селезенки, внутрибрюшное кровотечение, в ближайшие и отдаленные сроки — дисфагия, атония желудка, поддиафрагмальный абсцесс, рецидив ЖПР, отрыв манжетки (14, 15); 3) восстановление острого угла Гиса путем подшивания левой стенки пищевода к дну желудка (16, 17) применяется в сочетании с приемами гастропексии и диафрагмофундорафии при операциях Хила, Латаста, Туле, Шалимова и др. К сожалению, этот хирургический прием не всегда приводит к восстановлению функции клапана Губарева. Рецидив ЖПР и РЭ — яркое этому подтверждение. Вероятно, этот оперативный прием не всегда обеспечивает герметичное прилегание стенок пищевода на входе в желудок; 4) формирование поперечной складоки передней и левой боковой стенки дистального отдела пищевода и субкардиального отдела желудка из трансплеврального доступа — операция Mark IV — Belsey R. По описанию Шалимова А.А., Саенко В. Ф. , Шалимова С.А. в монографии «Хирургия пищевода», 1975 г. (3), операцию Belsey выполняют из левого трансплеврального заднебокового доступа по VII — VIII межреберью. Пищевод мобилизуют до нижней легочной вены с сохранением блуждающих нервов. Рассекают пищеводно-диафрагмальную связку. Дно желудка втягивают в плевральную полость через расширенное КПОД. Нередко для этого пересекают и перевязывают 1 или 2 короткие желудочные артерии. Накладывают провизорные швы на ножки диафрагмы. По передней и левой боковой поверхности пищевода и кардии накладывают продольные серозно-мышечные швы, образующие поперечные складки-пликации. Пищевод прошивают на 2-3 см выше, а желудок — на 2 см ниже пищеводно-желудочного соединения. После завязывания этих швов накладывают второй ряд швов, п-образно прошивающих сухожильную часть диафрагмы на расстоянии 2 см от КПОД, желудок — на 2 см ниже, а пищевод на 1 см выше линии предыдущих швов. После завязывания второго ряда швов, дно желудка и пищевод оказываются фиксированными к диафрагме, а кардия — погруженной в брюшную полость. Завязывают провизорные швы на ножках диафрагмы. Ушивают торакотомную рану.
Слабым местом операции является слишком большой суммарный захват в швы стенки пищевода (до 4 см). Это нецелесообразно потому, что натяжение тканей пищевода на линии второго ряда швов, при его продольных сокращениях и укороченности, неизбежно приводит к их прорезыванию. Дубликатура, образованная первым рядом швов и обращенная внутрь, может выполнять функцию антирефлюксного клапана, если ее край будет соприкасаться с противоположными стенками субкардиального отдела желудка. Но этого не происходит при прорезывании швов на стенке пищевода. Рецидив ЖПР после этой операции достигает 15% (18).
Недостатки операции: в травматичном доступе и несовершенстве клапанного механизма. Ей присущи все те осложнения, которые бывают и при других операциях, выполняемых из трансплеврального доступа.
Операция Ниссена в модификации Nadjafi A. (19). Автор дополнил фундопликацию Ниссена из трансабдоминального доступа формированием глубокой дубликатуры передней стенки желудка. Выполнено 14 операций. В отдаленные сроки от 18 до 24 месяцев больные не предъявляли жалоб. Сочетание двух антирефлюксных приемов не дают право присвоить заслугу в этих результатах одному из них. Но, вероятно, их сочетание сыграло свою положительную роль.
В двух последних операциях мы усматриваем рациональные моменты, заключающиеся в формировании антирефлюксного клапана из передней стенки желудка, в виде дубликатуры, обращенной в его просвет. Их можно рассматривать как прототип предлагаемого мною способа хирургической коррекции клапанной недостаточности кардии, базирующегося на концепции, рассматривающей недостаточность кардии как следствие нарушения функции клапана Губарев. Поэтому ее коррекцию я выполняю без вовлечения в антирефлюксную операцию сфинктерного компонента. Его функция нарушается вторично. После устранения ЖПР и РЭ она может нормализоваться.
ЗАДАЧА ИЗОБРЕТЕНИЯ — уменьшить травматичность хирургической коррекции клапанной недостаточности нормально расположенной кардии и повысить функциональную надежность антирефлюксного клапана.
Поставленную задачу решают за счет обнажения заднего средостения передним внеплевральным доступом, рассечения передней части диафрагмально-пищеводной связки, выведения в средостение 5 см передней стенки желудка, фиксации к передней и боковым дугам КПОД на протяжении 1,5 см с каждой стороны, погружения ее складки под переходную зону пищевода в виде дубликатуры и сшивания связки.
МЕТОДИКА ОПЕРАЦИИ.
Положение больного на спине. Наркоз эндотрахеальный с ИВЛ.
Доступ к заднему средостению передний внеплевральный наддиафрагмальный, разработанный мною ранее (Заявка на изобретение 9911069/14 �1866, приоритет от 02.06.1998 г.), проходящий между левой среднеключичной линией и краем грудины по VI межреберью послойно до внутренней грудной фасции. Далее разрез продлевают вниз до конца мечевидного отростка с анатомичным отделением VII ребра от грудины. У края грудины фасцию перфорируют и проникают пальцем в нижний треугольник переднего средостения. Конец VII ребра отводят книзу. Переднюю переходную складку плевры отслаивают от грудной стенки к верхушке сердца. Фасцию рассекают по межреберью до среднеключичной линии. В рану вводят реечный ранорасширитель и разводят ее края до 10 см. При этом обнажают переднюю линию сращения перикарда с диафрагмой. Ее очищают от жировой клетчатки. Между нижней грудино-перикардиальной связкой и верхушкой сердца рассекают образующие ее фиброзные волоски. По наружной дуге верхушки сердца сращения не рассекают, во избежание повреждения диафрагмального нерва. Далее их разделяют кзади вдоль линии, соединяющей грудино-перикардиальную связку и левую стенку нижней полой вены. Там они наиболее прочные и служат ориентиром направления. От верхушки сердца, по мере углубления доступа, зону рассечения сращений суживают (фиг. 1). К моменту достижения задней линии сращения, на глубине 7-8 см, она должна быть около 4 см (задняя медиастинотомия). Справа от нее фиброзные волокна, отграничивающие стенку НПВ, а слева и сзади — стенка пищевода. Заднюю апертуру осторожно расширяют в правую сторону до средостенной плевры, увеличивая ее размер до 6-8 см. По мере углубления доступа, при необходимости, наружную рану постепенно разводят ранорасширителем до 15 см. Переднебоковые стенки пищевода мобилизуют на 5 см вверх от КПОД, не повреждая адвентиции и блуждающих нервов. Заднюю стенку пищевода не мобилизуют. В этом нет необходимости. Сердечным зеркалом снизу вверх придерживают сердце. Диафрагму отводят книзу стальной лопаткой, прикрепленной к нижней бранше ранорасширителя. Узким длинным зеркалом отводят и защищают от ранения иглой листки средостенной плевры и НПВ.
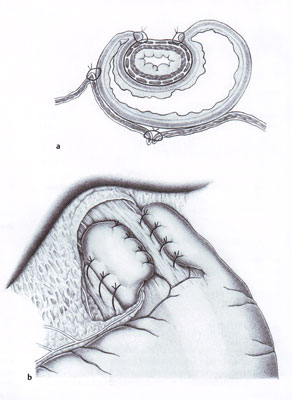
На мембранозную часть диафрагмы на расстоянии 1,0 см от переднего края КПОД и на 1,0 см в стороны от осевой линии пищевода, условно продленной на диафрагму, накладывают 2-е прошивных капроновых держалки 5 и берут их на зажимы. При их подтягивании КПОД смещается кпереди, а диафрагма образует поперечную складку. Между держалками ее рассекают на 0,5 см. Через отверстие вводят сомкнутые бранши диссектора и, прижимая их снизу к диафрагме, оттесняют абдоминальный отдел пищевода кзади. Держалками осуществляют встречную тягу. При этом брюшинный и фасциальный листок диафрагмально-пищеводной связки растягиваются. Изогнутыми ножницами, строго по переднему краю КПОД, связку рассекают и расширяют разрез по 1,5 см в обе стороны. Боковые отделы связки сохраняют и усиливают отдельными серозно-мышечными швами через стенку пищевода и КПОД, если они выглядят слабыми. Диссектор убирают. Отверстие в диафрагме ушивают. Переднюю стенку желудка вытягивают в средостение и на расстоянии 5 см от пищевода фиксируют П-образным швом к КПОД по осевой линии. В обе стороны от этого шва ее сшивают с краями КПОД без складок, провисания и натяжения (фиг. 2 а), (фиг. 2 б). Складку передней стенки желудка, образованную кзади от фиксирующих швов, погружают в виде дубликатуры под переходную зону пищевода (фиг. 3). Кромку диафрагмально-пищеводной связки с захватом серозно-мышечного слоя пищевода сшивают с КПОД.
Фиксированная к КПОД часть дубликатуры снизу наполовину перекрывает кардию. Не фиксированная задняя часть перекрывает вторую ее половину, губовидным краем герметично прилегая к задней стенке субкардиального отдела желудка (фиг. 4).
Сформированный таким образом клапан порциально пропускает пищу в желудок и препятствует ЖПР. Об этом свидетельствуют исчезновение симптомов ЖПР и РЭ, данные эндоскопического и рентгенконтрастного исследования пищевода и желудка у пациентов, перенесших эту операцию. На фиг. 5, 6 и 7 представлены ксерокопии контактных фотографий рентгенограмм больной К., 40 лет, на 13 сутки после антирефлюксной операции, выполненной 18.02.99 г. по выше описанной методике по поводу недостаточности нормально расположенной кардии, эрозивно-язвенного эзофагита с 3-х летним анамнезом. История болезни 608. Дата поступления больной в стационар 15.03.99 г. Дата выписки из стационара по выздоровлению 05.03.99 г.
На фиг. 5 зафиксирован момент прохождения контрастной массы через пищевод и зону антирефлюксного клапана, на фиг. 6 — завершающая фаза прохождения контрастной массы в желудок и возвращение клапана к задней стенке кардии. На фиг. 7 зафиксировано положение антирефлюксного клапана во время проведения пробы Вальсальвы в положении Тренделенбурга. ЖПР нет.
Переднее и заднее средостение, соединенные в процессе выполнения операционного доступа, дренируют силиконовым трубчатым дренажом с боковыми отверстиями. Наружу дренаж выводят через прокол в левом подреберье у внутреннего края левой прямой мышцы живота. В переднем средостении ближайшее боковое отверстие дренажа устанавливают на расстоянии 1,5 см от реберной дуги.
Дренаж подключают к подводному клапану с активной вакуумирующей системой.
Операционную рану ушивают послойно наглухо.
Дренаж из средостения удаляют на вторые сутки, после контрольной рентгенографии грудной клетки.
Всего таких операций выполнено 4. Результаты обнадеживающие.
Преимущества нашего способа в том, что его выполняют из малотравматичного доступа, без вторжения в плевральную и брюшную полости, а формирование антирефлюксного клапана не требует мобилизации дна желудка, перевязки и пересечения его коротких артерий. Хороший обзор пищевода с трех сторон снижает возможность случайного повреждения блуждающих нервов. Удобная и надежная фиксация кардии и пищевода к КПОД без натяжения тканей сводит к минимуму вероятность рецидива ЖПР. Не отмечали случаев послеоперационной дисфагии.
Операцию и послеоперационное ведение больных осуществляют без транснозального желудочного зонда. Длительного пареза желудка после операции не возникает. Через сутки больные начинают ходить. Еще через сутки им разрешают пить бульон и кефир. На 3-и сутки они получают желудочный стол, на 5-е — общий.
При скоплении избыточных газов в желудке или во время рвоты клапан не создает сверхнормального препятствия опорожнению желудка через пищевод. В таких ситуациях задняя стенка субкардиального отдела желудка отходит кзади, а клапан кпереди и кверху за счет эластичности, открывая выход содержимому желудка в пищевод.
СПИСОК ЛИТЕРАТУРЫ 1. Петровский Б. В. , Каншин Н.Н., Николаев Н.О. «Хирургия диафрагмы», Медицина. Л. отд., 1966, с. 175.
2. Micaleff A. , Richard-Berthe С., Huyghe J.L. «Esophgite de reflux. Resultats d une enquete epidemiologique chez 679 patients, realisee par 146 gastro — enteroloques de ville «. Med. Chir. Digest., 1986,15, 8-14.
3. Шалимов А.А., Саенко В.Ф., Шалимов С.А. «Хирургия пищевода». М. Медицина, 1975, с. 116, с. 109.
4. Allison P.R. «Reflux esophagitis, sliding hiatal hernia, and anatomy of repair» Surg. Ginec. Obstet., 1951, 92, 419.
5. Harrington S. W. «Variosus types of diaphragmatic hernia treated surgically. Report of 43 cases.» Surg. Geniс. Obstet. 1948, 86, 735.
6. Niyboer J.H., Anne Т., Derom F. «De behandeling van gastroesofageale reflux biy middel van de Kaunitz technick.» Acta chir. beig., 1985, 85, 4, 211-216.
7. Ghilardi G. , Bortolanti E., Biasi G. «Le represtino del meccanismo antireflusso gastroesofageo antraverso la tecnica di Dor». Minerva chir., 1987, 42, 9, 781-784.
8. Оскретков В.И., Ганков В.А. «Результаты хирургической коррекции недостаточности кардии». Хирургия, 1997, 8, 43-46.
9. Nissen R. , Rossetti M. «La fundoplicatio et gastropexie dans le treitement chirurgical 1 insuflisance du cardia et de la hemie. Indications, technique et resultats» Ann. Chir. 1962, 16, 11-12, 825-836.
10. Шалимов А. А., Полупан В.Н. «Атлас операций на пищеводе, желудке и двенадцатиперстной кишке». Москва — Медицина, 1975, с. 44, рис. 68-71.
11. Уткин В.В., Амбалов Г.А., Демченко Ю.М. «Опасности и осложнения фундопликации по Ниссену». Хирургия, 1986, 3, с. 88-91.
12. Teimoyinnis Е. C., Lekras E.T., Berekos K., Tsianos E.V. «Modified Nissen fundopliction in the treatment of gastroesophageal reflux disease.» Int. Surg. -1993, -vol. 78, 2, — P. 112-116.
13. Галимов О.В., Сахаутдинов В.Г., Сендерович Е.И., Федоров С.В. «К методике фундопликации при хирургическом лечении рефлюксэзофагита». Вестн. хир., 1997, Т.-156, 3, с. 47-48.
14. Gossot D., Sarfati E., Azoulay D., Celerier M. «Facteurs de morbidite de J.interantition de Nissen.» G. Chir (Paris), 1987, 124, 6-7, 367-371.
15. О. Hanrahan Т., Marples M., Bencewicz J. «Recurrent reflux and wrap disruption after Nissen fundoplication: Detection incidence and timing». G. Surg.- 1990 — vol. 77, N 5 — P. 545-547.
16. Bernat M. «Wlasni sposob chirurgucznego leczenia prepukein rozworu prcelykowego przepony i nidomogi ukladu zaporowego wpustu». Pol. Przegl., 1968, 58, N 2, 142-148.
17. Воронов А. А. , Азаров П.И. «Диагностика и лечение недостаточности кардии». Хирургия, 1987, — 6, — 85-88.
18. Ferraris V. A., Sube J. «Retrospective study of the surgical management of reflux esophagitis» Surg. Ginec. Obstet, 1981, 152, 1, 17-21.
19. Nadjafi A. «Eine einfache technische Modifikation zur Behandlung der Hiatushernie» Helv. Chir. Acta, 1971, 38, 4, 395-402.
Формула изобретения
Способ хирургической коррекции клапанной недостаточности кардии, заключающийся в обнажении заднего средостения передним внеплевральным доступом, рассечении связки, выведении в средостение 5 см передней стенки желудка, фиксации к передней и боковым дугам кольца пищеводного отверстия диафрагмы на протяжении 1,5 см с каждой стороны, погружении ее под переходную зону пищевода в виде дубликатуры и сшивании связки.
РИСУНКИ
Рисунок 1, Рисунок 2, Рисунок 3, Рисунок 4, Рисунок 5, Рисунок 6, Рисунок 7, Рисунок 8, Рисунок 9, Рисунок 10



