Адъювантная химиотерапия рака желудка

Химиотерапия часто применяется при лечении рака желудка. Метод заключается во вводе в организм специальных противоопухолевых медицинских препаратов, способных остановить разрастание онкологического процесса. Назначают химиотерапию при онкологии и в других участках тела. Врачи считают способ эффективным для остановки роста опухоли и уменьшения метастазного разрастания. Химиотерапия в лечении онкологического процесса применяется совместно с облучением гамма-лучами и оперативным вмешательством. Применяется ряд видов и схем применения лекарственных препаратов. Из-за агрессивного воздействия средств на организм у химиотерапии есть противопоказания, часто проявляются побочные эффекты.
Показания для химиотерапии в лечении рака желудка
Рак желудка в первые 3 стадии лечится при помощи хирургического способа. 4 стадия считается неоперабельной. Здесь применяется химиотерапия, чтобы продлить жизнь пациенту на несколько лет и купировать неприятные симптомы.
После операции химиотерапия требуется для предотвращения рецидива, т.к. онкологический процесс в тканях желудка отличается стремительным и агрессивным разрастанием. С метастазами злокачественные клетки проникают в отдалённые участки тела, что может спровоцировать повторное появление опухоли в других органах. Химиотерапия предотвращает проникание онкологии через кровоток.
Известны случаи, когда курсы химиотерапии могут назначаться до операции. Противоопухолевые лекарства приостанавливают злокачественный процесс, предотвращается распространение метастазов, операция проходит без тяжёлых последствий, снижается риск рецидива.
Показания для применения данного метода:
- Пациенту отказано в проведении операции по удалению злокачественного новообразования из-за обширного метастазирования.
- Для операции требуется уменьшить объём опухоли.
- В целях профилактики после удаления онкологического образования, чтобы предотвратить рецидив болезни.
Курсы и дозировку онколог подбирает индивидуально. Делают химиотерапию в условиях стационара, в домашних условиях либо амбулаторно. Зависит выбор от перечня факторов:
- общее самочувствие больного;
- присутствует индивидуальная непереносимость применяемых лекарств;
- способ проведения ввода противораковых препаратов.
Есть показания, когда использовать противоопухолевые средства не стоит, но врач настаивает, поясняя, что метод не принесёт сильного вреда. Такими случаями считаются следующие:
- больной лечился антибактериальными средствами;
- проходило лечение эпилепсии;
- человек болен СПИДом;
- имеется хроническое заболевание – ревматоидный артрит;
- детям до 6 лет курсы назначают с осторожностью;
- пациентам после 65 лет проведение процедуры рекомендуется в случае крайней необходимости.
Противопоказания к применению метода
У химиотерапии есть ряд противопоказаний, когда использовать её опасно для человека. В этих случаях врач может отказаться от применения данного метода и остановиться на хирургическом методе и облучении.
Химиотерапия при раке желудка запрещена в следующих случаях:
- присутствуют патологии в почках и печени хронического характера;
- онкология диагностирована неинвазивного типа;
- у больного есть тяжёлые заболевания инфекционного характера;
- отсутствует положительный эффект от процедуры;
- присутствует закупорка в желчных протоках;
- у пациента диагностировано тяжёлое состояние;
- нервные расстройства;
- при беременности процедура не рекомендована до момента родов;
- нахождение опухоли во внутренних слоях органа.
При наличии подобных факторов врач подбирает другие варианты лечения. Введение противоопухолевых препаратов способно проявить неприятные последствия.
Особенности воздействия химии на организм при всех стадиях рака желудка
Курс противораковыми лекарствами может назначаться перед проведением операции, совместно с оперативным вмешательством либо после резекции в виде профилактики. На начальных 3 стадиях онкологию помогает вылечить приём комплекса лекарственных препаратов, останавливающих рост злокачественных клеток. Эффективность способа зависит от скорости проникания медикаментов по организму. Больному прописываются соответствующие препараты в виде таблеток либо инъекций.
На 3 и 4 стадии болезни применение химии учащается. Используется системный способ введения цитостатиков либо в брюшную полость через надрез. Онкология на 3 стадии лечится куративной или излечивающей химиотерапией. Курс проводится, если сохраняется возможность провести оперативное вмешательство. На последней стадии патологии используется паллиативный метод как основной. На этом этапе опухоль не реагирует на хирургический способ лечения и радиоактивное облучение, остановить рост возможно лишь при помощи средств из группы цитостатиков.
Эффективность метода в лечении патологии
Положительный эффект от химии можно получить при совместном применении с операцией по удалению злокачественного новообразования. Полностью вылечить рак желудка можно только при помощи полной или частичной резекции патологического узла. Большое влияние оказывает степень поражения организма злокачественными метастазами. При распространении опасного процесса на небольшой участок повышается шанс на полное излечение. Органы с метастазными ростками удаляются совместно с опухолью.
На 2 и 3 стадии патологии возможно продлить жизнь больному до 5 лет и дольше. В случае глубокого поражения организма цитостатики помогают продлить срок жизни пациента на несколько лет. Указанный метод на 4 стадии особенно востребован, чтобы позволить человеку прожить ещё 3 – 5 лет.
Разновидности химиотерапии
Сейчас разработано несколько разновидностей введения препарата в организм. Выделяются виды:
- Самостоятельный метод используется редко из-за сложности воздействия на ткани желудка лекарств. Применяют при серьёзных противопоказаниях к оперативному удалению. При распространении метастазов лекарства помогут остановить распространение злокачественных клеток по организму и купировать неприятные симптомы. Данный вид позволяет продлить жизнь больного и улучшить качество последних дней. Вылечить болезнь полностью не удастся.
- Адъювантная химиотерапия применяется после проведения резекции опасного новообразования. Оставшиеся патогены уничтожаются под воздействием препаратов – это помогает предотвратить рецидив. Сложность в проведении курса заключается в побочных эффектах, которые организму тяжело перенести после полной резекции опухоли. Возможно развитие опасных для жизни последствий. В этом случае решение принимает лечащий врач на основании медицинских показателей и физическом самочувствии больного.
- Неоадъювантный вид заключается во вводе лекарств в организм до операции – это увеличивает шанс больного на положительный результат оперативного вмешательства. Новообразование уменьшается в размерах и распространение метастазов останавливается, что увеличивает шансы пациента на выздоровление.
- Паллиативная химиотерапия применятся на последней стадии заболевания, когда метастазы проникли в большую часть тела. Лекарства позволяют купировать неприятные признаки и продлить срок жизни пациенту до 3-5 лет. Препарат вводят при помощи капельницы. Курс проходит совместно с радиоактивным облучением. После этого проводят процедуру резекции части больного органа. Вторая часть соединяется с кишечником. Медикаменты используются с сильным наркотическим действием.
- Внутрибрюшинный вид используется достаточно редко. Применяют при наличии жидкости и раковых клеток в брюшной полости. Постороннюю жидкость откачивают и вводят химпрепараты через катетер. Дополнительно назначаются для приёма внутрь лекарства противорвотного действия.
Виды лекарств, применяемые в химиотерапии
Противоопухолевые средства относятся к высокотоксичным лекарствам. Чаще всего используют Доцетаксел, 5-фторурацил, Митомицин, Лейковорин, Эпирубицин и Цисплатин. Курс длится 5 дней. При лечении болезни Ходжкина используют Винкристин, Преднизолон, Эмбихин и Кармазин.
Медикаменты делятся на следующие группы:
- Метаболиты состоят из фторпиримидинов. Препараты останавливают рост злокачественного образования, снижают распространённость по телу и уничтожают часть патогенов. Сюда относят 5-фторурацил, Гемцитабин, Кселоду и Фторафур.
- Антибиотики требуются для предотвращения воспаления внутри организма или чтобы остановить присутствующий процесс. Действующее вещество таких медикаментов – Нитрозомочевина. К данному типу относят Эпирубицин, Доксорубицин и Митомицин.
- Топоизомеразы являются активными противоопухолевыми препаратами. Чаще всего применяют UFI.
Схемы ввода лекарств при раке желудка
Любая схема имеет специальное название, помогающее медперсоналу определить курс приёма медикаментов. Выделяют перечисленные варианты приёма:
- МЕР используется у молодых людей с хорошей защитной функцией организма. Не допускается наличие внутренних кровотечений и индивидуальной непереносимости на вводимые вещества. Курсы чередуются каждый месяц. В 1 и 7 день вводят Митомицин. В 5 и 6 день – Этопозид и на 2 с 8 днем – Цисплатин.
- ELF подходит для людей после 55 лет. Лекарства вводят 1 раз каждые 27 дней. Внутривенно пациенту вводят Этопозид, Лейковорин и 5-фторурацил первые 3 дня. Это помогает снять высокую нагрузку с ослабленного организма.
- ТС относится к предельно эффективным, но отличается тяжёлыми побочными проявлениями. Поэтому применяют редко. Однократное введение повторяют через 21 день. Внутривенно вводятся Доцетаксел с Цисплатином по 75 мг каждый.
- TCF характеризуется более тяжёлым воздействием на опухоль и организм больного. По схеме приёма схожа со схемой ТС, дополнительно применяют 5-фторурацил (вводят ежедневно в течение 5 дней по 750 мл).
- ECF используется часто из-за отсутствия тяжёлых последствий и лёгкой переносимости пациентами. Применяют Эпирубицин, Цисплатин однократно. Затем только через 21 день. 5-фторурацил используют ежедневно на протяжении 20 недель.
- FLOT (флот) характеризуется приёмом Доцетаксела с Оксалиплатином, Лейковорин, 5-фторурацил. Курс повторяется каждые 14 дней.
В каждом случае врач индивидуально подбирает схему и вид лекарств для лечения опасного заболевания. Препараты используются в таблетках, внутривенно либо в виде суспензии.
Подготовка к процедуре
Для ввода сильнотоксичных средств требуется тщательно подготовить организм – это позволит снизить проявление побочных эффектов и повысить положительный результат курса.
За месяц до процедуры больному рекомендована специальная диета. Режим требуется для снижения побочных явлений со стороны желудочно-кишечного тракта. Также правильно подобранное питание снимет лишнюю нагрузку с органов пищеварения. Рацион составлен из большого количества белка с витаминами и микроэлементами. Кушать нужно часто и маленькими порциями. Разрешается однократно принять до 150 г пищи.
Рекомендуется полностью исключить жирные блюда, острые приправы, солёные и маринованные продукты, а также копчёности. Употреблять стоит пищу тёплую – холодная и горячая раздражает слизистую желудка, что негативно сказывается на самочувствии пациента.
Для химиотерапии требуется предварительный приём инфузионных препаратов и гепатопротекторов, эффективно влияющих на метаболические процессы внутри организма.
Проявление побочных эффектов после процедуры
После химиотерапии страдает защитная функция организма, что проявляется соответствующими симптомами. Некоторые признаки удаётся купировать приёмом медикаментов. Известны проявления, которые невозможно снять таблетками, рекомендуется ждать.
Частые побочные проявления:
- Выпадение волос в больших объёмах.
- В ротовой полости развиваются тяжёлые воспаления – стоматиты.
- Снижается или полностью отсутствует аппетит.
- Пациента постоянно мучают приступы тошноты.
- В некоторых случаях могут присутствовать рвотные позывы.
- Ослабевает костная ткань, что приводит к образованию остеопороза.
- Часто диагностируются различные заболевания сердечно-сосудистой системы.
- Может развиться лейкемия из-за нарушенного кровяного состава.
- Слёзные железы работают в усиленном режиме, что приводит к повышенному слезотечению.
- Снижается слуховая функция ушной раковины.
- На поверхности кожи появляются посторонние высыпания.
- Верхние и нижние конечности периодически немеют или ощущается покалывание.
- Снижается масса тела.
- Возможно заражение крови.
- Стремительно развивается нейтропения из-за отсутствия необходимых кровяных телец в костном мозге.
- Появляются проблемы с глотанием, может наступить спазм глотки.
- Формирование внутренних или внешних кровотечений.
Проявление неприятных симптомов индивидуально. Влияет физическое состояние пациента и правильно проведённая подготовительная процедура.
Возможные осложнения метода
Как и любой метод воздействия на организм при помощи высокотоксичных лекарственных препаратов химиотерапия обнаруживает ряд осложнений, негативно влияющих на здоровье человека. Погибают не только злокачественные патогены, страдают и здоровые клетки тела.
Чаще всего диагностируют следующие осложнения после приёма препаратов из группы цитостатиков:
- вторичное метастазирование с формированием новых онкологических очагов в других участках тела;
- у людей в зрелом возрасте резко снижается половая активность;
- внутренние кровотечения, связанные с неполной резекцией злокачественного новообразования и образованием рецидива патологии;
- полное отсутствие аппетита, требующее дополнительного лечения;
- острая реакция кишечного отдела на лекарства в виде тяжёлой диареи;
- развитие миелосупрессии – снижение уровня основных элементов в составе крови (лейкоцитов с тромбоцитами и эритроцитами);
- формируются опасные заболевания крови – тромбоцитопения или анемия;
- луковицы волос меняют структуру, что проявляется выпадением старого покрова и заменой на новый с другим цветом и структурой;
- качественно меняется состав крови, что характеризуется сильным переутомлением, частой усталостью после небольших нагрузок и кровоизлияниями верхние слои кожи;
- страдают слизистые желудка, что проявляется соответствующими расстройствами в переваривании пищи и метаболических процессах.
Во время проведения курсов химиотерапии требуется регулярно сдавать кровь в лаборатории на контроль основных элементов. В основном это проводится каждые 3 недели.
При появлении рвотных масс с примесью крови либо коричневого оттенка выделяемых масс курс приёма цитостатиков приостанавливается. Также следует поступить при наличии таких признаков в каловых выделениях. Здесь требуется применение симптоматической терапии с переливанием крови. При выявлении распада опухоли после кровотечения желудок вырезается полностью.
При резком снижении массы тела процедура также останавливается до момента набора нужного веса, чтобы продолжить лечение. Расхождение веса в 10% считается опасным для жизни человека.
Питание при лечении противоопухолевыми средствами
Восстановление желудка после рака и химиотерапии идёт быстрее при правильно подобранном и сбалансированном питании. Приём продуктов, содержащих витамины и микроэлементы, восполняет дефицит полезных веществ.
Потребуется исключить из рациона животные жиры – сметану, молоко и кисломолочные продукты, яйца, мясо, рыбу и т.п. Сахар и соль использовать редко, по необходимости. Копчёности и маринованные блюда полностью убрать. Запрещено употреблять соленые, консервированные салаты и другие заготовки – это раздражает слизистую желудка, что негативно влияет на процесс лечения. Не стоит готовить блюда при помощи жарки, даже на гриле. Сладкую выпечку, сдобу, пирожные и торты, пирожки не стоит употреблять.
Организму требуется большое количество растительной клетчатки, стоит увеличить потребление таких продуктов. Врачи советуют обогатить готовые блюда оливковым или льняным маслом. Брать лучше холодного отжима. Рекомендуется обогатить питание кашами из цельного зерна на воде. Хлеб разрешается с отрубями, приготовленный без использования дрожжей. Овощи и фрукты нужно кушать ежедневно в сыром виде и в большом количестве. Все готовые блюда подавать к столу с зеленью в достаточном объёме.
Готовить рекомендуется пищу на пару, варить, тушить без острых приправ и запекать в духовке. Количество употреблений нужно увеличить до 5-6 раз. Порции не должны превышать 150 г – это снизит отдачу необходимой энергии организмом.
Диета заключается в приёме следующих продуктов:
- Мясо нужно заменить на бобовые продукты – это богатый источник белка, который не требует высоких затрат организма на переваривание и усвоение.
- Рыбу можно принимать редко и заменить на морскую нежирных сортов.
- Продукты из молока должны быть обезжиренными.
- Пригоревшую пищу употреблять нельзя.
- Кофе, сладкие газировки и алкогольные напитки запрещены.
- На время химиотерапии и восстановления можно пить простую воду без газа.
- Массу тела нужно контролировать каждый день.
Восстановление слизистой после процедуры
Препараты из группы цитостатиков обладают высокотоксичным действием, поэтому оказывают на организм угнетающее действие. После курсов химии требуется индивидуальная программа восстановления пострадавшего органа. Здесь подбирается специальная диета, очищение лекарственными травами, ароматерапия, лечебное плавание и т.п.
Купировать осложнения, связанные с расстройством слизистой органов желудочно-кишечного тракта, можно при помощи отваров из лечебных трав. Остановить рвотные позывы можно полынью, горечавкой и др. Расстройство стула лечится: понос настойками из бадана, калгана и сабельника болотного; запор – сенной, укропом, фенхелем, крушиной и анисом.
Курс восстановления заключается в следующих мероприятиях:
- Снять признаки общей интоксикации можно употреблением большого количества жидкости – отвар из ягод шиповника, рябины, ягодные морсы из брусники и клюквы.
- Назначаются мочегонные травы – корень пырея и хвощ полевой.
- Вывести токсины помогут Полифепан, Активированный уголь, Зостерин, из трав можно взять – дягиль, семечки льна, алтей.
- Приготовить отвар из багульника болотного, чабреца ползучего и цетрарииисландской.
Правильно проведённая процедура с набором эффективных препаратов поможет вылечить рак желудка без появления опасных побочных эффектов и осложнений.
Выберите город, желаемую дату, нажмите кнопку «найти» и запишитесь на приём без очереди:
Новости онкологии
18.10.2012
С.А. Тюляндин
Российский онкологический научный центр им. Н.Н. Блохина РАМН
Несмотря на то, что до настоящего времени хирургическое лечение остается главным методом лечения ранних стадий рака желудка, становится все более очевидным, что в большинстве случаев он представляет собой системное заболевание. Системность подтверждается неудовлетворительными результатами хирургического лечения больных I-III стадиями. Более чем у 50% из них после радикальной операции в последующем отмечается прогрессирование заболевания в основном за счет развития отдаленных метастазов.
Примерно у 30% больных раком желудка I-II стадий определяются циркулирующие опухолевые клетки в периферической крови и/или микрометастазы в костном мозге, наличие которых значимо увеличивает шанс развития отдаленных метастазов после операции. Все это делает обоснованным желание использовать системную терапию, в частности, химиотерапию, на предоперацинном или послеоперационном этапе у больных операбельным раком желудка для улучшения отдаленных результатов лечения.
Для оценки эффективности адъювантной терапии рака желудка в конце 1990-х – начале 2000-х годов было проведено несколько рандомизированных исследований, однако немногочисленность больных, включенных в эти исследования, и противоречивость их результатов не позволили сделать однозначного заключения о клинической целесообразности подобного подхода. Вместе с тем, проведенный мета-анализ этих исследований все же свидетельствовал о том, что проведение адъювантной терапии с включением фторпиримидинов может увеличивать 5-летнюю общую выживаемость на 4,8% (с 49,5% в группе хирургического лечения до 55,3% в группе комбинированного лечения, HR=0,82, р<0,001) [1].
Однако адъювантная терапия до сегодняшнего дня не является стандартным подходом в лечении больных раком желудка. И для этого есть несколько причин. Основной причиной является отсутствие эффективных препаратов и комбинаций для лечения рака желудка. Сегодня ни одна из используемых комбинаций для лечения метастатического рака желудка не позволяет достигнуть медианы продолжительности жизни ≥12 месяцев, что ставит под сомнение эффективность этих же комбинаций при использовании их в адъювантом режиме (с целью увеличения шанса на излечение).
Следствием этого является отсутствие единого мнения о стандарте проведения первой линии химиотерапии. В некоторых странах это комбинация цисплатина и капецитабина или инфузий 5-фторурацила, другие используют режим ЕСF (эпидоксорубицин, цисплатин, капецитабин) или ECF (эпидоксорубицин, цисплатин, капецитабин). Остается популярным назначение комбинации TCF (доцетаксел, цисплатин, 5-фторурацил). Все большую популярность завоевывает режим CAPOX (капецитабин+оксалиплатин).
Другая важная причина непопулярности адъювантной терапии – плохое общее состояние больных после перенесенной гастрэктомии, часто или всегда сопровождаемой лимфодиссекцией в разных объемах. На момент начала терапии большинство подобных больных имеют серьезный дефицит веса, который продолжает нарастать после операции в связи с нарушениями всасывания и развитием у части больных демпинг-синдрома. Проведение химиотерапии на этом фоне сопровождается частым развитием тяжелых осложнений, требующих снижения доз препаратов, увеличения интервалов или отказом от дальнейшего лечения. Все это приводит к потере потенциальной пользы от проведения адъювантной терапии больных раком желудка.
Однако результаты последних исследований заставляют по-новому оценить возможности адъювантной химиотерапии рака желудка. В исследовании японских авторов больным раком желудка II-III стадий выполняли гастрэктомию с лимфодиссекцией D2 с или без добавления в послеоперационном периоде препарата S-1 (комбинированный препарат, состоящий из фторафура и ингибиторов фермента дигидропиримидиндегидрогеназы, разрушающего фторпиримидины) в течение года [2]. В исследование было включено 1059 больных, и на сегодняшний день известны результаты 5-летнего наблюдения.
Общая 5-летняя выживаемость в группе, получившей только хирургическое лечение, составила 61,1%, а в группе адъювантной терапии – 71,7% (снижение относительного риска смерти на 33%, HR=0,67, р<0,05), 5-летняя безрецидивная выживаемость составила 53,1% и 65,4% соответственно (снижение относительного риска прогрессирования заболевания на 35%, HR=0,65, р<0,05). Лечение S-1 переносилось хорошо, основным проявлением токсичности было снижение аппетита. Нежелательные явления 3-4 степени выраженности наблюдалась лишь у 5% больных.
Закончили 12-месячный прием препарата 66% больных, из них у половины потребовалось снижения дозы. Подгрупповой анализ показал, что улучшение результатов лечения при назначение адъювантной терапии наблюдалось вне зависимости от стадии заболевания, морфологии опухоли, возраста и пола больных. На основании этих данных авторы сделали вывод о том, что годичная адъювантная терапия пероральным фторпиримидином S-1 улучшает результаты лечения больных раком желудка II-III стадии, подвергнутых гастрэктомии с лимфодиссекцией D2.
![Общая (А) и безрецидивная (B) выживаемость больных раком желудка после радикального хирургического лечения с или без адъювантной терапии S-1 [1]](https://rosoncoweb.ru/news/oncology/2012/10/18/image001.png)
Рисунок 1. Общая (А) и безрецидивная (B) выживаемость больных раком желудка
после радикального хирургического лечения с или без адъювантной терапии S-1 [1].
Другое исследование (CLASSIC) было также выполнено в странах Азии (Китай, Корея, Тайвань) у больных раком желудка после гастрэктомии и лимфодиссекции D2 [3]. В этом исследовании, в которое было включено 1035 больных, в качестве адъювантной терапии использовали комбинацию CAPOX (оксалиплатин в дозе 130 мг/м2 1 день и капецитабин в дозе 1000 мг/м2 внутрь 2 раза в день 1-14 дни, каждые 3 недели 8 курсов лечения). При среднем сроке наблюдения 34 месяца 3-летняя безрецидивная выживаемость составила 59% в группе только хирургического лечения и 74% в группе адъювантной терапии (снижение относительного риска прогрессирования на 44%, HR=0,56, р<0,0001).
Назначение химиотерапии сопровождалось развитием нежелательных явлений 3-4 степени у 56% больных (наиболее часто наблюдали нейтропению (22%), тромбоцитопению (8%), тошноту (8%) и рвоту (8%), слабость). Частота развития сенсорной нейропатии 1-2 степени составила 10%, и лишь у 3 больных это осложнение достигло 3 степени выраженности. Все 8 курсов терапии получили 67% больных, однако почти все они потребовали снижения дозы. Токсичность была причиной прекращения терапии у 10% больных.
Подгрупповой анализ показал, что польза от проведения адъювантной терапии отмечена у больных N1-2, мужчин и не зависела от стадии заболевания и возраста. Авторы данного исследования также сделали вывод о том, что проведение адъювантной терапии после гастрэктомии с лимфодиссекцией D2 уменьшает риск прогрессирования заболевания у больных раком желудка.
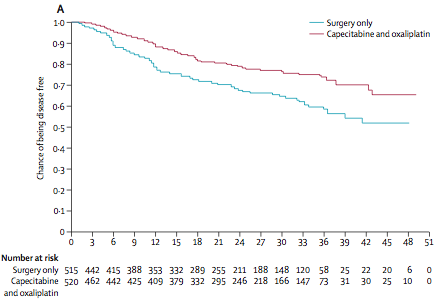
Рисунок 2. Безрецидивная выживаемость больных раком желудка
после хирургического лечения с или без проведения адъювантной терапии комбинацией CAPOX [2].
Картина адъювантых методов лечения рака желудка будет неполной без упоминания химиолучевой терапии. Американские коллеги в исследовании SWOG-0116 показали, что введение 5-фторурацила и лейковорина до, в процессе и после лучевой терапии на верхний этаж брюшной полости СОД 45 Гр улучшает показатели общей и безрецидивной выживаемости больных раком желудка Т3-4 и N+ после гастрэктомии и лимфодиссекции D0-1 [4].
Данная методика стала стандартной в США, где гастрэктомия зачастую не сопровождается расширенной лимфодиссекцией. Большинство комментаторов пришло к заключению, что проведение лучевой терапии в данном случае компенсирует недостаточный объем оперативного вмешательства. В другом, уже корейском исследовании (ARTIST) была предпринята попытка оценить целесообразность добавления лучевой терапии к адъювантной химиотерапии CAPOX у больных раком желудка после гастрэктомии и лимфодиссекции D2 [5].
Добавление лучевой терапии не улучшило результаты адъювантного лечения, хотя в группе больных с метастазами в регионарные лимфоузлы и была отмечена тенденция к улучшению безрецидивной выживаемости. Была предпринята попытка улучшения результатов химиолучевой терапии за счет замены 5-фторурацила и лейковорина на режим ECF [8]. Предварительный анализ показал отсутствие преимуществ при использовании более интенсивной химиотерапии.
В России проведение химиолучевой терапии при раке желудка в целом (включая местно-распространенные, неоперабельные опухоли) и в качестве адъювантной терапии в частности не пользуется популярностью. Во всяком случае, в моей практике не было ни одного больного, получившего данное лечение в нашей стране. Методика облучения верхнего этажа брюшной полости трудоемка, требует современных ускорителей и тщательного дозиметрического планирования.
Поэтому я не берусь обсуждать перспективы химиолучевого лечения при раке желудка в нашей повседневной практике. Тем более, что в России отмечается тенденция к увеличению числа больных, у которых гастрэктомия сопровождается лимфодиссекцией D2, после которой проведение химиолучевой терапии не доказало своего преимущества.
Еще одним подходом, исследовавшимся при операбельном раке желудка, является проведение лекарсственного лечения до и после операции. Cunnignam et al. оценивали эффективность добавления к операции 3 курсов лечения в режиме ECF предоперационно и 3 курсов адъювантно [7]. Потенциальными преимуществами предоперационной системной терапии являлось ожидаемое увеличение частоты R0 резекции вследствие уменьшения размеров опухоли, элиминация микрометастазов, уменьшение выраженности симптомов, обусловленных опухолевым процессом, и оценка чувствительности опухоли к проводимой химиотерапии.
Комбинация ECF предусматривала введение каждые 3 недели эпидоксорубицина в дозе 50 мг/м2 и цисплатина 60 мг/м2 и постоянную инфузию 5-фторурацила в суточной дозе 200 мг/м2 в течение 21 дня. В исследование были включены 503 больных с резектабельной аденокарциномой желудка и нижних отделов пищевода, рандомизированно распределявшиеся на проведение радикальной операции с или без дополнительного лекарственного лечения.
Больные, получившие предоперационную химиотерапию, продемонстрировали хорошую переносимость, меньшую опухолевую распространенность и одинаковую частоту послеоперационных осложнений. Из 250 больных, рандомизированных в группу химиотерапии, 215 (86%) получили 3 курса предоперационно и 104 (42%) закончили 6 курсов химиотерапии. По сравнению с больными, которым была выполнена только операция, проведение системной терапии уменьшило относительный риск прогрессирования на 34% (HR=0,66, p<0,001) и риск смерти на 25% (HR=0,75, p=0,009), что позволило увеличить 5-летнюю выживаемость с 23% до 36%.
Выражу свое субъективное мнение, что предоперационная терапия рака желудка в ближайшее время не будет востребована в России. Это потребует изменения психологии хирургов, к которым в первую очередь попадают больные операбельным раком желудка и которые рассматривают это заболевание как чисто хирургическую проблему.
Системность рака желудка, как и всех других злокачественных опухолей, требует мультидисциплинарного подхода, обсуждения тактики лечения больного, в том числе и целесообразность выполнения операции или проведения системной терапии на первом этапе, онкологами различных специальностей сразу после постановки диагноза. Пока это не станет повседневной практикой в работе любого онкологического учреждения, предоперационная системная терапия у операбельных больных не будет популярной.
Однако уже сегодня онкологи-химиотерпевты могли бы более активно использовать в своей практике назначение адъювантной системной терапии. За последние годы получены убедительные свидетельства, что проведение адъювантной химотерапии достоверно улучшает отдаленные результаты оперативного лечения рака желудка, в том числе и подвергнутого операциям с включением лимфодиссекции D2.
Комбинация CAPOX широко используется в нашей стране для лечения колоректального рака, и большинство практикующих химиотерапевтом имеют личный опыт ее применения. С учетом 15% разницы в 3-летней безрецидивной выживаемости у нас нет оснований отказывать в проведении адъювантной химиотерапии CAPOX больным раком желудка, имеющим общее удовлетворительное состояние после гастрэктомии и лимфодиссекции D2 (как минимум при наличии метастазов в удаленных лимфоузлах).
Литература
- GASTRIC Group, Paoletti X, Oba K, Burzykowsky T, et al. Benefit of Adjuvant chemotherapy for resectable gastric cancer: a meta-analysis. JAMA 2010. 303: 1729-37.
- Sasako M, Sakuromoto S, Katai H, et al. Five-year outcomes of a randomized phase III trial comparing adjuvant chemotherapy with S-1 versus surgery alone in stage II or III gastric cancer. J. Clin. Oncol. 2011; 29: 4387-93.
- Bang Y-J, Kim Y-W, Yang H-K, et al. Adjuvant capecitabine and oxaliplatin for gastric cancer after D2 gastrectomy (CLASSIC): a phase 3 open-label, randomized controlled trial. Lancet 2012; 379: 315-21.
- Smalley SR, Benedetti JK, Haller DG, et al. Updated analysis of SWOG-directed Intergroup study 0116: A phase III trial of adjuvant radiochemotherapy versus observation after curative gastric cancer resection. J Clin Oncol. 2012. 30: 2327-2333.
- Lee J, Lim do H, Kim S, et al. Phase III trial comparing capecitabine plus cisplatin versus capecitabine plus cisplatin with concurrent capecitabine radiotherapy in completely resected gastric cancer with D2 lymph node dissection: The ARTIST trial. J Clin Oncol. 2012. 30: 268-273.
- Fuchs CS, Tepper JE, Niedzwiecki D, et al. Postoperative adjuvant chemoradiation for gastric or gastroesophageal junction (GEJ) adenocarcinoma using epirubicin, cisplatin, and infusional (CI) 5-FU (ECF) before and after CI 5-FU and radiotherapy (CRT) compared with bolus 5-FU/LV before and after CRT: Intergroup trial CALGB 80101. J Clin Oncol. 2011. 29 (suppl): 256s, abstr 4003.
- Cunningham D, Allum WH, Stenning SP, et al. Perioperative chemotherapy versus surgery alone for resectable gastroesophageal cancer. N Engl J Med. 2006. 355: 11-20.
![]()
![]()
![]()
Copyright © Российское общество клинической онкологии (RUSSCO)
Полное или частичное использование материалов возможно только с разрешения администрации портала.


