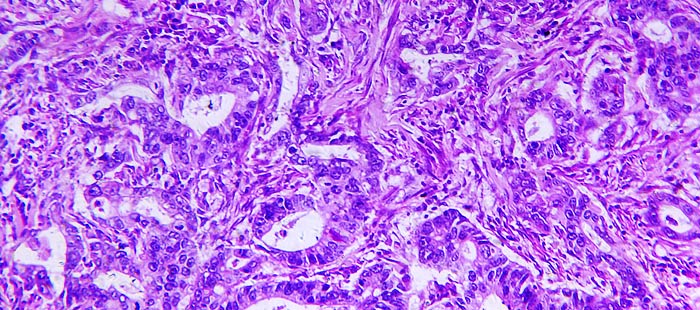
Рак желудка с некрозами

Как происходит некроз опухоли?
23-Окт-2015
Некроз опухоли – это процесс омертвления злокачественного или доброкачественного новообразования, при котором полностью прекращается обмен веществ в патологических тканях. Некротические изменения проходят четыре последовательные фазы:
- Обратимая фаза или паранекроз.
- Необратимая цитологическая стадия – некробиоз.
- Распад опухоли.
- Гибель клеточных структур опухоли.
Причины развития некроза опухоли
Формированию необратимого разрушения тканей новообразования способствуют следующие факторы:
- Механическое травмирование мутированных клеток.
- Воздействие высоких или сверхнизких температур.
- Облучение опухоли высокоактивным ионизирующим излучением.
- Химические факторы некроза.
Общее понятие фактора некроза опухоли
Фактор некроза или кахектин синтезируют т-лимфоциты и макрофаги. Это вещество вызывает геморрагический некроз определенных клеток злокачественного новообразования. До недавнего времени специалисты считали, что фактор некроза опухоли обладает токсическим действием только на онкологические ткани. Недавние исследования выявили участие кахектина также во многих физиологических и патологических реакциях человеческого организма. Действие ФНО напрямую зависит от его концентрации в кровеносной системе. Так, повышенное количество кахектина провоцирует развитие септического шока и снижает усвоение жиров, что тем самым способствует прогрессированию раковой кахексии. Недостаточное количество кахектина, в свою очередь, стимулирует концентрацию нейтрофилов в кровеносных стенках при воспалительном процессе.
Открытие фактора некроза опухоли в онкологии
Фактор некроза опухоли впервые был выделен в 1975 году в городе Кахектин, от которого, в результате, произошло второе название данного вещества. Исследования проводились на мышах, которым ввели БЦЖ и эндотоксин. В сыворотке крови этих животных ученые выявили кахектин. В ходе лабораторных анализов специалисты также установили противоопухолевую активность кровеносных клеток подопытных мышей.
Основные свойства фактора некроза
При нормальных физиологических состояниях кахектин является немаловажным медиатором воспалительного процесса и активным участником иммунной защиты организма. Дисфункция данной системы может привести к аллергическим реакциям в виде гиперчувствительности немедленного типа.
В ходе многочисленных исследований ученые выявили прямую связь между увеличением кахектина в крови подопытных животных и развитием эндоскопического шока.
Также науке известно, что фактор некроза для некоторых структурных элементов человеческих тканей является фактором роста, который стимулирует заживление ран, восстановление кровотока и формирование клеточных абсцессов.
Но все же, ключевой функцией кахектина считается его возможность вызывать некроз опухоли при раке. В современной онкологии эти способности некротического фактора нашли широкое применение. Следует отметить, что обширное омертвление мутированных клеток может быть опасным для жизни онкобольного.
Важно знать: Фактор некроза опухоли — Альфа: цена, где купить?

Некроз опухоли
Синдром острого опухолевого некроза
Синдром активного разрушения опухолевых тканей развивается после введения активных противораковых препаратов и химиотерапии. В таких случаях происходит гибель большого количества онкологических клеток и в кровеносную систему больного поступает большое количество продуктов распада и цитотоксинов. СООН может закончиться летальным исходом. Для предупреждения таких негативных последствий пациент во время терапии должен находиться под постоянным медицинским контролем для своевременного оказания неотложной помощи.
Механизм возникновения синдрома острого опухолевого некроза
Согласно статистическим данным, развитие данного синдрома преимущественно наблюдается у больных лейкозом и лимфомой. Специалисты связывают этот факт с повышенной концентрацией фосфатов в мутированных клетках кровеносной и лимфоидной системы. Предрасполагающими факторами к данной патологии также принято считать:
- Большой размер злокачественного новообразования.
- Рак крови.
- Множественные опухоли.
- Быстрый рост новообразования.
- Прорастание раковой опухоли во внутренние органы.
- Уменьшение объема циркулирующей крови.
Во время активного разрушения мутированных клеток в организм больного сбрасывается повышенное количество калия и фосфата. Именно симптомы гиперкалиемии, гиперфосфатемии и вызывают клинические проявления синдрома острого опухолевого некроза.
Некроз опухоли при онкологии: диагностика и анализы
В первую очередь, хочется отметить, что пациент получающий интенсивное противораковое лечение должен находится под постоянным контролем врачей. При обнаружении первых признаков интоксикации в виде диареи, тошноты и рвоты, ему проводятся следующие диагностические процедуры:
- Биохимический анализ крови, в котором обращается особое внимание на концентрацию ионов калия и фосфата.
- Электрокардиограмма. Увеличение концентрации калия в кровеносной системе может провоцировать брадикардию.
- Анализ мочи. Раковая интоксикация часто сопровождается повышением креатинина и ацетона в моче больного.
Методы лечения синдрома острого некроза опухоли
Неотложная медицинская помощь в таких случаях заключается в внутривенном введении раствора хлористого натрия, который нормализует уровень калия и фосфатов. Пациентам индивидуально определяется уровень необходимой жидкости, которую также вводится парэнтерально, что способствует дезинтоксикации организма. При вторичном увеличении концентрации калия показано введение препаратов на основе ионов кальция.
Некроз опухоли по современным стандартам онкологии необходимо контролировать на всех этапах противотанковой терапии, начиная от специфической диагностики и заканчивая на этапе реабилитации пациента. Профилактика такого осложнения заключается только в наиболее точном установлении размера и локализации злокачественного новообразования.
Аденокарцинома желудка — это одна из наиболее часто встречающихся разновидностей рака данной локализации. На ее долю приходится до 95% всех злокачественных новообразований желудка. Заболевание коварно тем, что на начальных стадиях никак себя не проявляет, затем возникают боли, тошнота, потеря аппетита, на фоне этих симптомов нарастает слабость и потеря веса. Единственный на сегодняшний день радикальный метод лечения аденокарциномы это хирургическая операция. Лучевая терапия и химиотерапия назначаются в качестве дополнительного лечения или при невозможности хирургического вмешательства.
Причины развития
Причина злокачественной трансформации клеток слизистой оболочки до конца не выявлены, но ученые определили несколько факторов, которые достоверно повышают такую вероятность:
- Хронический атрофический гастрит. На его фоне развивается до 60% всех случаев рака желудка. При локализации атрофического процесса в теле желудка, риск увеличивается в 3-5 раз, в антральной его части — в 18 раз, а если поражен весь желудок — в 90 раз.
- Нарушение питания — употребление большого количества острых и соленых продуктов, маринадов, копченостей, вяленого мяса, а также жиров, особенно подвергшихся термической обработке. Имеет значение характер приема пищи. Переедание, недостаточно тщательное пережевывание пищи может привести к хронической травматизации стенки желудка и на этом фоне — к злокачественному перерождению клеток.
- Инфицирование бактерией Хеликобактер пилори увеличивает риски в 3-4 раза.
- Курение и злоупотребление алкоголем.
- Наличие в анамнезе операций на желудке. Риск развития рака увеличивается в 4 раза.
- Пернициозная анемия — злокачественная анемия, связанная с невозможностью усвоения витамина В12. На этом фоне происходит снижение иммунитета, что в 10% случаев приводит к развитию рака.
- Иммунодефицитные состояния, в том числе СПИД.
- Наследственная предрасположенность по данным разных авторов увеличивает риск на 5-20%. В научной литературе описаны случаи наследования аденокарциномы желудка.
- Работа с вредными производственными факторами (никель, асбест).
- Язва желудка. При ее расположении в теле желудка, риски малигнизации увеличиваются в 2 раза, а при поражении антрального отдела данной закономерности не отмечается.

Виды аденокарциномы желудка
Согласно современной классификации выделяют следующие виды аденокарцином, поражающих желудок:
- Папиллярная — визуально напоминает полип.
- Тубулярная. Произрастает из клеток кубического или цилиндрического эпителия.
- Муцинозная. Произрастает из слизисто-продуцирующих клеток.
По степени дифференцировки выделяют следующие формы:
- Высокодифференцированная аденокарцинома желудка. Клетки опухоли имеют высокий уровень дифференцировки и «напоминают» здоровую ткань. Характеризуется медленным ростом и, при своевременной диагностике, хорошо поддается излечению. Главная проблема заключается в том, что в самом начале данную опухоль сложно обнаружить, даже при эндоскопическом обследовании, а ее выявление на поздних стадиях не позволяет достичь желаемого результата.
- Умеренно дифференцированная аденокарцинома желудка. Клетки этой опухоли сложно идентифицировать с тканью, из которой она произрастает. Характеризуется умеренной злокачественностью и скоростью роста.
- Низкодифференцированная аденокарцинома желудка. Клетки данной опухоли невозможно идентифицировать с определенной тканью. Это наиболее злокачественный тип рака желудка. Характеризуется быстрым ростом и метастазированием.
Симптомы
- Потеря аппетита.
- Явления диспепсии — вздутие живота, тошнота, отрыжка, чувство тяжести. Если опухоль имеет большие размеры, она может перекрывать просвет желудка, что вызывает рвоту при приеме пищи, но это происходит уже на последних стадиях.
- Слабость и апатия.
- Боль. Как правило, она возникает не сразу, а преимущественно на распространенных стадиях. В это время она носит постоянный характер и не зависит от приема пищи. Возникает без видимых причин и часто усиливается после еды. На последних стадиях она настолько сильная, что не купируется привычными анальгетиками.
Как мы видим, эти симптомы неспецифичны, и человек может долгое время пытаться купировать их самостоятельно.

Диагностика аденокарциномы желудка
Своевременная диагностика рака желудка имеет важнейшее значение, поскольку прогноз на ранних стадиях заболевания куда более благоприятен, чем при распространенном опухолевом процессе. Но аденокарцинома на начальных стадиях характеризуется либо бессимптомным течением, либо ее симптомы воспринимаются как признаки другого заболевания, например, гастрита, язвы, желчнокаменной болезни, панкреатита. В результате пациенты не обращаются к врачу, купируя симптомы самостоятельно с помощью препаратов, купленных в аптеке.
Стадии аденокарциномы
- 0 стадия или рак in situ. Злокачественные клетки не распространяются на пределы эпителиального слоя.
- 1 стадия. Опухоль прорастает эпителий и распространяется на другие слои стенки желудка, но не выходит за ее пределы.
- 2 стадия. Опухоль увеличивается в размерах и дает метастазы в регионарные лимфатические узлы.
- 3 стадия. Аденокарцинома прорастает в соседние органы (поджелудочная железа, печень) и/или дает метастазы в несколько групп лимфатических узлов.
- На четвертой стадии, аденокарцинома дает метастазы в отдаленно расположенные органы и лимфатические узлы.
Диагностика
Диагностика аденокарциномы желудка носит комплексный характер и включает ряд обследований, которые не только помогают определить тип опухоли, но и стадию заболевания:
- ФГДС — обследование, которое осуществляется с использованием специального прибора — гибкого эндоскопа. С его помощью производится визуальный осмотр слизистой оболочки желудка, причем прибор транслирует увеличенное изображение исследуемого участка на монитор, что позволяет обнаружить незначительные изменения слизистой. Во-вторых, эндоскоп оснащен специальной манипуляционной системой, с помощью которой можно взять кусочек ткани на гистологический анализ и точно определить вид опухоли и степень дифференцировки ее клеток.
- УЗИ. Этот метод исследования позволяет уточнить размер опухоли, ее соотношение с соседними органами, наличие метастазов в регионарные лимфатические узлы.
- КТ и МРТ также помогают верифицировать размеры злокачественного новообразования и его врастание в окружающие ткани, но главной целью является поиск метастазов в лимфоузлы и отдаленные органы (например, легкие).
- ПЭТ-КТ (позитронно-эмиссионная компьютерная томография) позволяет обнаружить отдаленные метастазы размером до 1 мм.
- Определение онкомаркеров РЭА, СА72-4, СА19-9. При раке желудка эти маркеры не имеют диагностического значения как такового, но при исходном повышении нормы, их можно использовать в качестве контроля лечения и возникновения рецидива. После операции уровень онкомаркеров должен снизиться, он может достичь нормы. При возникновении рецидива или прогрессирования заболевания, он будет опять нарастать.

Доктор М.С. Бурдюков проводит диагностическое обследование желудка — ФГДС
Метастазирование аденокарциномы желудка
Для аденокарциномы характерно лимфогенное, гематогенное и имплантационное метастазирование.
Имплантационное метастазирование предполагает распространение клеток посредством контакта опухоли с воспринимающей поверхностью. В случае рака желудка такой поверхностью может быть брюшина, плевра, перикард, диафрагма. На четвертой стадии часто обнаруживается канцероматоз (массивное метастазирование в различные ткани).
Лимфогенное метастазирование подразумевает распространение опухоли по лимфатическим сосудам. Сначала поражаются близлежащие лимфатические узлы, а потом и более отдаленные. При раке желудка существуют специфические формы лимфогенных метастазов:
- Поражение узлов левой надключичной области — метастазы Вирхова.
- Поражение параректальных ЛУ — метастазы Шницлера.
- Поражение подмышечных ЛУ — метастазы Айриша.
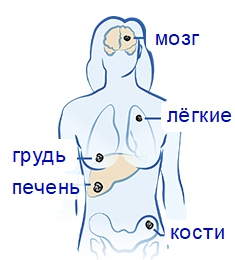
Гематогенное метастазирование предполагает перенос раковых клеток по кровеносным сосудам. Чаще всего поражается печень в результате миграции клеток по воротной вене. Также возможно поражение легких, почек, головного мозга, костного мозга.
Лечение аденокарциномы желудка
Лечение аденокарциномы зависит от стадии заболевания и гистологического типа опухоли. Как правило, оно носит комплексный характер и предполагает сочетание хирургической операции с химио- или лучевой терапией. Хирургический компонент здесь является ключевым фактором.
В рамках лечения может проводиться удаление всего желудка (гастрэктомия), или его части (резекция желудка). Одновременно удаляются ткани, пораженные злокачественными клетками — регионарные лимфатические узлы, части органов, куда проросла опухоль (печень, тонкая кишка, брюшина и др).
Химиотерапия и лучевая терапия могут применяться в дооперационном (неоадъювантный режим) и послеоперационном периоде (адъювантный режим). В первом случае их целью является уменьшение размеров опухоли, чтобы ее можно было удалить с наименьшим объемом тканей, а во втором — уничтожение оставшихся раковых клеток. Кроме того, применение химиотерапии и лучевой терапии может уменьшить выраженность болевого синдрома.
Если радикальное удаление образования невозможно, проводится паллиативное лечение. В этом случае оно направлено на устранение осложнений, вызванных аденокарциномой, и улучшение качества жизни больного. Например, если опухоль перекрыла просвет желудка, накладываются обходные анастамозы или выводится гастростома, благодаря чему пациент сможет питаться.
Прогноз аденокарциномы желудка
Прогноз при аденокарциноме зависит от стадии заболевания. Чем раньше начать лечение, тем более эффективным оно будет:
- При первой стадии пятилетняя выживаемость достигает 80%. Причем высоки шансы на полное выздоровление. К сожалению, на этой стадии рак желудка выявляется очень редко, как правило, случайно.
- На второй стадии пятилетняя выживаемость приближается к 55%. Половина из этих людей имеет шансы на полное излечение. Согласно данным литературы, менее 10% злокачественных опухолей желудка выявляются на второй стадии.
- При третьей стадии пятилетняя выживаемость находится на уровне менее 40%, а при четвертой — не превышает 5%. К сожалению, до 75% аденокарцином выявляется именно на четвертой стадии.

Профилактика
Профилактика рака желудка направлена на предотвращение или снижение воздействия факторов риска, приводящих к развитию данного заболевания:
- Нормализация питания. Употребление в пищу достаточного количества пищевых волокон (овощи, фрукты, каши), ограничение употребления соли, пряностей, маринадов и копченостей.
- Отказ от курения и злоупотребления алкоголем.
- Лечение инфекций и предраковых заболеваний — хронический гастрит, полипы желудка.
- Поддержание достаточного уровня физической активности
Запись
на консультацию
круглосуточно
Распад опухоли — это закономерное следствие слишком активного роста ракового узла по периферии или осложнение избыточно высокой реакции распространённого злокачественного процесса на химиотерапию.
Не каждому пациенту доводится столкнуться с тяжелой проблемой распада ракового процесса, но при любой интенсивности клинических проявлений инициируемое распадом злокачественной опухоли состояние непосредственно угрожает жизни и радикально меняет терапевтическую стратегию.
Распад опухоли: что это такое?
Распад — это разрушение злокачественного новообразования, казалось бы, что именно к распаду необходимо стремиться в процессе противоопухолевой терапии. В действительности при химиотерапии происходит уничтожение раковых клеток, только убийство органичное и не массовое, а единичных клеток и небольших клеточных колоний — без гибели большого массива ткани с выбросами в кровь из распадающихся клеток токсичного содержимого.
Под действием химиотерапии клетки рака приходят не к распаду, а к процессу апоптоза — программной смерти. Останки раковых клеток активно утилизируются фагоцитами и уносятся прочь от материнского образования, а на месте погибших возникает нормальная рубцовая ткань, очень часто визуально не определяющаяся.
Регрессия злокачественного новообразования в форме апоптоза происходит медленно, если наблюдать за новообразованием с перерывами в несколько дней, то заметно, как по периферии раковый узел замещается совершенно нормальной тканью и сжимается в размере.
При распаде раковый конгломерат не замещается здоровыми клетками соединительной ткани, мертвые клеточные пласты формируются в очаг некроза, отграничивающийся от остальной раковой опухоли мощным воспалительным валом. Внутри злокачественного новообразования некроз не способен организоваться и заместиться рубцом, он только увеличивается, захватывая новые участки ракового узла, походя разрушая опухолевую сосудистую сеть. Из мертвого очага в кровь поступают продукты клеточного гниения, вызывая интоксикацию.
При некоторых злокачественных болезнях крови или лимфатической ткани на фоне химиотерапии тоже возникает распад, но без формирования зоны некроза, при этом массово погибающие раковые клетки выбрасывают в кровь свое содержимое, которое не успевает утилизироваться фагоцитами, «забивает» почки и заносится в сосуды других органов. Именно массированный выброс клеточного субстрата становится причиной тяжелейшей интоксикации, способной привести к смерти.
Запись
на консультацию
круглосуточно
Причины распада злокачественной опухоли
Инициируют распад ракового образования всего только две причины: сама жизнедеятельность клеток злокачественной опухоли и химиотерапия.
Первая причина спонтанного — самопроизвольного распада характерна для солидных новообразований, то есть рака, сарком, злокачественных опухолей головного мозга и меланомы. Вторая причина распада типична для онкогематологических заболеваний — лейкозов и лимфом, при онкологических процессах встречается чрезвычайно редко.
С течением времени центральная часть злокачественного новообразования любой морфологической принадлежности начинает испытывать трудности с доставкой питательных веществ. Происходит это из-за того, что раковые клетки размножаются быстрее, чем формируется «кормящая» их сосудистая сеть. Голодающие клеточные пласты погибают, что проявляется распадом с образованием зоны некроза, отграниченной от живой опухолевой ткани, с постепенным формированием полости, в которой протекают процессы медленного гниения.
Если некротическая полость находится близко к коже, то может прорваться наружу в виде распадающегося «гнойника» и образованием незаживающей язвы, к примеру, молочной железы. В легком при рентгене внутри ракового узла с распадом будет видна тёмная «дырка» с отдельно расположенным внутри островковым кусочком некротической ткани — секвестром.
Второй вариант распада, типичный для онкогематологических заболеваний, можно констатировать по клиническим симптомам тяжелейшей интоксикации с осложнениями — тумор-лизис-синдрому (СОЛ) и биохимическим анализам крови, где резко повышена концентрация мочевой кислоты, калия и фосфора, но существенно снижен кальций. Конкретная побудительная причина для развития СОЛ — обширное злокачественное поражение с очень высокой чувствительностью к химиотерапии.
При онкологических процессах — раках, саркомах, меланоме реакция на цитостатики преимущественно умеренная и не столь стремительная, поэтому СОЛ принципиально возможен только в исключительных случаях мелкоклеточного, недифференцированного или анаплазированного злокачественного процесса.
Симптомы распада злокачественной опухоли
Клиническим итогом спонтанного распада раковой опухоли становится хроническая интоксикация, нередко сочетающаяся с симптомами генерализованного воспаления вследствие образования гнойного очага. Симптомы разнообразны, но у большинства отмечается прогрессивно нарастающая слабость, повышение температуры от субфебрильной до лихорадки, сердцебиение и даже аритмии, изменение сознания — оглушенность, нарушение аппетита и быстрая потеря веса.

Локальные проявления спонтанного разрушения раковой опухоли определяются её локализацией:
- рак молочной железы, меланома и карцинома кожи, опухоли ротовой полости — гнойная, обильно секретирующая открытая язва с грубыми подрытыми краями, часто источающая гнилостный запах;
- распадающаяся карцинома легкого — при прободении некротической полости в крупный бронх возникает приступообразный кашель с гнойной мокротой, нередко с прожилками крови, иногда случается обильное легочное кровотечение;
- разрушение новообразования органов желудочно-кишечного тракта — развитие локального перитонита при прободении ракового конгломерата в брюшную полость, кровотечение с чёрным стулом и рвотой кофейной гущей;
- распадающаяся карцинома матки — интенсивные боли внизу живота, нарушение мочеиспускания и дефекации при образование гнойных свищей.
Синдром опухолевого лизиса при лейкозах и лимфомах потенциально смертельное состояние, приводящее:
- в первую, очередь к осаждению кристаллов мочевой кислоты в почечных канальцах с выключением функции и острой почечной недостаточностью;
- дополнительно повреждает почки быстрое закисление крови — лактатацидоз;
- снижение уровня кальция и повышение фосфатов инициирует судорожный синдром, дополняемый неврологическими проявлениями вследствие выброса цитокинов;
- повышения калия негативно отражается на сердечной деятельности;
- выброс биологически-активных веществ из клеток приводит к повышению проницаемости мелких кровеносных сосудов, что снижает уровень белков и натрия крови, уменьшает объем циркулирующей плазмы, клинические проявляется падением давления и усугублением поражения почек;
- обширные и глубокие нарушения метаболизма во всех системах органов с исходом в полиорганную недостаточность.
Лечение распада опухоли
Для эффективного лечения распадающегося опухолевого конгломерата необходимо восстановление внутриопухолевого питания посредством быстрого формирования новой сосудистой сети, что совершенно невозможно. Поэтому при спонтанном распаде прибегают к симптоматической терапии, в том числе паллиативным хирургическим — «санитарным» вмешательствам.
Формально при распадающейся опухоли невозможна радикальная операция, зачастую заболевание считается неоперабельным, но химиотерапия и облучение исключаются из программы, потому что способны усугубить некроз. Отчаянное положение пациента и вероятность массированного кровотечения из изъеденного раком крупного сосуда оправдывает выполнение паллиативной операции, основная цель которой — удаление очага хронического воспаления и интоксикации.
Синдром лизиса опухоли лечится многочасовыми капельными вливаниями при усиленном диурезе — выведении мочи, связыванием мочевой кислоты специальными лекарствами. Одновременно поддерживается работа сердечно-сосудистой системы, купируется интоксикация и воспаление. При развитии острой почечной недостаточности проводится гемодиализ.
Синдром лизиса опухоли сложно лечить, но можно предотвратить или хотя бы уменьшить его проявления. Профилактика начинается за несколько дней до курса химиотерапии и продолжается не менее трёх суток после завершения цикла. Кроме специальных препаратов, выводящих мочевую кислоту, назначаются продолжительные капельницы, вводятся недостающие микроэлементы, а избыточные выводятся или связываются другими лекарствами.
Профилактика лизиса опухоли стала стандартом лечения онкогематологических больных, чего нельзя сказать об онкологических пациентах с распадающимися злокачественными процессами, которым очень сложно найти хирурга, готового выполнить паллиативную операцию. Во вмешательстве по санитарным показаниям отказывают из-за сложности выхаживания тяжелого больного после обширного хирургического вмешательства. В нашей клинике никому не отказывают в помощи.
Запись
на консультацию
круглосуточно
Список литературы
- Cairo M.S., Bishop M. /Tumour lysis syndrome: New therapeutic strategies and classification// Brit. J Haematol// 2004; 127.
- Howard S.C., Jones D.P., Pui C-H. /The Tumor Lysis Syndrome// N Engl J Med.; 2011;364(19).
- Jeha S. /Tumor lysis syndrome// Semin Hematol 2001; 38
- Sarno J./ Prevention and Management of Tumor Lysis Syndrome in Adults With Malignancy// J Adv Pract Oncol.; 2013; 4(2).
- Wossmann W., Schrappe M., Meyer U. et al./ Incidence of tumor lysis syndrome in children with advanced stage Burkitt’s lymphoma/leukemia before and after introduction of prophylactic use of urate oxidase//Ann Hematol, 2003.