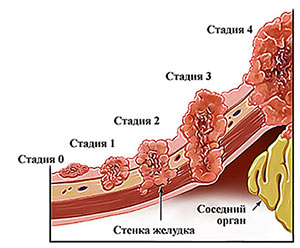
Рак проксимального отдела желудка
Рак желудка — злокачественная опухоль, которая развивается из клеток слизистой оболочки желудка. По распространенности он занимает пятое место среди всех видов рака. Как правило, болеют люди старше 40 лет. Основной метод лечения — хирургический, удаление всего желудка или его пораженной части.
Причины рака желудка
Точные причины рака желудка неизвестны. В слизистой оболочке органа возникают мутации ДНК, и получаются «неправильные» клетки, которые могут приобрести способность к неконтролируемому росту. Почему это происходит — не совсем понятно. Зато хорошо изучены факторы риска — условия, которые повышают риск рака желудка.
Наследственность и рак желудка
Некоторые люди носят в себе «бомбу замедленного действия», спрятанную в генах. Иногда даже не одну. Это подтверждается некоторыми фактами:
- Если у близкого родственника (родители, братья, сестры, дети) человека диагностирован рак желудка, его риски повышены примерно на 20%.
- Мужчины болеют чаще, чем женщины. Сложно сказать, с чем конкретно это связано, но можно предположить, что замешана разница между мужскими и женскими генами.
- Японцы, которые мигрировали в США, болеют раком желудка реже соотечественников, но чаще, чем «коренные» американцы. Это говорит о том, что дело не только в характере питания, но и в наследственности. Главный подозреваемый — ген под названием RNF43.
- Карцинома — самый распространенный тип рака желудка — чаще встречается у людей с группой крови A (II), которую они, конечно же, получили вместе с генами.
- Риски повышены при некоторых наследственных заболеваниях: злокачественной анемии (в 3-6 раз), гипогаммаглобулинемии, неполипозном раке толстой кишки.
- Заболеваемость раком желудка повышается после 70 лет: считается, что это происходит из-за того, что с возрастом в клетках тела накапливаются нежелательные мутации.
Рак желудка и характер питания
Роль питания в возникновении злокачественных опухолей желудка изучена хорошо. Риски повышает большое количество соли, крахмала, нитратов, некоторых углеводов. Чаще болеют люди, которые едят много соленых, копченых, маринованных продуктов, мало овощей и фруктов.
Рак желудка и вредные привычки
Курение повышает риск рака желудка примерно вдвое. Ученые в Великобритании считают, что примерно каждый пятый случай связан именно с курением. Когда человек вдыхает табачный дым, часть его попадает в желудок, и содержащиеся в нем вредные вещества повреждают клетки слизистой оболочки. Риски тем выше, чем больше стаж курильщика и ежедневное количество сигарет. Алкоголь тоже в списке подозреваемых, но прямых доказательств пока нет.
Хеликобактер пилори (H. Pylori) и рак желудка
H. Pylori — бактерия, которая способна вызывать язвенную болезнь и хронический атрофический гастрит. В настоящее время она считается важным фактором развития рака желудка. При хеликобактерной инфекции вероятность возникновения злокачественной опухоли в желудке повышается в 4 раза. В половине удаленных опухолей обнаруживают этого возбудителя.
Другие факторы риска
- Язвенная болезнь. Данные исследований по этому поводу противоречивы. Если язва находится в теле желудка, риск рака повышается почти в 2 раза. При язве нижнего отдела риски, видимо, не повышаются.
- Аденоматозные полипы слизистой оболочки.
- Семейный аденоматозный полипоз — заболевание, вызванное мутацией в гене APC и приводящее к возникновению множества полипов в желудке, кишечнике. При этом незначительно повышается риск рака.
- Перенесенные на желудке операции повышают риск рака в 2,5 раза. Это происходит из-за того, что желудок производит меньше соляной кислоты, и в нем активнее размножаются бактерии, продуцирующие нитриты, происходит обратный заброс желчи из тонкой кишки. Обычно злокачественные опухоли возникают спустя 10-15 лет после хирургического вмешательства.
- Социальное и материальное положение: риск увеличивается при низком уровне доходов, проживании в перенаселенной квартире, без удобств, в неблагоприятном районе.
- Другие онкологические заболевания: рак пищевода, простаты, мочевого пузыря, молочных желез, яичников, яичек.
- Болезнь Менетрие (гипертрофическая гастропатия) характеризуется разрастанием слизистой оболочки желудка, появлением в ней складок и снижением продукции соляной кислоты. Патология встречается редко, поэтому неизвестно, как часто она приводит к раку желудка.
- В группе повышенного риска работники угольной, металлургической и резиновой промышленности.
- Иммунодефицит повышает вероятность развития рака, лимфомы желудка.
Классификация рака желудка: каким он бывает?
Злокачественные опухоли желудка, согласно Международной гистологической классификации ВОЗ, делят на 11 типов, в зависимости от того, из каких клеток они происходят. Преобладает рак из железистых клеток, которые выстилают слизистую оболочку и вырабатывают слизь — аденокарцинома. Он составляет 90-95% всех случаев. Также встречаются опухоли из иммунных (лимфома), гормонпродуцирующих (карциноид) клеток, из нервной ткани.
Одна из старейших классификаций делит злокачественные опухоли желудка на 3 типа:
- Кишечный. Как следует из названия, в окружении опухоли имеется кишечная метаплазия, то есть слизистая оболочка желудка становится похожа на слизистую кишечника. Этот тип рака чаще встречается у пожилых людей, отличается более благоприятным прогнозом. Это типично «японский» тип рака.
- Диффузный. Опухолевые клетки расползаются по стенке желудка, они окружены нормальной слизистой оболочкой.
- Смешанный.

Аденокарцинома желудка
Стадии рака желудка
Рак желудка делят на ранний (начальный) и распространенный. При раннем опухоль не прорастает глубже слизистой оболочки и подслизистой основы. Такие опухоли проще удалить (в том числе эндоскопическим путем), при них лучше прогноз. Также используют классификацию TNM, которая учитывает размеры и прорастание в разные ткани первичной опухоли (T), метастазы в регионарных (близлежащих) лимфатических узлах (N), отдаленные метастазы (M).
Классификация в зависимости от состояния первичной опухоли (T):
- Tx — первичную опухоль невозможно оценить;
- T0 — первичная опухоль не обнаруживается;
- T1 — тяжелая дисплазия клеток слизистой оболочки, опухоль находится в поверхностном слое слизистой оболочки («рак на месте»);
- T2 — опухоль проросла в мышечный слой стенки органа;
- T3 — рак достиг серозной (наружной) оболочки желудка, но не пророс в нее;
- T4 — опухоль проросла в серозную оболочку (T4a), в соседние структуры (T4b).
Классификация в зависимости от наличия поражения в регионарных лимфатических узлах:
- Nx — невозможно оценить метастазы в лимфатических узлах;
- N0 — метастазы в регионарных лимфоузлах не обнаружены;
- N1 — поражены 1-2 лимфоузла;
- N2 — опухолевые клетки распространились в 3-6 лимфоузлов;
- N3 — метастазы в 7-15 (N3a) или в 16 и более (N3b) лимфоузлах.
Классификация в зависимости от наличия отдаленных метастазов:
- M0 — отдаленные метастазы не обнаружены;
- M1 — обнаружены отдаленные метастазы.
Аденокарциному делят на 4 стадии:
- I стадия (T1M0N0 — стадия Ia; T1N1M0, T2N0M0 — стадия Ib). Опухоль находится в пределах слизистой оболочки и подслизистой основы, не прорастает вглубь стенки желудка. Иногда раковые клетки обнаруживают в близлежащих лимфатических узлах.
- II стадия (T1N2M0, T2N1M0, T3N0M0 — стадия IIa; T1N3aM0, T2N2M0, T3N1M0, T4aN0M0 — стадия IIb). Опухоль прорастает в мышечный слой стенки желудка и распространяется в лимфатические узлы.
- III стадия (T2N3aN0, T3N2M0, T4aN1M0, T4aN2M0 — стадия IIIa; T1N3bM0, T2N3bM0, T3N3aM0, T4aN3aM0, T4bN1M0 — стадия IIIb; T3N3bM0, T4aN3bM0, T4bN3aM0 — стадия IIIc). Рак пророс через всю стенку желудка и, возможно, распространился на соседние органы, успел сильнее поразить близлежащие лимфатические узлы.
- IV стадия (любые T и N, M1). Есть отдаленные метастазы.
Метастазы рака желудка
Раковые клетки могут отрываться от материнской опухоли и мигрировать в другие части тела различными путями:
- С током лимфы они могут попасть в лимфатические узлы брюшной полости, а из них — в лимфоузлы надключичной области — метастаз Вирхова. Метастаз в лимфоузлы, окружающие прямую кишку, называют метастазом Шницлера.
- С током крови раковые клетки чаще всего распространяются в печень, реже — в легкие.
- Также раковые клетки могут рассеиваться по брюшной полости. Если они оседают на яичниках, образуется метастаз Крукенберга, в пупке — метастаз сестры Марии Джозеф.Редко при раке желудка обнаруживают метастазы в головном мозге, костях.
Симптомы: как проявляется рак желудка?
На ранних стадиях рак желудка либо не имеет симптомов вообще, либо маскируется под другие заболевания: гастрит, обострение язвенной болезни. Ухудшение аппетита и боли под ложечкой редко заставляют людей сразу же подозревать онкозаболевание и бежать в больницу. Обычно ограничиваются диетой и приемом разрекламированных таблеток «от желудка». Если человек уже страдает язвенной болезнью, он может воспринять первые признаки рака желудка как очередное обострение язвы. И уже позже, когда диагностировано онкологическое заболевание, больной вспоминает, что проявления были «не такими, как всегда».
Существует так называемый «синдром малых признаков» — его сформулировал один из основоположников советской онкологии, Александр Иванович Савицкий. Если беспокоят похожие симптомы — это повод сходить к врачу и провериться:
- Необъяснимая слабость и повышенная утомляемость.
- Плохой аппетит.
- Снижение работоспособности.
- Потеря веса.
- «Желудочный дискомфорт»: неприятные ощущения, из-за которых даже любимая еда больше не радует.
В дальнейшем нарастают более яркие, «кричащие» признаки. Они зависят от того, в какой части органа находится опухоль:
- Дисфагия. Возникает, если новообразование сдавливает место перехода желудка в пищевод. Сначала становится сложно глотать твердую пищу, затем и жидкую.
- Рвота недавно съеденной пищей. Характерна для опухолей в нижней части желудка, в месте перехода в двенадцатиперстную кишку.
- Стойкая изжога.
- Постоянные боли в области желудка, которые отдают в спину. Они не проходят ни днем, ни ночью.
- Потеря веса.
- Увеличение живота. Возникает из-за асцита — скопления жидкости в брюшной полости.
- Под ложечкой можно почувствовать и нащупать жесткое выпирающее образование. Это — опухоль, которая срослась с передней брюшной стенкой.
Со временем в опухоли начинаются процессы изъязвления и распада, развивается желудочное кровотечение. Проявляется оно в виде черного дегтеобразного стула, рвоты, которая выглядит как «кофейная гуща» или содержит примеси алой крови. Если человек теряет много крови, он становится бледным, возникает слабость, головокружение. У некоторых людей рак диагностируется, когда их приводят в клинику в таком состоянии на машине «Скорой помощи».
Как вовремя диагностировать заболевание? Что такое скрининг, и почему он важен?
Статистика говорит о том, что в 75% случаев рак желудка диагностируют уже на распространенной стадии, когда опухоль успевает прорасти в соседние ткани, дать метастазы. Лечить таких больных сложно, прогноз, как правило, неблагоприятный. Обычно выраженные симптомы говорят о том, что рак уже успел распространиться по организму.
Как проверить желудок на рак: на ранних стадиях помогает скрининг — регулярные обследования людей, которые не испытывают никаких симптомов. В качестве скринингового исследования применяют гастроскопию — эндоскопическое исследование, во время которого в желудок вводят гибкую трубку с миниатюрной видеокамерой и лампочкой на конце. Насколько эффективна гастроскопия? Лучше всего это демонстрирует японский опыт. Распространенность рака желудка в Японии очень высока, а смертность от него одна из самых низких в мире. Достичь этого удалось благодаря внедрению массового скрининга.
В Европейской онкологической клинике существуют специальные скрининговые программы, которые помогают вовремя диагностировать разные онкологические заболевания. Посетите врача, узнайте о своих рисках и получите индивидуальные рекомендации по поводу скрининга.
Какие методы диагностики может назначить врач?
Помимо гастроскопии, программа диагностики рака желудка может включать:
- Рентгенографию, перед которой пациенту дают выпить контрастный раствор. При этом контуры желудка хорошо видны на снимках.
- Компьютерную томографию, позитронно-эмиссионную томографию.
- Диагностическую лапароскопию. Это операция, во время которой в живот пациента через отверстия вводят лапароскоп с миниатюрной видеокамерой и специальные инструменты. Процедура помогает оценить, как далеко за пределы желудка успел распространиться процесс.
- Биопсию. Врач получает образец подозрительной ткани и отправляет в лабораторию для изучения под микроскопом. Этот метод диагностики помогает максимально точно диагностировать онкологическое заболевание и установить тип рака. Биопсию можно провести во время гастроскопии, хирургического вмешательства.
Современные принципы лечения рака желудка
Основной метод лечения рака желудка — хирургический. Объем операции зависит от того, на какой стадии обнаружена опухоль. Если она не успела распространиться вглубь стенки органа, проводят эндоскопическую резекцию — удаление пораженного участка при помощи инструмента, введенного через рот, как во время гастроскопии.
При субтотальной гастрэктомии удаляют часть органа, пораженную опухолевым процессом. На более поздних стадиях орган приходится удалять целиком вместе с окружающими тканями. При этом пищевод соединяют с тонкой кишкой. Если лимфатические узлы в брюшной полости поражены метастазами, их также нужно удалить.
В запущенных случаях, когда излечение невозможно, проводят паллиативную операцию. Хирург удаляет пораженную часть желудка, чтобы облегчить состояние пациента.
Лучевая терапия при раке желудка бывает:
- неоадъювантной — проводится перед операцией, чтобы уменьшить размеры опухоли и облегчить её удаление;
- адъювантной — чтобы уничтожить раковые клетки, которые остались в организме после операции.
Наиболее распространенные побочные эффекты лучевой терапии при облучении области живота: тошнота, нарушение пищеварения, диарея.
Химиотерапия также бывает адъювантной и неоадъювантной. Часто её сочетают с лучевой терапией. Химиолучевая терапия может стать основным методом лечения при метастатическом раке на поздних стадиях, когда прогноз неблагоприятный, но есть возможность облегчить симптомы и продлить жизнь больного.
В некоторых случаях эффективны таргетные препараты: трастузумаб, рамуцирумаб, иматиниб, сунитиниб, регорафениб. Но они подходят лишь в тех случаях, когда опухолевые клетки обладают определенными молекулярно-генетическими свойствами.
Какой прогноз при раке желудка?
Прогноз при раке желудка зависит от стадии опухоли, на которой был установлен диагноз и начато лечение. Шансы на стойкую ремиссию наиболее высоки, если опухоль не проросла за пределы слизистой оболочки и подслизистой основы. При метастазах прогноз, как правило, неблагоприятен.
В онкологии существует такой показатель, как пятилетняя выживаемость. Он показывает, какой процент больных остаются живы в течение 5-ти лет. Срок достаточно большой, в определенном смысле его можно приравнять к выздоровлению. Пятилетняя выживаемость при разных стадиях рака желудка составляет:
- I стадия — 57-71%;
- II стадия — 33-46%;
- III стадия — 9-20%;
- IV стадия — 4%.
Некоторые цифры и факты:
- Эксперты Всемирной организации здравоохранения (ВОЗ) утверждают, что ежегодно от рака желудка во всем мире погибают 754 000 людей.
- В XXI веке распространенность заболевания снижается, но в разных странах неодинаково. Так, на одного больного из Великобритании приходится двое из России и трое из Японии.
- По распространенности среди прочих онкозаболеваний рак желудка занимает пятое место, но среди причин смерти — третье.
- Одна из лидирующих стран по распространенности рака — Япония, во многом за счет характера питания.
В Европейской онкологической клинике применяются наиболее современные методы лечения рака желудка и других онкологических заболеваний. Даже если прогноз неблагоприятен, это не означает, что больному ничем нельзя помочь. Наши врачи знают, как облегчить симптомы, обеспечить приемлемое качество жизни, продлить жизнь
Цены на лечение рака желудка на 1-4 стадиях в Европейской онкологической клинике
- Гастроэнтеростомия — 72 200 руб.
- Дистальная резекция желудка с лимфаденэктомией — 192 900 руб.
- Удаление гастростомы — 77 900 руб.
- Консультация клинического онколога — от 4 100 рублей
Подробнее о диагностике рака желудка
Подробнее о лечении рака желудка
Запись
на консультацию
круглосуточно
В сложной и многоплановой проблеме диагностики и лечения рака желудка особое место занимает рак проксимальною его отдела [1, 2, 3, 9].
За последние два десятилетия достстигнуты определенные успехи в диагностике и лечении рака этой локализации, которые обусловлены усовершенствованием методов диагностики, техники оперативных вмешательств, совершенствованием анестезтологического пособия, проведением обоснованной пред- и послеоперационной терапии. Однако, по-прежнему, число больных с распространенным раком желудка, в том числе и проксимального отдела, остается довольно высоким и не имеет тенденции к снижению [4, 5, 7, 8, 10].
Сложности своевременного распознавания рака проксимального отдела желудка состоит в том, что клинические проявления его, особенно на ранних стадиях, не отличаются от таковых при различных хронических желудочных заболеваниях.
Диагностика рака проксимального отдела желудка представляется трудной и сложной не только для врачей общего профиля, но и для специалистов, занимающихся изучением патологии желудочно-кишечного тракта.
Анализ результатов проведенного обследования 400 радикально леченных больных выявил явное преимущество комплексных методов в установлении диагноза заболевания.
Результат анализа хирургического лечения больных свидетельствует о травматичности и сложности операции при раке проксимального отдела желудка. Это подтверждается тем, что из 400 радикально выполненных операций 179 (49,2%) сопровождались осложнениями, послеоперационная летальность составила 26,4%.
Более частое возникновение осложнений отмечено при проксимальной резекции (55,7%), чем при экстирпации желудка (47,7%), послеоперационная летальность — 29,1% и 25,6% соответственно. Среди осложнений наиболее часто наблюдается пневмония, которая отмечена у каждого третьего больного (33,5%), а в сочетании с другими осложнениями -у 14,5% больных. Второе место по частоте занимает перитонит — 18,9%, который является основной причиной послеоперационной смертности • 35,4% из числа всех осложнений, закончившихся летальным исходом. Перитонит в сочетании с другими осложнениями отмечен у 45 больных (25,1%), из которых 43 (95,6%) погибли в послеоперационном периоде.
Большинство хирургов, занимающихся лечением рака проксимального отдела желудка, видит путь к повышению результатов лечения в возможности расширения блока удаляемых или резецируемых органов. Поэтому до настоящего времени вопрос об обоснованности комбинированных операции продолжает оставаться предметом дискуссии. Анализ нашего материала основан на изучении 160 (43,9%) больных, подвергнутым комбинированным операциям.
Полученные нами данные позволяют сделать вывод о том, что какие бы не производились расширенные комбинированные операции, отдаленные результаты хирургического лечения определяются состоянием регионарного лимфатического аппарата.
Наши данные свидетельствуют о том, что основными показаниями к дополнительному удалению или резекции органа является прорастание в него рака желудка или наличие метастазов в регионарных лимфатических ушах, радикальное удаление которых невыполнимо без хирургического вмешательства на рядом расположенном органе. Имеются все основания считать, что радикализм онкологической операции заключается не только в необходимом объеме удаляемых тканей пораженного органа, но и в полноте регионарной лимфаденэктомии.
Как и при всех операциях, выполняемых по поводу рака проксимального отдела желудка, наиболее частыми осложнениями являются перитонит (22,4%) и пневмония (27,1%). Перитонит в сочетании с другими осложнениями развился у 22 больных (25,9%), больных, а пневмония у 9 (10,6%). Общее число осложнений составило 53,1%, послеоперационная летальность — 29,4%, которая практически была одинакова как среди больных, перенесших комбинированную экстирпацию желудка, так и комбинированную проксимальную резекцию — 29,2% и 30,0% соответственно(p<0.001).
С целью улучшения результатов лечения больных раком проксимального отдела желудка в последние годы широкое применение получил комбинированный метод лечения, при этом лучевая терапия, как правило, предшествует хирургическому вмешательству.
Главная задача предоперационного облучения состоит в девитализации опухолевых элементов и, тем самым, профилактике обсеменения опухолевыми клетками во время операции.
Задаче повышения абластичности хирургического вмешательства вполне отвечают режимы крупного фракционирования дозы, при которых за счет увеличения дозы возрастает вероятность повреждения радиорезистентных клеток, резко сокращается время, необходимое для выполнения предоперационного облучения в концентрированном режиме, опережает развитие грубых морфологических постлучевых изменений в зоне воздействия ионизирующей радиации.
Нами использована методика крупнофракционного облучения в суммарной очаговой дозе 20 Гр, проводимой за 4 ежедневных фракции по 5 Гр, что эквивалентно суммарной очаговой дозе 31 Гр при стандартном режиме.
На основании проведенного сравнительного анализа осложнений после комбинированного и хирургическою лечения отдаленных результатов было установлено, что выполнение операции с предварительным облучением в концентрированном режиме наиболее обосновано и оправдано при недифференцированном раке проксимального отдела желудка, эндофитном его росте и без распространения опухоли на пищевод.
По нашим данным, противопоказаниями для комбинированного лечения рака проксималыюго отдела желудка являются следующие:
подозрение на возможность перфорации или кровотечения из опухоли;
выраженное перифокальное воспаление вокруг новообразования;
артериальная гипертония с высокими цифрами артериального давления;
врожденные и приобретенные пороки сердца;
хроническая ишемическая болезнь сердца с частыми приступами стенокардии;
тяжелые нарушения ритма сердечной деятельности;
сердечная недостаточность II-III степени;
признаки печеночной и почечной недостаточности;
выраженные нарушения со стороны свертывающей системы крови;
отдаленные метастазы.
Учитывая что качественные изменения в ткани опухоли в ранние сроки (до трех суток) после облучения в концентрированном режиме трудно определимы, особый интерес, с точки зрения оценки чувствительности опухоли к лучевому воздействию, представляют количественные критерии, определяемые морфологически. Радиационный патоморфоз изучался по ряду тканевых и клеточных показателей: объему оставшейся после облучения паренхимы опухоли, индексу повреждения опухолевых клеток, митотическому индексу, доле патологических митозов.
Полученные данные свидетельствуют о том, что пострадиационные изменения в опухоли проявлялись неравномерно и наступали как в центральных, так и периферических ее участках.
Количественные показатели радиационного повреждения опухоли характеризовались уменьшением объема ее паренхимы до 27,0 ед, по сравнению с контрольной группой — 77,0 ед. Величина индекса повреждения колебалась в широких пределах — от 3,0% до 67,0%, составляя в среднем по группе 49,0%.
Другим важным количественным показателем является митотический режим опухоли. Как нам удалось установить, под влиянием лучистой энергии в митотическом режиме опухоли происходили определенные сдвиги, выражающиеся прежде всего снижением митотического индекса. Так, если в необлученных опухолях этот показатель был равен 8,0%, то после облучения он значительно снизился и оказался равным 2,3%. Следует подчеркнуть, что в отдельных случаях митозы в клетках опухолей полностью отсутствовали, а паренхима оказалась максимально поврежденной. Кроме того, было отмечено отчетливое увеличение количества патологических митозов.
При изучении отдаленных результатов лечения больных раком проксимальною отдела желудка в зависимости от степени повреждения опухоли под воздействием облучения оказалось, что при индексе повреждения менее 50,0% ни один больной не дожил до пятилетнего срока(p<0.001).
В другой группе (индекс повреждения более 50,0%) пятилетняя выживаемость составила 37,9%.
Таким образом, предоперационное облучение рака проксимального отдела желудка в концентрированном режиме вызывает объективные дегенеративные изменения в опухолевых клетках, что может быть выявлено методами количественной морфологической оценки. Представляется, что эти методы могут найти применение в качестве объективного критерия в контроле эффективности различных схем и способов предоперационного облучения.
Данные, полученные на основании проведенного исследования, свидетельствуют о том, что комбинированный метод улучшает отдаленные результаты лечения по сравнению с хирургическим, практически вдвое. Так, 3-летняя выживаемость больных, подвергнутых комбинированному лечению, составила 54,3% в то время как после хирургического лечения — 27,9%, 5-лстняя выживаемость составила соответственно 35,8% и 17,9%(медиана=34,2 ; x2=0,7426 ;P=0,4036).
Следует отметить, что в группе больных, имеющих неблагоприятные прогностические признаки, результаты комбинированного лечения были значительно выше, чем после хирургического лечения. Так, каждый второй больной (50,6%), подвергнутый лечению по поводу недифференцированного рака проксимального отдела желудка, доживает до пятилетнего срока, в то время как при хирургическом лечении до этого периода доживает только 2,8% больных.
Улучшение результатов комбинированного лечения по сравнению с хирургическим наблюдается и при эндофитной форме рака — 31,6% и 11,1%(p<0,001) соответственно. Отмечена тенденция улучшения пятилетних результатов лечения и больных, подвергнутых комбинированному лечению, при гистологически подтвержденных метастазах рака в регионарных лимфатических узлах (18,1% и 11,1% соответственно), при переходе опухоли на пищевод (29,6% и 14,6% соответственно(p<0,001)). При локализации опухоли только в проксимальном отделе желудка и отсутствии метастазов в регионарных лимфатических узлах отдаленные результаты лечения при комбинированном методе увеличиваются вдвое. Так, при раке проксимального отдела желудка без перехода на пищевод пятилетняя выживаемость составила 46,8% после комбинированного лечения, а после хирургического — 20,1%; без вовлечения в опухолевый процесс регионарных лимфатических узлов — 54,6% и 27,0% соответственно. При этом заслуживает тот факт, что число осложнений практически одинаково как при комбинированном так и при хирургическом методах лечения (48,1% и 44,5% соответственно). Послеоперационная летальность при комбинированном лечении составила 25,9%, при хирургическом — 22,5%. Предварительное лучевое воздействие по разработанной методике не увеличивает кровопотери во время операции, не осложняет ход операции и не является препятствием для выполнения любого необходимого объема хирургического вмешательства.
При изучении результатов комбинированною лечения в зависимости от режима облучения оказалось, что пятилетняя выживаемость при подвижном способе концентрированного облучения, проводимом на γ-терапевтическом аппарате РОКУС, выше, чем при статистическом (54,0% и 20,6% соответственно).
Таким образом, комбинированное лечение с использованием предоперационного облучения в концентрированном режиме представляет собой перспективный метод, способствующий повышению выживаемости больных раком проксимального отдела. Такое лечение является адекватным и не сопровождается увеличением числа послеоперационных осложнений и легальности.
В настоящее время в клиническую онкологию входят понятие не только о том «сколько прожил» онкологический больной, но и «как он прожил» эти годы. Именно в этом плане особое место занимает изучение форм и методов коррекции состояния больного, а также границ и возможностей социально-трудовой реабилитации.
Оценивая результаты восстановления трудоспособности больных раком проксимального отдела желудка, необходимо отметить, что каждый второй вернулся к труду — 53,3%.
Наиболее выраженное влияние на восстановление трудоспособности оказало профессиональное положение больных. Лица умственного труда чаще возвращаются к работе (89,7%), по сравнению с лицами физического и неквалифицированного физического труда (41,8%). Однако, программа социальной реабилитации онкологических больных, оперированных по поводу рака проксимального отдела желудка, представляется достаточно сложной. Тяжелые анатомо-функциональные нарушения, связанные с радикальным лечением, возможность развития рецидивов и метастазов, необходимость проведения повторных курсов лечения затрудняют восстановление трудоспособности и накладывают определенный отпечаток на психику больного, его положение в обществе и отношения в семье.
Всестороннее изучение процесса реабилитации в динамике показало, что имеется ряд факторов, использование которых может привести к расширению ее границ и возможностей. К их числу следует отнести: санаторно-курортное лечение и периодическое общеукрепляющее лечение в условиях стационара; оправданное и обусловленное сокращение сроков инвалидности II группы и перевод на III группу с правом возвращения к адекватному труду; предоставление работающим больным права на дополнительный отпуск и сокращенный рабочий день.
Таким образом, комплексная диагностика, способствующая выявлению ранних форм рака проксимального отдела желудка, применение комбинированного лечения, реабилитация этих больных способствуют улучшению результатов лечения больных раком проксимального отдела желудка.