Пептическая язва анастомоза после резекции желудка лечение
Пептическая язва анастомоза — постгастрорезекционный язвенный дефект в области желудочно-кишечного соустья. Проявляется болью в эпигастрии, околопупочной или правой подреберной области, диспепсией, похудением, астеническим синдромом. Диагностируется с помощью эзофагогастродуоденоскопии, рентгенографии желудка, УЗИ органов брюшной полости, радионуклидного исследования, гистаминового теста, биохимического анализа крови. Для лечения используют антисекреторные, цитопротективные, антацидные, антибактериальные препараты, стимуляторы регенерации. При отсутствии эффекта проводят ререзекцию, ваготомию, удаление желудка или его части, операции на паращитовидных железах.
Общие сведения
Впервые о пептической язве, возникшей у пациента с гастроэнтеростомой, сообщил в 1899 году немецкий хирург Г. Браун. Аналогичный язвенный дефект после гастрорезекции был описан австрийским хирургом Г. Хаберером в 1929 году. По результатам наблюдений, образованием язвы анастомоза осложняется до 5-10% гастроэнтеростомий, 0,5-2% резекций желудка, 0,5-1% антрумэктомий с пересечением блуждающего нерва, 5-15% дренирующих вмешательств с ваготомией. В 90-98% случаях патология диагностируется у больных, прооперированных по поводу язвенной болезни двенадцатиперстной кишки. Особенностью рецидивировавшей пептической язвы является более тяжелое течение с быстрым возникновением опасных для жизни осложнений.

Пептическая язва анастомоза
Причины пептической язвы анастомоза
Дефект слизистой оболочки в области гастроеюнального соустья обычно формируется из-за технических ошибок и сохранения высокого уровня секреции переваривающих компонентов желудочного сока после выполнения хирургического вмешательства. По наблюдениям специалистов в области гастроэнтерологии, причинами образования язвы анастомоза становятся:
- Необоснованно экономная резекция. При удалении менее 2/3 желудка зачастую сохраняется кислотопродуцирующая зона. Ситуация усугубляется отказом от пересечения блуждающего нерва или его ветвей, стимулирующих секрецию пептических факторов.
- Технические ошибки резекции на выключение. При выполнении операции по методу Бильрот II на дуоденальной культе может частично остаться антральная слизистая. Из-за выключения кислого тока указанный участок продуцирует избыток гастрина.
- Высокий тонус блуждающего нерва. Парасимпатическая нервная система стимулирует выделение пептического сока. При вагусной гипертонии или сочетании экономной гастрорезекции с неполной ваготомией сохраняется первопричина пептической язвы.
- Эндокринная патология. Рецидив заболевания отмечается у 75% пациентов с синдромом Золлингера-Эллисона. Повторному образованию язвы также способствует гиперсекреция желудочного сока при гиперпаратиреозе (синдромах Вермера, Сиппла, Шимке).
Патогенез
Основой развития пептической язвы анастомоза является дисбаланс между сохранившимся высоким уровнем производства агрессивных компонентов желудочного секрета, оказывающих повреждающий эффект на слизистую соустья, и снижением активности защитных факторов. Особенности патогенеза заболевания зависят от причин, спровоцировавших рецидив язвенной болезни. При недостаточном иссечении кислотопродуцирующей части желудка соляная кислота и пепсин продуцируются в количестве, практически сопоставимом с дооперационным периодом.
В остальных случаях выявляются условия, способствующие гиперстимуляции париетальных и главных клеток фундальных желудочных желез, — вагусный эффект (при гипертонусе или неполном пересечении блуждающего нерва), гастринемия (при сохранении G-клеток пилорической части, синдроме Золлингера-Эллисона), гиперкальциемия (при гиперпаратиреоидных состояниях). Одновременно в зоне анастомоза в результате послеоперационного нарушения иннервации и кровоснабжения снижается выработка слизи, простагландинов, медленнее восстанавливается эпителий. В результате действие агрессивных факторов недостаточно компенсируется защитными механизмами, в слизистой соустья постепенно формируется язвенный дефект.
Симптомы пептической язвы анастомоза
Заболевание развивается в срок от 6 месяцев до 3 лет после операции. У пациентов появляются интенсивные «голодные» и ночные боли, которые в зависимости от разновидности выполненного анастомоза имеют различную локализацию (околопупочная область, эпигастрий, правое подреберье). Зачастую наблюдается иррадиация болей в левую лопатку, кардиальную область, поясницу. Интенсивность болевых ощущений притупляется после еды, приема атропинсодержащих препаратов, бикарбоната натрия. Возникают диспепсические расстройства: тошнота, рвота, изжога, отрыжка кислым, метеоризм, диарея. При длительном течении пептической язвы боли приобретают постоянный характер, их появление теряет связь с приемом пищи или лекарственных препаратов. Наблюдается нарушение общего состояния пациента, включающее ухудшение аппетита, снижение трудоспособности, потерю веса. Возможна субфебрильная температура тела.
Осложнения
У некоторых больных выявляется пенетрация язвы в соседние органы (поджелудочную железу, брыжейку) с изменением типичного ритма и характера болей. При формировании желудочно-ободочного свища зачастую наблюдается каловая рвота. Частое осложнение пептической язвы — перфорация, сопровождающаяся профузным кровотечением, которое требует немедленной медицинской помощи. Иногда происходит инвагинация тощей кишки в желудок, проявляющаяся кровавой рвотой, сильными болями и возникновением опухолевидного образования в эпигастральной области. При хроническом течении болезни может формироваться сужение анастомоза, приводящее к затруднениям прохождения пищи. В редких случаях диагностируется малигнизация язвы.
Диагностика
Постановка диагноза пептической язвы анастомоза не представляет затруднений при наличии характерной клинической картины и сведений о проведенном оперативном вмешательстве. Диагностика заболевания направлена на определение локализации и размеров дефекта, выявление осложнений и сопутствующих патологий желудочно-кишечного тракта. Наиболее информативными являются:
- Эзофагогастродуоденоскопия. Введение гибкого эндоскопа в пищевод и культю желудка позволяет оценить состояние анастомоза, обнаружить язвенный дефект, выявить гиперемию и отечность слизистой. Во время эндоскопии выполняется биопсия пораженного участка для последующего гистологического исследования.
- Рентгенография желудка. Контрастирование пищеварительного тракта при помощи перорального приема сульфата бария помогает обнаружить характерные признаки пептической язвы на рентгенограмме — наличие «ниши», конвергенцию складок слизистой. Метод также применяется для оценки моторной функции желудка.
- УЗИ брюшной полости. В ходе ультразвукового исследования можно изучить структуру органов пищеварительного тракта и гепатобилиарной системы, состоятельность анастомоза. Методику дополняют проведением дуплексного сканирования сосудов для выявления патологии чревного ствола, брюшного отдела аорты.
- Радионуклидное исследование. Внутривенное введение препарата, меченного радиоизотопом, проводится для определения секреторной функции культи желудка. При пептической язве отмечается избыточное накопление изотопа в области анастомоза, что свидетельствует об оставленном участке антрального отдела.
- Гистаминовый тест. Метод дает возможность исследовать базальную и стимулированную секрецию желудочных желез. Исследование имеет высокую информативность для диагностики синдрома Золлингера-Эллисона, при котором отмечается высокая активность базальной секреции, слабый ответ на подкожное введение гистамина.
В клиническом анализе крови наблюдается умеренный лейкоцитоз, незначительное повышение СОЭ, может снижаться количество гемоглобина и эритроцитов, что является признаком кровотечений из пептической язвы. В биохимическом анализе крови определяется гипопротеинемия, повышение содержания гастрина (при болезни Золлингера-Эллисона), увеличение показателей кальция и паратгормона (при гиперпаратиреозе). Для оценки качества проведенной ваготомии производится инсулиновый тест, положительный результат которого указывает на сохранность волокон блуждающего нерва.
Дифференциальная диагностика проводится с другими видами болезней оперированного желудка, злокачественными желудочными неоплазиями, первичной язвой тонкой кишки, несостоятельностью анастомоза, острым аппендицитом, панкреатитом, холециститом. Кроме гастроэнтеролога пациенту необходимы консультации хирурга, онколога, гематолога, эндокринолога.
Лечение пептической язвы анастомоза
В большинстве случаев эффективным оказывается прием препаратов, снижающих секреторную функцию желудка, — ингибиторов М-холинорецепторов, H2-гистаминоблокаторов, ингибиторов протонной помпы в комбинации с цитопротективными, антацидными, регенерирующими средствами. При возможном хеликобактериозе проводится антибактериальная элиминация возбудителя с помощью β-лактамных пенициллинов, макролидов, других антибиотиков. Медикаментозную терапию дополняют коррекцией диеты. Оперативное лечение рекомендовано пациентам с терапевтически резистентной пептической язвой, гастриномой, осложненным течением заболевания. С учетом клинической ситуации выполняют:
- Корригирующие операции. Позволяют устранить механические или функциональные нарушения пищеварения. Создание условий для максимально физиологического переваривания пищи обеспечивается путем ререзекции с созданием нового анастомоза, трансторакальной или поддиафрагмальной стволовой, селективной проксимальной ваготомии, комбинации этих операций.
- Удаление пораженной части или органа. При повторной пептической язве пациентам с болезнью Золлингера-Эллисона показано удаление доброкачественной опухоли желудка (солитарной гастриномы), резекция желудка с ваготомией, тотальная гастрэктомия. Для коррекции гипертиреоза производится субтотальное или тотальное удаление паращитовидных желез.
Прогноз и профилактика
Послеоперационные гастроеюнальные язвы характеризуются рецидивирующим течением с частыми осложнениями. Прогноз относительно неблагоприятный, у ослабленных пациентов с тяжелыми сопутствующими патологиями возрастает риск летального исхода. Профилактика пептических язв заключается в тщательном выборе метода создания анастомоза, проведении резекции не менее двух третей желудка для снижения кислотопродуцирующей функции, соблюдении техники хирургического вмешательства, назначении эффективной консервативной терапии для эрадикации хеликобактерной инфекции перед операцией, лечении сопутствующих заболеваний.
Впервые возникновение пептической язвы после гастроэнтеростомии описал Н. Braun в 1899 г., а после резекции желудка – Н. Haberer в 1929 г. В литературе за последние 20 лет авторы приводят частоту постгастрорезекционных пептических язв от 1 до 4% [3]. 90 — 98% пептических язв соустья развиваются после резекции, выполненной по поводу язвы двенадцатиперстной кишки. Это связывают с тем, что дуоденальные язвы, как правило, сопровождаются желудочной гиперсекрецией и гиперхлоргидрией, а сохранение секреторной функции культи желудка на уровнях, сравнимых с дооперационными, и является основной причиной развития пептической язвы.
Выделяют четыре основные причины сохранения кислотопродукции в культе желудка: 1) экономная резекция (менее 2/3) без ваготомии, с сохранением кислотопродуцирующей зоны; 2) оставление части антральной слизистой оболочки на культе двенадцатиперстной кишки при резекции по второму способу Бильрота; 3) гипертонус блуждающих нервов и неполная ваготомия, если она выполнялась в сочетании с экономной резекцией желудка; 4) эндокринные заболевания – первичный гиперпаратиреоидизм, синдром Золлингера-Эллисона, синдром Вермера и др. Из указанных причин чаще всего встречаются первые две. Они являются техническими погрешностями операции. Самая распространенная ошибка – экономная резекция желудка при язве двенадцатиперстной кишки без ваготомии.
Она не только не снижает повышенной кислотности и пептической активности желудочного сока, но и создает условия для постоянного воздействия агрессивного желудочного содержимого на слизистую оболочку тощей или двенадцатиперстной кишки в результате удаления привратника. Другая характерная ошибка – оставление части антрального отдела на культе двенадцатиперстной кишки. Чаще всего это бывает при резекции на выключение, когда не иссекается антральная слизистая оболочка в оставляемом участке желудочной стенки. Выключенный из тока кислого желудочного содержимого антральный отдел при этом является постоянным источником гастринемии, причем уровни сывороточного гастрина могут быть при этом так велики, а течение болезни так жестоко, что отличить эту патологию от синдрома Золлингера-Эллисона до операции можно только по результатам определения уровней гастрина с применением секретинового теста. Причины гипергастринемии при отключенном антральном отделе – в отсутствие тормозящего действия хлористоводородной кислоты на гастринпродуцирующие клетки антральной слизистой оболочки и в вагусной денервации [1].
Сведения о гипертонусе блуждающих нервов как причине сохранения кислотопродукции в культе желудка в литературе немногочисленны. Замечено, что даже при значительных по объему резекциях и отсутствии эндокринных расстройств у 5-10% больных кислотность остается высокой. Попытки выделить группу больных с гипертонусом блуждающих нервов по различным секреторным тестам, в том числе и с ложным кормлением, вряд ли могут значительно помочь хотя бы из-за трудностей интерпретации результатов в условиях резецированного желудка (с одной стороны, быстрая эвакуация кислоты, с другой – заброс щелочного кишечного содержимого в культю желудка). Тем не менее, на основании благоприятных непосредственных и отдаленных результатов изолированной ваготомии при пептических язвах можно сделать вывод о наличии у таких пациентов гипертонуса блуждающих нервов [1].
Следующая группа причин пептической язвы — эндокринные заболевания. Встречаются они редко, но значение их определяется, например, тем фактом, что больные с синдромом Золлингера-Эллисона имеют в анамнезе операцию и страдают рецидивной язвой. По некоторым данным, у 75% больных с синдромом Золлингера-Эллисона язвы имеют типичную локализацию, при этом может не быть ни клинических, ни лабораторных специфических признаков. Попытки рентгенологической диагностики синдрома основываются на ряде признаков: 1) большой атоничный желудок с грубыми складками или гиперсекреция в маленькой культе; 2) большая атоничная двенадцатиперстная кишка; 3) усиленная перистальтика, быстрый пассаж по тонкой кишке, отек слизистой оболочки; 4) необычная локализация язвы с признаками пенетрации. Единственным достаточно точным методом дооперационной диагностики синдрома Золлингера-Эллисона является радиоиммунологическое исследование уровней гастрина в периферической крови.
Другой важный вопрос при выявлении синдрома Золлингера — Эллисона состоит в локализации источника гипергастринемии до операции, так как это может радикально изменить лечебную тактику. Дело в том, что, во-первых, различают два типа синдрома Золлингера-Эллисона: тип 1–без опухоли вообще, обусловленный гиперплазией гастринпродуцирующих клеток антрального отдела желудка, и тип 2–когда источник гастрина (опухоль-гастринома) локализуется вне антрального отдела. При первом типе можно добиться излечения применением простой резекции желудка с ваготомией. Трудности локализации гастрином при втором типе состоят в том, что опухоль может быть микроскопической (в стенке двенадцатиперстной кишки), множественной, злокачественной и давать метастазы, которые также продуцируют гастрин.
При синдроме Вермера чаще всего поражаются паращитовидные железы, поджелудочная железа, гипофиз, надпочечники, реже щитовидная железа. При синдроме Сиппла развивается медуллярная карцинома щитовидной железы, медуллярная феохромоцитома и гиперпаратиреоидизм; при синдроме Шимке – то же самое, плюс выступающая челюсть, толстые губы, марфаноподобный вид, множественные невриномы на слизистых оболочках, гастроинтестинальный нейроматоз, плоскостопие. Гиперпаратиреоидизм, входящий в понятие полиэндокринного аденоматоза, может быть первичным и также приводить к возникновению желудочных и дуоденальных язв. Непаратиреоидные опухоли (в том числе и гастринома) могут продуцировать паратгормон и тем самым вызывать гиперкальциемию и гипофосфатемию. В дифференциальной диагностике первичного гиперпаратиреоидизма в этом случае может помочь только селективная катетеризация сосудов с забором крови непосредственно от паращитовидных желез и определением в ней уровня паратгормона [1].
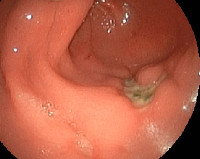
При типичной клинической картине диагностика пептической язвы не сложна. Сильные голодные (в том числе ночные) боли в эпигастральной области, уменьшающиеся после еды или приема соды, атропина, тошнота и рвота (каловая при осложнении язвы развитием желудочно-ободочного свища), поносы, похудание, рецидивирующее желудочно-кишечное кровотечение позволяют заподозрить наличие язвы в желудочно-кишечном анастомозе [1-3]. Зачастую пептические язвы протекают гораздо более злокачественно, чем первичная язва, по поводу которой была предпринята операция. Пептические язвы располагаются, как правило, на кишечной стороне гастроэнтероанастомоза, вблизи брыжеечного края кишки, что объясняет склонность таких язв к кровотечению, которое бывает часто очень сильным. Нередко одновременно существуют две язвы в области анастомоза (рис.).

Рис. Две пептические язвы, выявленные при эндоскопическом исследовании области желудочно-кишечного анастомоза
Эти язвы достигают иногда больших размеров, они пенетрируют в соседние органы и ткани (брыжейку тонкой и ободочной кишки, поджелудочную железу, печень, диафрагму), что объясняет часто очень выраженный болевой синдром.
Однако клиника может быть и не такой яркой. Боли могут быть умеренными или даже отсутствовать вовсе. В таких случаях пептическая язва проявляется обычно желудочно-кишечным кровотечением.
Рентгенологическая диагностика пептической язвы сложна и выявляет в среднем 50-65% от всех язв анастомоза. Это связано с наличием в области анастомоза различных деформаций и карманов, в которых может маскироваться язва и которые в свою очередь могут симулировать ее.
Лучше всего выявляются пептические язвы при эндоскопическом исследовании, но и эндоскопия может мало помочь, если не удается пройти аппаратом в приводящую или отводящую петлю, т. е. ниже анастомоза. При эндоскопическом исследовании в подавляющем большинстве случаев язва обнаруживается на приводящей или отводящей петле тонкой кишки.
В ряде случаев при яркой клинической картине и при обнаружении гиперацидности в культе желудка сама язва не выявляется ни рентгенологически, ни эндоскопически, а иногда даже и на операции. Пептическая язва иногда может быть поверхностной, легко заживать от консервативного лечения, но затем быстро рецидивирует, давая подчас осложнения, чаще всего кровотечение [1].
Консервативное лечение пептической язвы анастомоза включает назначение больным блокаторов Н2-рецепторов, ингибиторов протоновых помпов. При подозрении на H. pylori назначаются антибиотики. Большинство больных поддаются медикаментозному лечению. Хирургическое лечение показано больным, для которых консервативная терапия малоэффективна, при гастриноме, при таких осложнениях как профузное кровотечение, перфорация, сужение анастомоза, желудочно-ободочный свищ [3].
Повторные операции на желудке и кишечнике при язвенной болезни предпринимаются нечасто и являются сложными вмешательствами. Из большого числа операций, предложенных для лечения болезней оперированного желудка, можно выделить две основные группы: одна направлена на ликвидацию всевозможных функциональных (патофизиологических) или механических расстройств – так называемые корригирующие операции; вторая преследует цель удаления пораженной части или целого органа. Важным моментом и при тех, и при других операциях является создание условии для пищеварения, максимально приближенных к физиологическим, для чего, например, стремятся восстановить дуоденальный пассаж путем реконструкции анастомоза по Бильрот I или за счет использования одного из вариантов гастроеюнодуоденопластики [1].
Диапазон операций, применяемых при пептической язве желудочно-кишечного соустья, довольно широк. Это и ререзекция по обоим способам Бильрота в различных модификациях, ваготомия стволовая (трансторакальная и поддиафрагмальная) и селективная желудочная, а также различные сочетания ваготомии и ререзекции.
Выбор операции при пептической язве зависит прежде всего от ее причины. В этом смысле большое значение приобретает полноценное предоперационное обследование, которое должно обязательно включать, например, определение уровней гастрина в сыворотке крови, чтобы не пропустить синдром Золлингера-Эллисона. Например, самой простой операцией при пептической язве является трансторакальная ваготомия. Она эффективно снижает желудочную секрецию и способствует быстрейшему заживлению язвы. Но эта операция не позволяет выполнить необходимое корригирующее вмешательство на органах брюшной полости, например, при вторичном синдроме приводящей петли за счет пептической язвы или при сопутствующем демпинг-синдроме.
Ререзекция культи желудка необязательна, если она маленькая – в таких случаях ваготомия (и, если нужно, удаление оставленного антрального отдела) оказывает быстрый и стойкий лечебный эффект. Удаление самой язвы принципиально необязательно, но вопрос этот в каждом конкретном случае решается индивидуально – при большой пенетрирующей язве, резко деформирующей и стенозирующей зону анастомоза, лучше выполнить ререзекцию, хотя мобилизация культи желудка в таких условиях всегда достаточно сложна. Кроме того, нельзя полностью исключить опасность возникновения кровотечения из оставленной язвы в ближайшем послеоперационном периоде.
При большой желудочной культе (после экономной резекции 1/2 желудка или антрумэктомии) необходима ререзекция культи желудка. Но если предыдущая операция сделана по первому способу Бильрота, можно ограничиться ваготомией. Необходимо отметить, что после резекции по Бильрот I пептические язвы бывают гораздо реже, чем после резекции по Бильрот II, но протекают также тяжело, с пенетрацией, повторными кровотечениями и выраженным болевым синдромом. Если делать при них ререзекцию, могут возникнуть те же трудности с обработкой двенадцатиперстной кишки, как и при низких пенетрирующих дуоденальных язвах. В таких ситуациях селективная проксимальная ваготомия (СПВ) является методом выбора.
Гастрэктомия остается методом выбора при синдроме Золлингера-Эллисона. При выявлении синдрома Золлингера-Эллисона у больного с дуоденальной язвой в настоящее время большинство хирургов склоняются к более консервативному подходу. Предлагается два основных хирургических метода: 1–лечение блокаторами желудочной секреции, затем резекция желудка в сочетании с ваготомией, затем опять длительное, иногда пожизненное лечение блокаторами Н2-рецепторов; 2–сначала лечение блокаторами Н2-рецепторов, затем СПВ, затем снова блокаторы Н2-рецепторов. При обнаружении солитарной аденомы все предпочитают ее удалять.
Пептические язвы при гиперпаратиреоидизме и синдроме Вермера должны лечиться иссечением гормонально-активных тканей (паратиреоидэктомия или субтотальная резекция паращитовидных желез).
Наиболее тяжелые ситуации встречаются при осложнении пептической язвы перфорацией или профузным кровотечением. Естественное желание быстрее завершить экстренную операцию может приводить к техническим ошибкам. Конечно, в условиях выраженного спаечного процесса, пенетрации язвы и при тяжелом общем состоянии больного делать реконструктивную ререзекцию не стоит. Методом выбора в таких случаях являются ушивание язвы и стволовая ваготомия. После выведения больного из тяжелого состояния его необходимо полноценно обследовать и решить вопрос о дальнейшем лечении, возможно, о новой реконструктивной операции [1].
Нами проведен анализ историй болезней 5 больных с диагнозом пептическая язва желудочно-кишечного анастомоза, госпитализированных в отделении хирургической гастроэнтерологии клинической больницы N 3 г. Еревана с апреля 1987г. по август 2000г. Все больные – мужчины в возрасте от 35 до 54 лет. У 2 больных пептическая язва анастомоза была осложнена кровотечением, а у одного больного имелись синдром приводящей петли и желчнокаменная болезнь. Больные перенесли резекцию желудка по Бильрот II по поводу язвенной болезни двенадцатиперстной кишки (3 больных) или желудка (2 больных). Больные предъявляли следующие жалобы: боли в эпигастральной области (5 больных), тошнота (3), рвота (3), чувство дискомфорта в животе (3), общая слабость (2), отрыжка (1), боль в правом подреберье (1 больной). У больных с кровоточащей пептической язвой анастомоза была боль в эпигастральной области, общая слабость, тошнота, рвота кофейной гущей, дегтеобразный стул, чувство дискомфорта в животе. Вышеуказанные жалобы у больных появились от 4 месяцев до 8 лет после резекции желудка по Бильрот II.
Пептическая язва анастомоза у больных была установлена эндоскопически, в течение нескольних часов с момента поступления в клинику. При эзофагогастродуоденоскопии (ЭГДС) у больных с пептической язвой на стенке анастомозированной петли тонкой кишки были обнаружены язвы величиной 0,3-2,5см. В одном случае при эндоскопии был выявлен рефлюкс желчи из приводящей петли тонкой кишки в культю желудка. Все больные получили консервативное лечение, некоторые отказались от предложенной операции и были выписаны из стационара с улучшением в сроки от 2 до 24 дней.
Таким образом, ЭГДС является наиболее достоверным способом диагностики пептической язвы анастомоза. Эндоскопическое исследование дает возможность также с достоверностью судить о размерах культи желудка, т. е. в ряде случаев выявляет причину возникновения пептической язвы.
Литература
- Черноусов А.Ф., Богопольский П.М., Курбанов Ф.С. Хирургия язвенной болезни желудка и двенадцатиперстной кишки. М., 1996, с. 202-208.
- Christiansen S., Ram M., Sachatello C., Griffen W. Management of gastrocolic fistula. Am. Surg. 1981; 47. p. 63-66.
- Glasgow R.E., Mulvihill S.J. Postgastrectomy syndromes. 1997, p. 149-150.



