Диссеминированный рак желудка что это

Пациент: больная К., рак желудка с метастазами
Возраст: 45 лет
28.10.2002 г. больная поступила в клинику с диагнозом рак желудка (пилорического отдела) T4N3M1, осложненный декомпенсированным стенозом, метастазы в яичники, лимфоузлы брюшной полости и забрюшинного пространства.
Из анамнеза: в 2002 году отметила прогрессирующее снижение веса на 19 кг. В августе 2002 года у больной выявлен рак желудка (пилорического отдела) T4N3M1, осложненный декомпенсированным стенозом, метастазы в яичники, лимфоузлы брюшной полости и забрюшинного пространства.
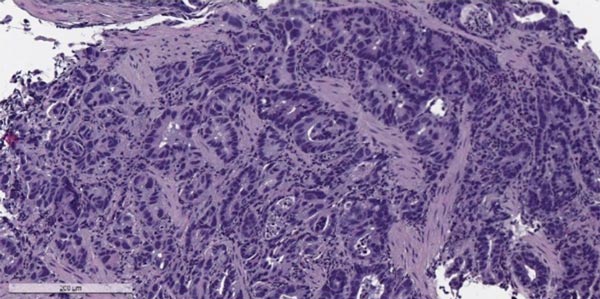
Цитология № 7751/53 – низкодифференцированная аденокарцинома желудка.
10.09.2002 г. произведена операция – лапаротомия, ревизия органов брюшной полости. Наложение переднего впередиободочного гастроэнтероанастомоза с анастомозом Брауна. Проведение полихимиотерапии не планировалось, учитывая большую распространенность опухоли и низкую эффективность химиотерапии.
При поступлении в клинику “К-тест” состояние удовлетворительное, ослабленное, определяется асцит. При рентгеноскопии подтвержден рак дистальной половины желудка с метастазами. На КТ определяется асцит, двусторонний плеврит, увеличение отдельных забрюшинных лимфоузлов до 10 мм (рис. 3а). При ультразвуковом исследовании в малом тазу лоцируется метастаз Крукенберга размером 50 × 40 мм.
30.10.2002 г. проведен первый сеанс общей гипертермии с полихимиотерапией (5-фторурацил, лейковорин, доксорубицин). Максимальная температура составила 42,45 °С. В постгипертермическом периоде отмечалась транзиторная гипербилирубинемия (49,6 ммоль/л).
Повторно больная поступила в клинику 02.12.2002 г. через 4 недели после первого сеанса гипертермии. Состояние при поступлении удовлетворительное, жалоб нет, прибавила в весе 3 кг. При ультразвуковом исследовании органов малого таза отмечено уменьшение размеров метастазов в яичниках до 45 × 35 мм, что соответствует стабилизации.
05.12.2002 г. проведен второй сеанс общей гипертермии с полихимиотерапией, максимальная температура составила 42,58 °С. Постгипертермический период протекал гладко, и больная была выписана в удовлетворительном состоянии на пятые сутки после сеанса гипертермии.
Обследована в январе 2003 года через 1 месяц после второго сеанса общей гипертермии. При КТ брюшной полости асцита, плеврита и увеличения забрюшинных лимфоузлов не отмечается (рис. 3б). При ультразвуковом исследовании размеры яичников уменьшились до 30 × 28 мм, что соответствует частичной регрессии.
В марте 2003 года больная чувствует себя удовлетворительно, за период с октября 2002 года по март 2003 года прибавила в весе 16 кг, ремиссия сохраняется.
Оперативное лечение рака желудка с метастазами стало возможным
Учитывая выраженный клинический эффект, достигнутый после двух сеансов общей гипертермии с полихимиотерапией, 22.04.2003 г. выполнена операция – верхне-срединная лапаротомия: в брюшной полости – спаечный процесс, по всей брюшной полости – разрастание фиброзной ткани, метастазы в оба яичника. Выполнена субтотальная резекция желудка по Ру, резекция обоих яичников. Гистологически: в желудке – на фоне выраженного фиброза, эластоза единичные рассеянные комплексы атипичных клеток с гиперхроматозом и пикнозом ядер. Картина терапевтического патоморфоза III степени по Г.А. Лавниковой. В обоих яичниках на фоне фибротекоматоза и фиброза – комплексы опухолевых клеток с «целлюлярными» очагами некроза, пикнозом и рексисом ядер. Заключение: рак желудка (малодифференцированная аденокарцинома) с термохимиотерапевтическим патоморфозом III степени. Метастатическое поражение обоих яичников с терапевтическим регрессом.
Данный пример показывает возможность достижения частичной регрессии при использовании общей гипертермии у больной диссеминированным раком желудка. В приведенном примере объективный эффект был получен после второго сеанса общей гипертермии с полихимиотерапией, что дало возможность выполнить радикальную операцию.
Ист. болезни: 526/586
© 2020 Онкологическая клиника «К-тест» · Копирование материалов запрещено. *Цены, указанные на сайте, не являются офертой. Стоимость услуг устанавливается и оплачивается согласно прейскуранту Клиники, действующему на момент оказания услуги. Подробности по тел.8 (831) 439-15-14. Имеются противопоказания. Необходима консультация специалиста. Лицензия ЛО-52-01-005717 от 16.02.2017. ОГРН 1025203029763. ИНН 5260013184
Опубликовано: 21 мая 2015 в 10:09
 Среди онкологических заболеваний тотальный рак желудка занимает одно из первых мест в «черном» списке. От этой патологии страдает сотни тысяч человек, и, к сожалению, зачастую исход болезни летальный. Лучшие специалисты тратят силы, крупные средства для поиска панацеи от смертоносного недуга.
Среди онкологических заболеваний тотальный рак желудка занимает одно из первых мест в «черном» списке. От этой патологии страдает сотни тысяч человек, и, к сожалению, зачастую исход болезни летальный. Лучшие специалисты тратят силы, крупные средства для поиска панацеи от смертоносного недуга.
При тотальном раке желудка различают несколько типов: экзофитный, эндофитный и смешанный. В первом случае новообразование имеет форму бляшки, гриба, полипа и выступает наружу органа с четко выраженным очертанием. Второй тип относится к более опасным видам и процент выживаемости довольно низок. Опухоль прорастает внутрь полости желудка и распространяется на весь орган по его поверхности. Смешанный тип сочетает в себе экзофитный и эндофитный рак и считается самым злокачественным образованием. К сожалению, прогнозы в данном случае неутешительны.
Симптомы тотального рака желудка
Раковые заболевания в начальной стадии проходят незаметно, в чем и заключается проблема преждевременного выявления онкологии. Только у 5% пациентов на ранних стадиях ощущают приступы тошноты, рвоты, отрыжки. Остальная часть не чувствует никакого дискомфорта. Именно по этой причине следует проходить профилактические проверки всего организма со сдачей онкомаркеров каждые полгода – год. Также на начальных стадиях тотального рака у 75% присутствует болевой синдром. 15% больных чувствует дисфагию, то есть проблемы с глотанием, воспалительные процессы в пищеводе, попадание пищи в ротовую полость, в нос, сухость дыхания.
Рак желудка с распадом
 Одним из самых тревожных симптомов при онкологическом заболевании желудка является перфорация органа. На стенках образуется перфорация, через которую поглощенная пища или желудочный сок проникает в полость живота. У больного развивается воспаление, отравление и причиняет острую боль, рвоту, тошноту. Врачи называют такое состояние термином «острый живот» и в таких случаях следует немедленно вызывать неотложку и прибегнуть к помощи квалифицированных специалистов. Также при онкологии с распадом доктора настоятельно рекомендуют не пользоваться обезболивающими средствами, так как временное снятие боли приведет к более тяжелым последствиям.
Одним из самых тревожных симптомов при онкологическом заболевании желудка является перфорация органа. На стенках образуется перфорация, через которую поглощенная пища или желудочный сок проникает в полость живота. У больного развивается воспаление, отравление и причиняет острую боль, рвоту, тошноту. Врачи называют такое состояние термином «острый живот» и в таких случаях следует немедленно вызывать неотложку и прибегнуть к помощи квалифицированных специалистов. Также при онкологии с распадом доктора настоятельно рекомендуют не пользоваться обезболивающими средствами, так как временное снятие боли приведет к более тяжелым последствиям.
Диссеминированный рак желудка
 Диссеминированный рак может распространяться на другие органы брюшной полости, на почки, печень, и другие системы. Опасность данного вида онкологического заболевания заключается в его быстром прорастании метастаз на другие органы организма. Любой вид поражения может сопровождаться мощным «выбросом» токсичных клеток и распространятся на всю полость пораженного органа. Вследствие воздействия тотального рака происходит распад органа, то есть обрыв желудка на несколько и более фрагментов.
Диссеминированный рак может распространяться на другие органы брюшной полости, на почки, печень, и другие системы. Опасность данного вида онкологического заболевания заключается в его быстром прорастании метастаз на другие органы организма. Любой вид поражения может сопровождаться мощным «выбросом» токсичных клеток и распространятся на всю полость пораженного органа. Вследствие воздействия тотального рака происходит распад органа, то есть обрыв желудка на несколько и более фрагментов.
Обширный рак желудка
 Обширный рак желудка включает в себя различные типы онкологических новообразований: экзофитный, эндофитный, опухоли с метастазами в другие органы брюшной полости. Данный тип заболевания сопряжен с большими трудностями при лечении. Болезнь выявляется на поздних стадиях.
Обширный рак желудка включает в себя различные типы онкологических новообразований: экзофитный, эндофитный, опухоли с метастазами в другие органы брюшной полости. Данный тип заболевания сопряжен с большими трудностями при лечении. Болезнь выявляется на поздних стадиях.
Опытные специалисты, ведущие онкологи всего мира настоятельно рекомендуют проходить тщательное обследование организма как минимум каждые полгода. В то же время, для профилактики онкологических и других видов заболеваний, для поднятия иммунитета, укрепление общего состояния организма следует вести здоровый образ жизни, отказаться от алкогольных напитков, курения. Ежедневные прогулки по свежему воздуху, здоровое питание, крепкий сон, обход стрессовых ситуаций – прямой путь к одолению серьезных заболеваний, в том числе и тотальных.
В статье представлены результаты клинического наблюдения за больным диссеминированным раком желудка. Химиотерапия оказалась эффективной и позволила достичь полной регрессии отдаленных метастазов и длительной ремиссии болезни. От предложенного хирургического лечения пациент отказался, в связи с чем ему была продолжена поддерживающая химиотерапия в течение 18 месяцев. Спустя два года после ее завершения зарегистрировано прогрессирование болезни в виде метастазов в легких, лимфатических узлах средостения. Химиотерапия была возобновлена. Продолжительность жизни больного к сентябрю 2016 г. составила 57 месяцев, выживаемость без прогрессирования болезни на первой линии химиотерапии – 48 месяцев, длительность частичной ремиссии – 46 месяцев. На фоне возобновления трехкомпонентного режима первой линии в современной модификации в качестве терапии второй линии также была достигнута и подтверждена частичная регрессия опухоли. Продолжительность жизни пациента с момента начала химиотерапии второй линии превышает девять месяцев.
Введение
Рак желудка занимает лидирующие позиции в структуре онкологической заболеваемости и смертности как в России, так и за рубежом. Ежегодно в мире выявляют свыше 1 млн новых случаев заболевания, около 700 000 больных умирают [1]. В России рак желудка на протяжении многих лет занимает второе место в структуре смертности от онкологических заболеваний [2].
Согласно статистике, на момент установления диагноза операбельный процесс выявляется лишь у 20% пациентов, более чем у половины больных отмечаются отдаленные метастазы.
Тактика лечения
В настоящее время стандартным методом лечения больных диссеминированным раком желудка является лекарственная терапия. Химиотерапия позволяет увеличить продолжительность жизни до одного года при выживаемости без прогрессирования заболевания до шести месяцев и более, а также устранить или облегчить симптомы, связанные с опухолью, и тем самым улучшить качество жизни пациентов [3]. Сравнительный анализ эффективности двух- и трехкомпонентных режимов химиотерапии показал статистически достоверное увеличение продолжительности жизни больных при использовании трехкомпонентных комбинаций [4, 5].
Одной из наиболее эффективных схем химиотерапии при диссеминированном раке желудка признана комбинация DCF (доцетаксел + цисплатин + 5-фторурацил (5-ФУ) в режиме суточных инфузий) [6]. Однако ее применение ограничено высокой токсичностью. Так, нейтропения 3–4-й степени наблюдается у 82% больных, в том числе у 29% лечение сопровождается фебрильной лихорадкой.
С 1996 г. в отделении химиотерапии РОНЦ им. Н.Н. Блохина было начато изучение эффективности и токсичности доцетаксела в составе трехкомпонентных режимов в качестве первой линии химиотерапии при неоперабельном раке желудка. Первая изучаемая оригинальная комбинация включала Таксотер 75 мг/м² во второй день, цисплатин 75 мг/м² во второй день, 5-ФУ по 500 мг/м² в виде трехчасовой инфузии в первый – третий дни (режим TPF) [7–9]. В одной из последующих модификаций режима цисплатин был заменен на оксалиплатин. Химиотерапию по схеме «Таксотер 75 мг/м2 во второй день, Элоксатин 100 мг/м2 во второй день, лейковорин 50 мг внутривенно струйно с последующим введением 5-ФУ в дозе 500 мг/м2 внутривенно капельно в течение трех часов в первый, второй, третий дни каждые 21 день (TOFL)» получили 39 пациентов. Объективный эффект зарегистрирован у 19 (48,7%) больных, стабилизация болезни – у 14 (35,9%), прогрессирование заболевания – у шести (15,4%). Медиана выживаемости без прогрессирования составила 6,5 месяца, медиана общей продолжительности жизни – 14,9 месяца. Токсичность режима TОFL была умеренной.
Полная регрессия отдаленных метастазов зафиксирована у трех пациентов. Двум из них после достижения полной регрессии отдаленных метастазов по брюшине была выполнена паллиативная операция в объеме гастрэктомии с лимфодиссекцией D2. Продолжительность жизни этих пациентов составила 16 и более 31 месяца. Третий пациент после констатации полной регрессии отдаленных метастазов от хирургического лечения отказался, и ему была продолжена поддерживающая химиотерапия. Приводим выписку из его истории болезни.
Клинический случай
Больной М. 53 лет обратился в РОНЦ им. Н.Н. Блохина в ноябре 2011 г. с жалобами на нарушение прохождения пищи по пищеводу (дисфагия 2-й степени), снижение веса на 10 кг в течение пяти месяцев.
При эзофагогастродуоденоскопии (ЭГДС) выявлена бугристая опухоль, исходящая из желудка, распространяющаяся на пищевод, с проксимальной границей инфильтрации на уровне 35 см от резцов. Опухоль циркулярно охватывала стенки пищевода, деформируя и суживая его просвет до 1 см. Эндоскоп с трудом был введен в желудок, где на уровне субкардиального отдела визуализирована дистальная граница опухоли. Розетка кардии циркулярно занята изъязвленной опухолью, стенки ригидные, несмыкаемые. Гистологическое заключение: аденокарцинома.
Ультразвуковое исследование (УЗИ) органов брюшной полости и забрюшинного пространства показало наличие множественных метастатически измененных лимфатических узлов в забрюшинном пространстве от уровня эпигастрия до бифуркации аорты размером 3,8 × 1,5 см. В шейно-надключичной области слева визуализировались множественные лимфатические узлы до 1,7 × 1,3 см (метастазы), справа – до 1,2 × 0,5 см.
Результаты магнитно-резонансной томографии брюшной полости: конгломерат увеличенных парагастральных лимфатических узлов общим размером до 5,5 × 4,5 см, увеличенные парааортальные, паракавальные и аортокавальные лимфатические узлы размером до 3,5 см. Утолщение стенок желудка. Асцит отсутствовал.
Диагностирован рак проксимального отдела желудка с переходом на пищевод (аденокарцинома) с метастазами в надключичные лимфатические узлы слева, забрюшинные лимфатические узлы, стадия IV, сTхNxM1.
Сопутствующие заболевания отсутствовали.
С декабря 2011 г. по май 2012 г. проведено восемь курсов химиотерапии по схеме TOFL: доцетаксел 75 мг/м² во второй день + оксалиплатин 100 мг/м² во второй день + лейковорин 50 мг внутривенно струйно в первый – третий дни + 5-ФУ 500 мг/м² в первый – третий дни в виде трехчасовой инфузии. Значимых побочных явлений в ходе лечения не зарегистрировано.
На фоне терапии жалобы на дисфагию полностью исчезли после первого курса, пациент начал прибавлять в весе. При контрольном обследовании после трех курсов отмечалась выраженная положительная динамика. По данным УЗИ перестали определяться забрюшинные и шейно-надключичные лимфатические узлы с обеих сторон. При ЭГДС в пищеводе на уровне 35 см от резцов по заднеправой полуокружности обнаружено плоское изъязвление с подрытыми относительно мягкими краями, от которого плоский инфильтрат в виде продольного участка распространялся до кардии и далее до границы с субкардией. Розетка кардии была эластичная, свободно проходима. Просвет пищевода на уровне опухоли расширился, стенки стали эластичными. При ретрофлексионном осмотре выявлен небольшой участок опухолевой инфильтрации субкардии по задней стенке.
По окончании трех курсов лечения зарегистрирована частичная регрессия опухоли с полной регрессией забрюшинных и надключичных лимфатических узлов. Пациент продолжал получать химиотерапию по прежней схеме.
При обследовании по окончании шести курсов химиотерапии данных о наличии отдаленных метастазов при УЗИ не получено, что было подтверждено результатами компьютерной томографии (КТ) брюшной полости. Данные ЭГДС также подтвердили частичную регрессию опухоли.
В связи с нарастающей положительной динамикой было решено провести еще два курса химиотерапии по прежней схеме.
После завершения восьми курсов химиотерапии при ЭГДС в нижнегрудном отделе пищевода визуализировалась опухоль, которая занимала половину окружности стенки пищевода и половину диаметра просвета за счет экзофитного компонента. Дистальный край опухоли лоцировался на уровне 38 см от резцов, дистальнее на 2 см определялась плоская овальная язва 0,6 × 0,4 см, с выраженной краевой эпителизацией, без признаков неопластической перестройки. Розетка кардии располагалась на уровне диафрагмального сужения (41 см), эластичная, слизистая оболочка в зоне кардии не инфильтрирована.
Таким образом, после восьми курсов химиотерапии, по данным УЗИ и КТ, зарегистрированы полная регрессия отдаленных метастазов и значительное уменьшение первичной опухоли.
Для уточнения распространенности процесса с последующим выбором лечебной тактики на консилиуме с участием хирургов пациенту предложили проведение лапароскопии. Однако и от лапароскопии, и от оперативного лечения он категорически отказался, в связи с чем ему назначили поддерживающую химиотерапию лейковорином по 50 мг внутривенно струйно в первый – третий дни в комбинации с 5-ФУ по 500 мг/м² в виде трехчасовой инфузии в первый – третий дни каждые 21–28 дней. С июня 2012 г. по декабрь 2013 г. проведено 20 курсов поддерживающей химиотерапии на фоне регулярного контрольного обследования каждые три курса.
При регулярном УЗИ периферических лимфоузлов, органов брюшной полости, забрюшинного пространства и таза в процессе поддерживающего лечения данных о метастазировании процесса не получено. При ЭГДС определялось лишь изъязвление в пищеводе на уровне 36 см от резцов размером от 0,5 до 1 см. При неоднократной биопсии слизистой оболочки в зоне изъязвления с последующим морфологическим исследованием биоптатов элементы опухоли не обнаружены. С января 2014 г. больному рекомендовано динамическое наблюдение.
В декабре 2015 г. во время очередного планового обследования при рентгеновской КТ грудной клетки в базальных отделах S2 верхней доли левого легкого у главной междолевой плевры выявлено узловое образование с бугристыми контурами диаметром 1,6 см. Паратрахеально справа определялись лимфатические узлы до 1,2 см в диаметре, паравазально и в аортопульмональном окне – множественные лимфоузлы до 0,9 см, в области бифуркации трахеи – конгломерат лимфатических узлов до 4,3 × 2,7 см. Корень левого легкого несколько расширен, в нем также определялись увеличенные лимфатические узлы размером до 1,5 см. Результаты рентгеновской КТ: метастатическое поражение легкого, лимфатических узлов средостения и корня легкого. При ЭГДС динамики не зафиксировано, по-прежнему по задней полуокружности в области кардиоэзофагеального перехода определялось изъязвление, при гистологическом исследовании биопсийного материала – лейкоцитарно-некротические массы и мелкий кусочек грануляционной ткани.
Изменения, выявленные при рентгеновской КТ органов грудной клетки, были расценены как метастатические, констатировано прогрессирование рака желудка и возобновлена химиотерапия по схеме FLOT в виде реиндукции.
С декабря 2015 г. по апрель 2016 г. проведено девять курсов химиотерапии. Лечение больной переносил удовлетворительно.
При обследовании после шестого курса зарегистрирована частичная регрессия опухоли: образование в базальных отделах S2 верхней доли левого легкого практически перестало определяться (на его месте сохранялось небольшое уплотнение легочной ткани). Конгломерат лимфатических узлов в области бифуркации трахеи уменьшился вдвое: с 4,3 × 2,7 см до 2,2 × 1,1 см. Лимфатические узлы средостения уменьшились на 50%, лимфатические узлы корня левого легкого – с 1,5 см до 0,8 см.
При обследовании после девяти курсов химиотерапии в мае 2016 г. частичная регрессия сохранялась. Пациенту рекомендовано динамическое наблюдение.
Таким образом, в результате химиотерапии доцетакселом, оксалиплатином и 5-ФУ продолжительность жизни больного исходно диссеминированным раком желудка к сентябрю 2016 г. составила 57 месяцев, выживаемость без прогрессирования заболевания на первой линии химиотерапии – 48 месяцев, длительность частичной ремиссии – 46 месяцев. Эффективным оказалось и возобновление трехкомпонентного режима первой линии в современной модификации в качестве терапии второй линии, на фоне которой также была достигнута и подтверждена частичная регрессия опухоли. Продолжительность жизни пациента с момента начала химиотерапии второй линии превышает девять месяцев.
Заключение
К сожалению, на современном этапе развития медицины мы не можем спрогнозировать ни эффективность определенного режима химиотерапии у конкретного больного диссеминированным раком желудка, ни вероятность достижения длительной ремиссии. Выбор химиотерапии обычно осуществляется эмпирически. Однако появление эффективных режимов химиотерапии при диссеминированной аденокарциноме желудка или кардиоэзофагеального перехода позволило существенно улучшить результаты лечения данной категории пациентов.
Представленное клиническое наблюдение демонстрирует возможность достижения длительной ремиссии на фоне применения современной трехкомпонентной химиотерапии с включением доцетаксела и оксалиплатина, а также ставит перед врачами новые тактические вопросы. Одним из них является вопрос о целесообразности подключения хирургического лечения в случае полной регрессии отдаленных метастазов на фоне эффективной химиотерапии.
Данное наблюдение свидетельствует также о том, что при прогрессировании диссеминированного рака желудка после длительной ремиссии целесообразна реиндукция той же схемы химиотерапии, при использовании которой был получен первый выраженный эффект.