Атрезия желчного пузыря это


Атрезия желчных ходов – аномалия развития желчевыводящих путей, выражающаяся в нарушении проходимости внутрипеченочных или/и внепеченочных желчных протоков. Атрезия желчных ходов проявляется упорной желтухой, обесцвечиванием испражнений, интенсивной темной окраской мочи, увеличением печени и селезенки, развитием портальной гипертензии, асцитом. Атрезия желчных ходов распознается с помощью УЗИ, холангиографии, сцинтиграфии, лапароскопии, биохимических проб, пункционной биопсии печени. При атрезии желчных ходов показано оперативное лечение (гепатико-, холедохоеюностомия, портоэнтеростомия).
Общие сведения
Атрезия желчных ходов (билиарная атрезия) – тяжелый врожденный порок развития, характеризующийся частичной или полной облитерацией просвета желчных ходов. Атрезия желчных ходов встречается в педиатрии и детской хирургии примерно в 1 случае на 20000-30000 родов, составляя около 8% всех пороков внутренних органов у детей. Атрезия желчных ходов представляет собой крайне опасное состояние, требующее раннего выявления и безотлагательного оперативного лечения. Без оказания своевременной хирургической помощи дети с атрезией желчных ходов погибают в течение первых месяцев жизни от пищеводного кровотечения, печеночной недостаточности или инфекционных осложнений.

Атрезия желчных ходов
Причины атрезии желчных ходов
Причины и патогенез атрезия желчных ходов до конца не ясны. В большинстве случаев при атрезии желчные протоки сформированы, однако их проходимость нарушена вследствие облитерации или прогрессирующей деструкции. Чаще всего причиной обстуктивной холангиопатии становятся внутриутробные инфекции (герпес, краснуха, цитомегалия и др.) или неонатальный гепатит. Воспалительный процесс вызывает повреждение гепатоцитов, эндотелия желчных ходов с последующим внутриклеточным холестазом и фиброзом желчных ходов. Реже атрезия желчных ходов связана с ишемией протоков. В этих случаях атрезия желчных ходов не обязательно будет носить врожденный характер, а может развиваться в перинатальном периоде вследствие прогрессирующего воспалительного процесса.
Истинная атрезия желчных ходов выявляется реже и связана с нарушением первичной закладки желчных путей в эмбриональном периоде. При этом в случае нарушения закладки печеночного дивертикула или канализации дистальных отделов желчевыводящей системы развивается атрезия внутрипеченочных желчных ходов, а при нарушении формирования проксимальных отделов желчевыводящей системы — атрезия внепеченочных желчных протоков. Желчный пузырь может являться единственным звеном наружных желчевыводящих путей или отсутствовать полностью.
Примерно у 20% детей атрезия желчных ходов сочетается с другими аномалиями развития: врожденными пороками сердца, незавершенным поворотом кишечника, аспленией или полиспленией.
Классификация атрезии желчных ходов
К аномалиям развития желчевыводящих путей относятся следующие клинико-морфологические формы: гипоплазия, атрезия, нарушение ветвления и слияния, кистозные изменения желчных ходов, аномалии холедоха (киста, стеноз, перфорация).
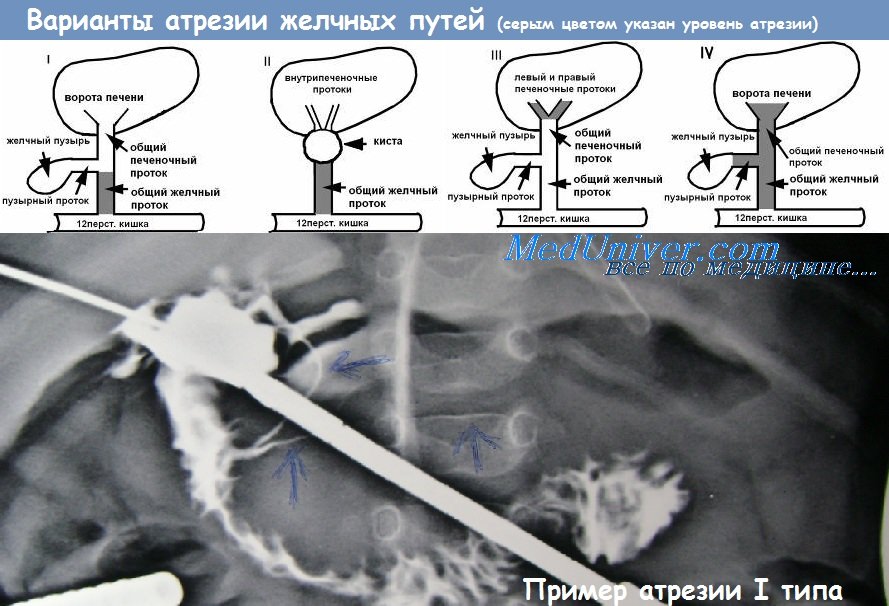
По локализации различают внепеченочную, внутрипеченочную и тотальную (смешанную) атрезию желчных ходов. С учетом места обструкции желчных протоков выделяют корригируемую атрезию желчных ходов (непроходимость общего желчного или общего печеночного протока) и некорригируемую атрезию желчных ходов (полное замещение протоков в воротах печени фиброзной тканью). Локализация и уровень обструкции желчных протоков являются определяющими факторами, влияющими на выбор техники хирургического вмешательства.
Симптомы атрезии желчных ходов
Дети с атрезией желчных ходов обычно рождаются доношенными с нормальными антропометрическими показателями. На 3-4-е сутки жизни у них развивается желтуха, однако в отличие от транзиторной гипербилирубинемии новорожденных, желтуха при атрезии желчных ходов сохраняется длительно и постепенно нарастает, придавая кожным покровам ребенка шафрановый или зеленоватый оттенок. Обычно атрезия желчных ходов не распознается в первые дни жизни ребенка, и новорожденный выписывается из роддома с диагнозом «затянувшаяся физиологическая желтуха».
Характерными признаками атрезии желчных ходов, присутствующими с первых дней жизни ребенка, служат ахоличный (обесцвеченный) стул и моча интенсивного темного («пивного») цвета. Сохранение обесцвеченного кала в течение 10 дней указывает на атрезию желчных ходов.
К исходу первого месяца жизни нарастает снижение аппетита, дефицит массы, адинамия, кожный зуд, задержка физического развития. В это же время отмечается увеличение печени, а затем – селезенки. Гепатомегалия является следствием холестатического гепатита, на фоне которого быстро развивается билиарный цирроз печени, асцит, а к 4-5 месяцам — печеночная недостаточность. Нарушение кровоснабжения печени способствует формированию портальной гипертензии и, как следствие, — варикозному расширению вен пищевода, спленомегалии, появлению подкожной венозной сети на передней брюшной стенке. У детей с атрезией желчных ходов отмечается геморрагический синдром: мелкоточечные или обширные кровоизлияния на коже, кровотечения из пуповинного остатка, пищеводные или желудочно-кишечные кровотечения.
При отсутствии своевременного хирургического лечения дети с атрезией желчных ходов обычно не доживают до 1 года, погибая от печеночной недостаточности, кровотечений, присоединившейся пневмонии, сердечно-сосудистой недостаточности, интеркурентных инфекций. При неполной атрезии желчных ходов некоторые дети могут дожить до 10 лет.
Диагностика атрезии желчных ходов
Крайне важно, чтобы атрезия желчных ходов была выявлена неонатологом или педиатром как можно раньше. Персистирующая желтуха и ахоличный стул должны навести детских специалистов на мысль о наличии у ребенка атрезии желчных ходов и заставить предпринять необходимые меры к уточнению диагноза.
Уже с первых дней жизни в крови новорожденного нарастают уровни биохимических маркеров печени, прежде всего, билирубина (вначале за счет увеличения прямой фракции, позже – за счет преобладания непрямого билирубина), щелочной фосфатазы, гамма-глютамил-трансферазы. Постепенно развивается анемия и тромбоцитопения, снижается ПТИ. При атрезии желчных ходов в кале ребенка отсутствует стеркобилин.
УЗИ печени, селезенки и желчных путей позволяет оценить размеры органов и структуру паренхимы, состояние желчного пузыря, вне- и внутрипеченочных желчных протоков, воротной вены. Обычно при атрезии желчных ходов желчный пузырь не определяется или визуализируется в виде тяжа, также не выявляется общий желчный проток. Информативными методами для уточнения диагноза служат чрескожная чреспеченочная холангиография, МР-холангиография, статическая сцинтиграфия печени, динамическая сцинтиграфия гепатобилиарной системы.
Окончательное подтверждение атрезии желчных ходов может быть достигнуто при выполнении диагностической лапароскопии, интраоперационной холангиографии, биопсии печени. Морфологическое исследование биоптата способствует уточнению характера поражения гепатоцитов и состояния внутрипеченочных желчных протоков.
Атрезию желчных ходов у детей следует дифференцировать с желтухой новорожденных, врожденным гигантоклеточным гепатитом, механической закупоркой желчных путей слизистыми или желчными пробками.
Лечение атрезии желчных ходов
Важным условием успешности лечения атрезии желчных ходов является проведение хирургического вмешательства в возрасте до 2-3-х месяцев, поскольку в более старшем возрасте операция, как правило, безуспешна из-за необратимых изменений.
В случае непроходимости общего желчного или печеночного протоков и наличия супрастенического расширения производится наложение холедохоэнтероанастомоза (холедохоеюностомия) или гепатикоеюноанастомоза (гепатикоеюностомия) с петлей тощей кишки. Полная атрезия внепеченочных желчных ходов диктует необходимость выполнения портоэнтеростомии по Касаи – наложения анастомоза между воротами печени и тонкой кишкой. Наиболее частыми послеоперационными осложнениями служат послеоперационный холангит, абсцессы печени.
При выраженной портальной гипертензии и рецидивирующих гастроинтестинальных кровотечениях может быть проведено портокавальное шунтирование. В случае прогрессирующей печеночной недостаточности и гиперспленизма решается вопрос о трансплантации печени.
Прогноз атрезии желчных ходов
В целом прогноз атрезии желчных ходов очень серьезный, поскольку цирротические изменения печени носят прогрессирующий характер. Без хирургической помощи дети обречены на гибель в течение 12-18 месяцев.
Очень важно выявить клинические проявления атрезии желчных ходов (упорную желтуху, ахоличный кал) в неонатальном периоде и провести раннее хирургическое лечение. В большинстве случаев наложение холедоходигестивных анастомозов или печеночных анастомозов способно продлить жизнь ребенка на несколько лет и отсрочить необходимость трансплантации печени.
Атрезия желчных ходов, она же билиарная атрезия желчевыводящих путей, представляет собой редкую болезнь, вызванную перекрытием желчных протоков внутри и снаружи печени. Встречается у 1 новорожденного на каждые 20-30 тыс. При отсутствии необходимого лечения прогноз врачей однозначен – летальный исход в течение 1-2 лет.
Симптомы
На 3-4-й день жизни новорожденного родители отмечают пожелтение его кожи, стул неестественного светлого цвета, а моча – очень темная. На свет такие дети появляются доношенными, без заметных отклонений в росте и весе. Случается, что грудничков выписывают из роддома, не установив правильный диагноз. В их медицинской карте указывают затянувшуюся физиологическую желтуху.
Однако дома тревожные симптомы не проходят, постепенно кожа желтеет все сильнее, приобретая красноватый или зеленоватый тон. Сохранение в течение 10 суток подряд обесцвеченного оттенка кала однозначно указывает на наличие атрезии желчевыводящих путей.
Развитие болезни к окончанию 1-го месяца жизни проявляется в стойком снижении аппетита, нехватке веса, кожном зуде, вялости и малоподвижности ребенка. Он начинает отставать в развитии от сверстников. Становится хорошо заметным увеличение печени и селезенки, которое возникает из-за холестатического гепатита.
В дальнейшем у малыша может развиться билиарный цирроз печеночных тканей. К 4-5 месяцам жизни в полной мере проявится печеночная недостаточность.
Печень снабжается кровью в аномальном режиме, из-за этого создаются все условия для развития портальной гипертензии. Вены пищевода расширяются, селезенка разрастается в размерах, на животе становится хорошо заметной венозная сетка. У детей с атрезией желчевыводящих путей проявляется геморрагический синдром. На коже в разных местах, особенно на животе, возникают крошечные (точечные) или обширные синяки, из пуповины возобновляется кровотечение, появляется также внутреннее – в пищеводе, желудке, кишечнике.
Без хирургического вмешательства до исполнения первого года жизни летальный исход неизбежен из-за печеночной недостаточности, множественных кровотечений. У младенцев с атрезией желчевыводящих путей появляется сердечная недостаточность, у новорожденных нередко начинается пневмония, присоединяются различные инфекции. Если атрезия неполная, ребенок сможет прожить без операции до 10 лет.
Диагностика
Процесс постановки диагноза начинается с визита к участковому терапевту. Врач проводит осмотр ребенка, выясняет жалобы на состояние его здоровья. После этого выдает направления на сдачу анализов в лабораторию:
- Общий и биохимический анализ крови.
- Коагулограмма.
- Анализ кала.
- ИФА на выявление внутриутробной инфекции.
Помимо этого применяют инструментальные методы диагностики:
- УЗИ печени и желчных протоков, селезенки.
- КТ печени и желчного пузыря.
- Эндоскопическая ретроградная панкреатохолангиография.
- МРТ.
- Холецистохолангиография.
- Биопсия печени.
- ЭКГ – для исключения внутренних пороков и патологии сердца.
При подтверждении результатами исследований предположительного диагноза атрезия ребенка перенаправляют к детскому хирургу, который выписывает направление на госпитализацию.
Для исключения дополнительных патологий рекомендован осмотр пациента детским инфекционистом, гепатологом, кардиологом и невропатологом.
Лечение
После постановки диагноза атрезия ребенок помещается в стационар. Иного выхода, кроме операции, нет. Крайне важно провести ее до 3-месячного возраста. На более запущенной стадии в организме произойдут необратимые изменения внутренних органов и систем.
Цель хирургического вмешательства – обеспечить естественный отток желчи. В местах перекрытия протоков накладывают анастомозы – соединения свободных участков друг с другом. Если требуется, анастомоз накладывают между тонким кишечником и общим желчным протоком или печеночным каналом. Методику создал хирург из Японии М. Касаи, в честь которого и получила название данная группа операций.
Помощь пациенту таким способом можно оказать только до того, как у него разовьется печеночная недостаточность. В противном случае спасти его сможет исключительно пересадка печени.
Своевременно проведенная операция – шанс на здоровую жизнь при условии проведения полноценной послеоперационной восстановительной терапии. На этом этапе назначаются препараты:
- Антибиотики. Их задача – предотвратить послеоперационные осложнения.
- Пробиотики и антимикотики. Они восстанавливают микрофлору кишечника, пострадавшую от антибиотиков, предотвращают присоединение грибковой инфекции.
- Желчегонные средства. С их помощью пищеварительному ферменту легче проходить по освобожденным после операции протокам.
- Гемостатические препараты. Их назначают для профилактики кровотечений.
Дополнительно показано проведение инфузионной терапии для выведения из организма скопившихся токсинов, восполнения кровопотери. Ребенка кормят парентерально: капельно вводят 5%-ный раствор глюкозы с комплексом аминокислот.
Если имеются сопутствующие заболевания, в комплекс восстановительной терапии включают бронхолитики, противовирусные препараты. Пациентам с анемией назначают препараты железа.
Атрезия желчных путей у детей и новорожденных
Все причины, из-за которых у плода развивается билиарная атрезия желчного пузыря, делят на две категории:
- эндогенные – имеющие генетическую природу;
- экзогенные – из-за внутриутробного или перинатального воспалительного процесса.
До конца природа атрезии пока не изучена, но врачи склонны акцентировать внимание на следующих предпосылках:
- Внутриутробная инфекция. В числе патогенных выделяют цитомегаловирус, ОРВИ, герпес, краснуху.
- Аномальное формирование внутренних органов плода в первом триместре беременности. В таких случаях всегда речь идет об истинной атрезии. У плода на 100% отсутствуют желчевыводящие пути, а в самых редких случаях – и желчный пузырь.
- Неонатальный гепатит. Речь о заболевании, которое проявляется у новорожденных в возрасте до 3 месяцев.
- Генные мутации. Обычно в таких случаях только атрезией перечень патологий не ограничивается. Дополнительно могут быть выявлены пороки развития других органов пищеварительного тракта, сердца. У младенца может не быть селезенки либо наблюдаться множественность этого органа.
Иногда причиной атрезии становится воспалительный процесс, развившийся сразу после рождения – не врожденная, а приобретенная патология. До сих пор нет данных о том, существует ли риск развития заболевания у плода из-за приема каких-либо препаратов или вакцинации на том или ином триместре беременности.
Видео
Атрезия желчных протоков у новорожденных детейАтрезия желчных протоков является конечным результатом деструктивного, воспалительного или идиопатического процесса с вовлечением внепеченочных и внутрипеченочных желчных протоков, приводящего к облитерации желчных протоков и циррозу. Атрезия желчевыводящих путей — наиболее частая причина хронического холестаза у новорожденных и детей в первые месяцы жизни, которая встречается с частотой 1:8000-1:12 000 среди живорожденных. Большинство младенцев с атрезиеи желчных протоков при рождении выглядят здоровыми, прогрессирующая желтуха развивается в первые недели жизни. У некоторых детей дисфункция печени отмечается сразу после рождения, возможно вследствие нарушенного эмбриогенеза. У таких детей описаны синдромальная, фетальная и эмбриональная формы атрезии желчных протоков. Эти формы составляют 10-15% всех случаев атрезии. Фетальная форма у 20% новорожденных сопровождается другими врожденными аномалиями, включая синдром полиспле-нии в сочетании с дефектами сердечно-сосудистой системы, обратное расположение органов брюшной полости и позиционные аномалии воротной вены и печеночной артерии. Несиндромальная форма атрезии желчных протоков (также называемая перинатальной или постнатальной формой атрезии) встречается примерно у 90% младенцев. Возникновение атрезии желчевыводящих путей после рождения не связано с аномалиями, такие случаи заставляют исследователей искать причину в действии внешних факторов, например токсинов или вирусов, на поздних сроках гестации или после рождения. Другими этиологическими факторами могут быть генетическая предрасположенность, нарушенная васкуляризация в фетальном и перинатальном периодах, частично или полностью нарушенный иммунный ответ на повреждающие факторы. Несмотря на проведенные в последнее время исследования, этиопатогенез атрезии желчных протоков остается неясным. Например, экспрессия мРНК с использованием микрочипа кДНК на РНК, выделенной из печени пациентов с атрезией желчных протоков, выявила, что генные профили позволяют отличить детей с конечной стадией атрезии от здоровых и тех, у кого есть заболевание печени. Профили генной экспрессии были связаны с сигнальными клетками, регуляцией транскрипции и морфофиброгенезом печени. Гены с повышенной экспрессией включали в процесс коллагены I, III, IV, VI и протеогликан (принимающий участие в фиброзе печени) в дополнение к остеонектину и металлопротеиназам (значимым для организации и деструкции внеклеточного матрикса). Результаты исследований позволяют предположить, что управление патогенезом атрезии желчных протоков происходит путем сложного взаимодействия воспалительного процесса с морфологическими и фиброгенными факторами. У новорожденных с эмбриональной атрезией желчных протоков другой анализ микрочипов комплементарной РНК выявил характерную клиническую фенотипическую экспрессию регуляторных генов в дополнение к избыточной экспрессии некоторых маркерных генов. Результаты этого небольшого клинического исследования свидетельствуют о несостоятельности регуляции эмбриональных генных программ в ходе созревания гепатобилиарной системы. Эти данные могут служить подтверждением транскрипционной основы патогенеза эмбриональной атрезии, имеющей особое значение из-за высокой частоты побочных дефектов у этой редкой формы атрезии желчных протоков.
Алгоритмы диагностики холестаза полезны для исключения более частых причин прямой гипербилирубинемии. Гистологическое исследование биоптатов печени может выявить классические признаки атрезии желчевыводящих путей: холестаз, пролиферацию мелких желчных протоков, отек в области ворот печени и воспалительную нейтрофильную инфильтрацию. К скрининговым исследованиям, позволяющим получить изображение гепатобилиарной системы, относят радионуклидную сцинтиграфию (IDA-сканеры, использующие меченную технецием-99m иминодиуксусную кислоту), магнитно-резонансную холангиографию и УЗИ. Для диагностики атрезии желчных протоков была предложена эндоскопическая ретроградная холангиография, но лишь немногие центры имеют соответствующее оборудование или навыки для выполнения этого более сложного исследования у детей. Проведение ранней диагностической лапаротомии с интраоперационной холангиографией при предполагаемой атрезии желчевыводящих путей может предотвратить нежелательную задержку в выполнении соответствующего хирургического вмешательства. Без хирургического лечения атрезия желчных протоков приводит к прогрессирующему нарушению функции печени и смерти ребенка в первые годы жизни. Раньше наилучший краткосрочный прогноз имели те дети с атрезией желчных протоков, которым была проведена операция квалифицированным хирургом, имеющим опыт работы в микрохирургии желчевыводящих путей. Тем не менее в целом выживаемость детей с атрезией желчных протоков увеличилась, когда наряду с печеночной портоэнтеростомией (по Касаи) стали проводить трансплантацию печени. Обычно успешность портоэнтеростомии определяется восстановлением тока желчи и последующей нормализацией уровня билирубина в сыворотке крови. При описании исходов операций результаты исследований других функций печени встречаются не так часто. Прогноз улучшения тока желчи после операции в большей степени зависит от срока проведения хирургического вмешательства и опыта хирурга в выполнении портоэнтеростомии по Касаи. Подтвержден краткосрочный положительный эффект этого вмешательства, однако 80-90% детей с атрезией желчевыводящих путей все равно понадобится трансплантация печени. Возраст ребенка более 60 дней на момент проведения операции относится к прогностическим факторам плохого исхода, хотя существуют аргументы в защиту того, что попытки восстановить ток желчи при атрезии желчных протоков должны быть предприняты, даже если возраст ребенка превышает 60-90 дней. Хотя операция Касаи имеет плохой долгосрочный прогноз, она позволяет отложить проведение трансплантации печени до того момента, пока ребенок не станет старше, что дает больше времени для поиска подходящего донора. К другим неблагоприятным прогностическим факторам относят наличие данных о циррозе при первичной биопсии, отсутствие желчных протоков в поперечнике ворот печени и возникновение варикоза или асцита в динамике. Понятно, что по сути паллиативная операция портоэнтеростомии играет комплементарную, ограниченную неблагоприятным отсроченным прогнозом роль в лечении большинства детей с атрезией желчных протоков. Знание факторов, определяющих прогноз, позволяет своевременно направлять пациентов с атрезией желчных протоков на трансплантацию печени (как правило, излечивающую операцию). Отдаленные исходы после трансплантации печени у детей с атрезией желчных протоков очень хорошие. Среди 1976 детей, перенесших первичную ортотопическую трансплантацию печени в связи с атрезией желчных протоков в США с 1988 по 2003 г., 5- и 10-летняя актуарная выживаемость составила более 87 и 85% соответственно. У детей, которым проводили операцию по пересадке части печени от живого донора (вместо органа, взятого у трупа), 5-летняя актуарная выживаемость увеличивалась до 98%. Другими факторами, определяющими лучший прогноз по выживаемости детей, перенесших трансплантацию печени, являются возраст ребенка старше 1 года и отсутствие необходимости поддерживать работу жизненно важных органов ко времени проведения операции. Также большей выживаемости можно добиться при совершенствовании хирургической техники, проведении антимикробной химиопрофилактики и терапии, а также адекватной иммуносупрессии. — Также рекомендуем «Гипоплазия желчных протоков и киста общего желчного протока у новорожденных детей» Оглавление темы «Желтуха у новорожденных детей»:
|